Clear Sky Science · es
La señalización de interferón tipo I define una firma patológica novedosa en queratinocitos humanos con xeroderma pigmentoso C
Por qué la luz solar puede ser tan peligrosa para algunas personas
Para la mayoría de nosotros, la luz solar significa calor y vitamina D. Pero para las personas con una rara condición genética llamada xeroderma pigmentoso C (XP‑C), incluso la luz diurna moderada puede provocar daños cutáneos graves y un riesgo extremo de cáncer de piel. Este estudio va más allá del conocido problema de la reparación del ADN en XP‑C y descubre una capa oculta de señalización tipo inmune sobreactivada dentro de sus células de la piel, aportando nuevas pistas sobre por qué su piel es tan vulnerable e inflamada tras la exposición solar.
Cuando la reparación del ADN falla en la piel
Nuestras células cutáneas reparan constantemente el daño del ADN causado por los rayos ultravioleta B (UVB) del sol. Una proteína llamada XPC es uno de los primeros “sensores” que detecta las lesiones inducidas por UV y moviliza un gran equipo de reparación. En XP‑C, las mutaciones en el gen XPC incapacitan este paso de alerta temprana, de modo que el daño por UV se acumula en lugar de corregirse. Los pacientes con XP‑C desarrollan cánceres de piel miles de veces más frecuentemente que la población general y deben evitar la luz solar con rigor. Aunque este defecto en la reparación del ADN es bien conocido, cómo reprograma los sistemas de comunicación internos de las células —especialmente los que controlan la inflamación— ha sido mucho menos claro.
Inspeccionando las señales celulares a lo largo del tiempo
Para abordar este problema, los investigadores modificaron queratinocitos humanos —las células principales de la capa externa de la piel— para que carecieran por completo de XPC, y los compararon con células normales idénticas en lo demás. Expusieron ambos tipos celulares a un nivel de UVB cuidadosamente elegido, realista y similar a una quemadura solar moderada. Luego examinaron las células en dos etapas. Una hora tras la irradiación, midieron la actividad de muchas enzimas llamadas tirosina quinasas de proteínas, que activan o desactivan señales añadiendo pequeños grupos fosfato. Veinticuatro horas después, usaron espectrometría de masas avanzada para obtener una instantánea amplia de miles de proteínas y ver cuáles aumentaban o disminuían en abundancia. Este enfoque en dos pasos les permitió rastrear tanto las “alarmas” tempranas como las respuestas “a valle” posteriores dentro de las células.
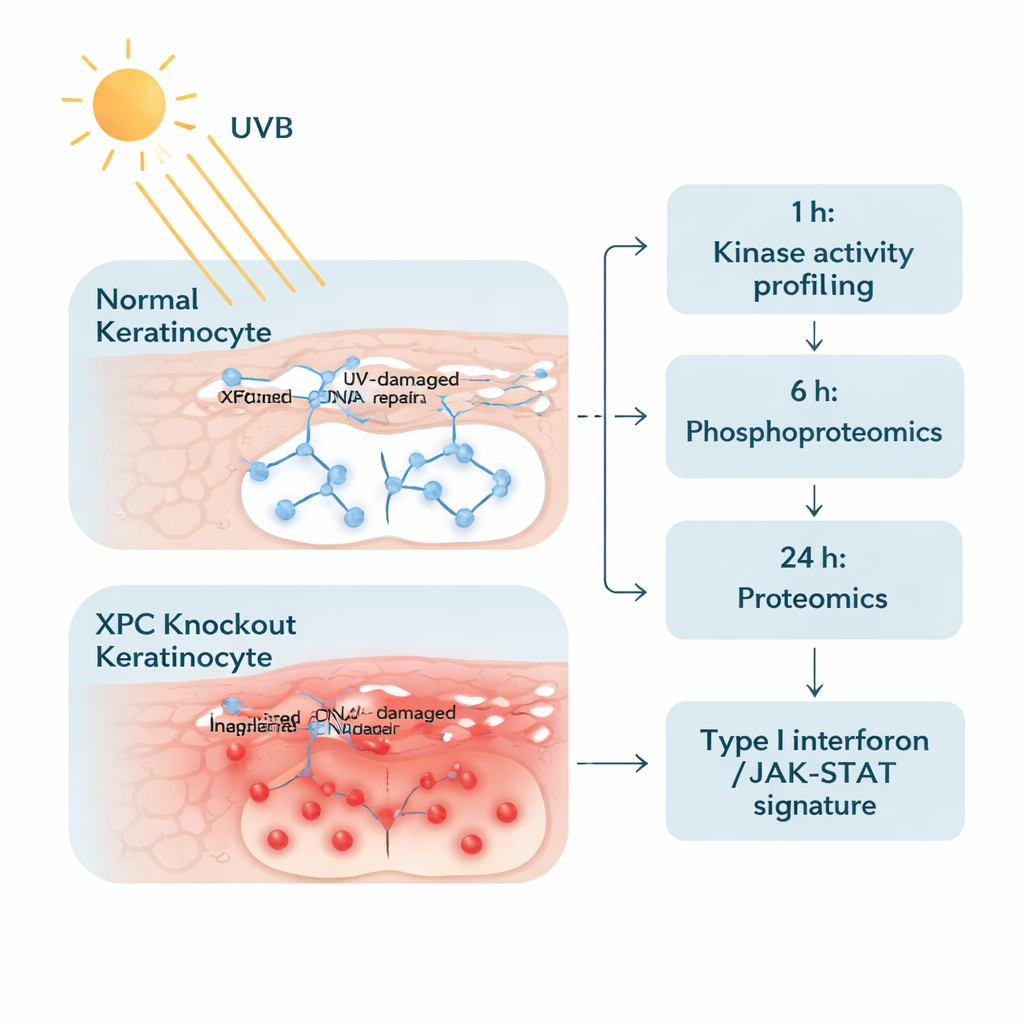
Se enciende una vía inflamatoria
El cribado temprano de quinasas reveló que los queratinocitos deficientes en XPC responden al UVB con un aumento de la fosforilación en más de un centenar de sitios en comparación con células normales. Notablemente, muchos de estos cambios se agruparon en la vía de señalización JAK/STAT —una ruta de comunicación central habitualmente utilizada por mensajeros inmunitarios como los interferones. Marcadores vinculados a JAK1, JAK2, JAK3, TYK2 y proteínas STAT estaban más activos en las células XP‑C, incluso antes del UVB, y se potenciaron tras la irradiación. Esto sugiere que las células estaban preparadas en un estado de “alta alerta”, listas para amplificar mensajes inflamatorios siempre que encontraran estrés inducido por UV.
Genes de alarma tipo interferón en células de la piel
La posterior y más amplia investigación proteómica confirmó y amplió este panorama. En las células con supresión de XPC, especialmente tras el UVB, se alteraron cientos de proteínas, y un gran grupo se correspondió con genes normalmente activados por interferones de tipo I —las mismas señales antivirales que usa el organismo para combatir infecciones. Proteínas como MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 e IRF9, clásicas “genes estimulados por interferón”, estaban fuertemente elevadas. Los análisis de redes y vías relacionaron estas proteínas de nuevo con JAK/STAT y señalización de interferón tipo I como tema dominante. Experimentos de western blot posteriores confirmaron que proteínas STAT clave estaban más fosforiladas y que estas proteínas responsivas al interferón se producían a niveles muy superiores en células XP‑C que en queratinocitos normales, tanto en reposo como, especialmente, tras la exposición a UVB.
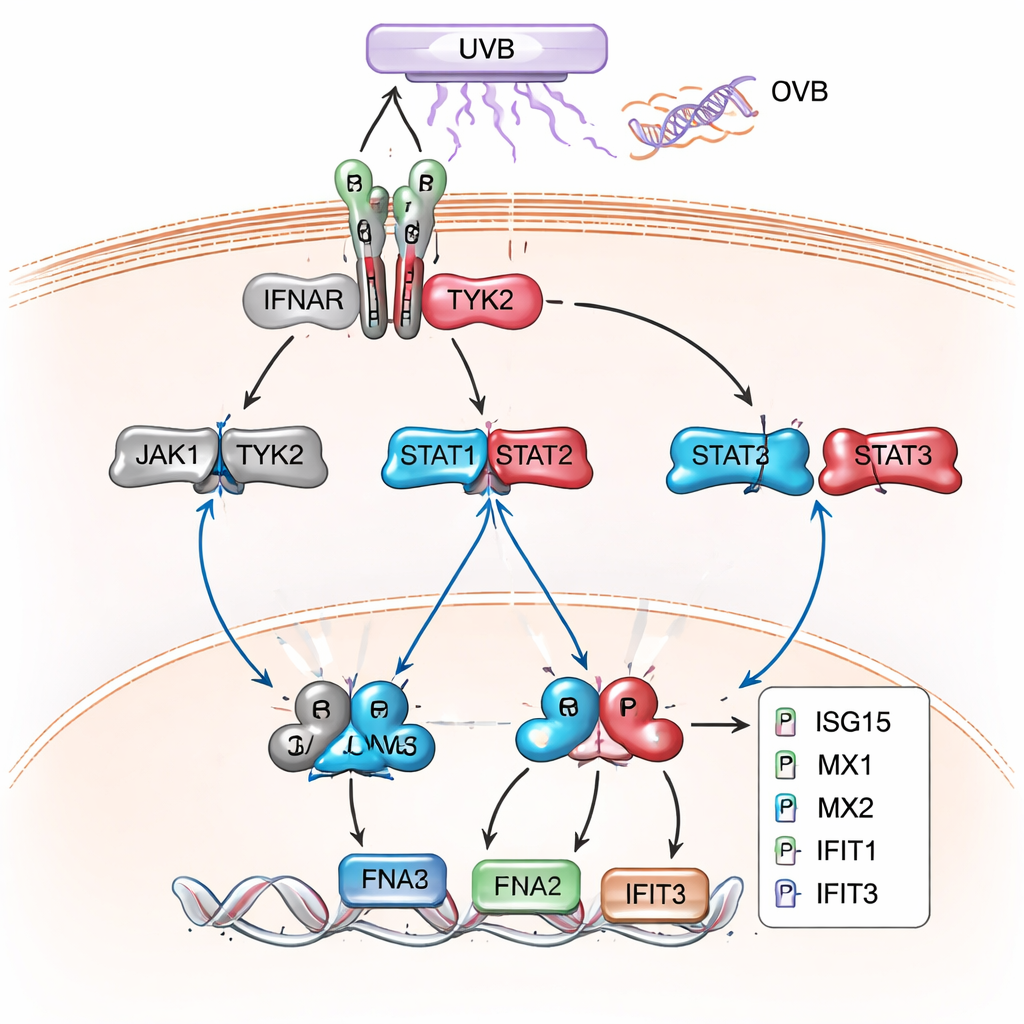
Qué significa esto para los pacientes y los tratamientos futuros
En conjunto, estos resultados muestran que XP‑C no es solo una enfermedad de reparación defectuosa del ADN; también se caracteriza por un estado inflamatorio persistente similar al inducido por interferón dentro de las células de la piel, impulsado por la vía JAK/STAT e intensificado por la luz UV. Para un lector no especializado, esto significa que los queratinocitos de XP‑C se comportan como si estuvieran constantemente combatiendo una infección invisible cada vez que ven la luz solar, superponiendo inflamación crónica al daño del ADN no reparado. Aunque el estudio no prueba tratamientos directamente, plantea la posibilidad de que fármacos cuidadosamente ajustados que apunten a JAK/STAT u otros circuitos inflamatorios relacionados puedan algún día ayudar a reducir el daño desencadenado por UV en XP‑C y, quizás, en otras afecciones inflamatorias de la piel que comparten esta firma molecular.
Cita: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Palabras clave: xeroderma pigmentoso, cáncer de piel, reparación del ADN, señalización por interferón, vía JAK STAT