Clear Sky Science · es
Wnt-3a agrava la producción de TNF-α en microglía estimulada con LPS independientemente de la vía canónica β-catenina
Por qué importa la inflamación cerebral
Muchos trastornos cerebrales, incluida la enfermedad de Parkinson, se sabe que implican inflamación crónica. En este proceso, las células inmunitarias residentes del cerebro, llamadas microglía, pueden pasar de ser ayudantes protectores a atacantes sobreactivados que dañan a las neuronas cercanas. Este estudio plantea una pregunta oportuna: ¿puede una molécula de señalización llamada Wnt‑3a, durante mucho tiempo considerada con efectos calmantes y protectores, empeorar en realidad la inflamación en determinadas condiciones? La respuesta resulta ser más compleja de lo esperado y subraya por qué la misma molécula puede ser útil en un contexto y perjudicial en otro.
Un mensajero con dos caras
Las proteínas Wnt son una familia de mensajeros químicos que ayudan a guiar el desarrollo cerebral, mantienen las células cerebrales en la edad adulta y modulan cómo responden las células a las lesiones. Uno de los miembros mejor estudiados, Wnt‑3a, suele asociarse con una vía de señalización “canónica” que estabiliza una proteína llamada β‑catenina dentro de las células. En muchos sistemas, activar esta vía parece atenuar la inflamación y favorecer la supervivencia neuronal, por lo que algunos investigadores se han preguntado si aumentar Wnt‑3a podría proteger a las neuronas productoras de dopamina vulnerables en la enfermedad de Parkinson. Sin embargo, las proteínas Wnt también pueden señalizar a través de rutas alternativas “no canónicas” que pueden, en cambio, promover la inflamación, y la vía que domina puede depender del tipo celular y de su estado.
Cuando las células en calma permanecen calmas
Para explorar estas posibilidades, los investigadores estudiaron microglía primaria cultivada a partir de cerebros de ratón. Primero observaron microglía en un estado de reposo homeostático y las expusieron solo a Wnt‑3a. En estas condiciones tranquilas, Wnt‑3a no aumentó la liberación de moléculas inflamatorias clave como TNF‑α o IL‑1β. Aunque se activó cierta señalización dentro de las células, la microglía no cambió a un modo fuertemente inflamatorio. Esto sugiere que en un cerebro sano y no inflamado, añadir Wnt‑3a por sí solo puede tener poco impacto directo sobre la producción inflamatoria microglial.
Cuando las células inflamadas se empujan más
El panorama cambió drásticamente una vez que se activó primero la microglía en un estado inflamatorio usando lipopolisacárido bacteriano (LPS), una herramienta estándar de laboratorio para simular infección. Como era de esperar, el LPS por sí solo generó un aumento notable en la producción de TNF‑α. Pero cuando se añadió Wnt‑3a junto con LPS, la microglía liberó significativamente más TNF‑α que con LPS solo, mientras que IL‑1β no aumentó más. Medidas detalladas mostraron que este aumento de TNF‑α no provenía de una mayor activación de la vía inflamatoria habitual NFκB ni de una activación extra de la vía canónica de β‑catenina. Bloquear la vía de β‑catenina con una proteína llamada DKK1 dejó intacto el aumento de TNF‑α inducido por Wnt‑3a, lo que indica que la vía “antiinflamatoria” esperada no era la responsable.
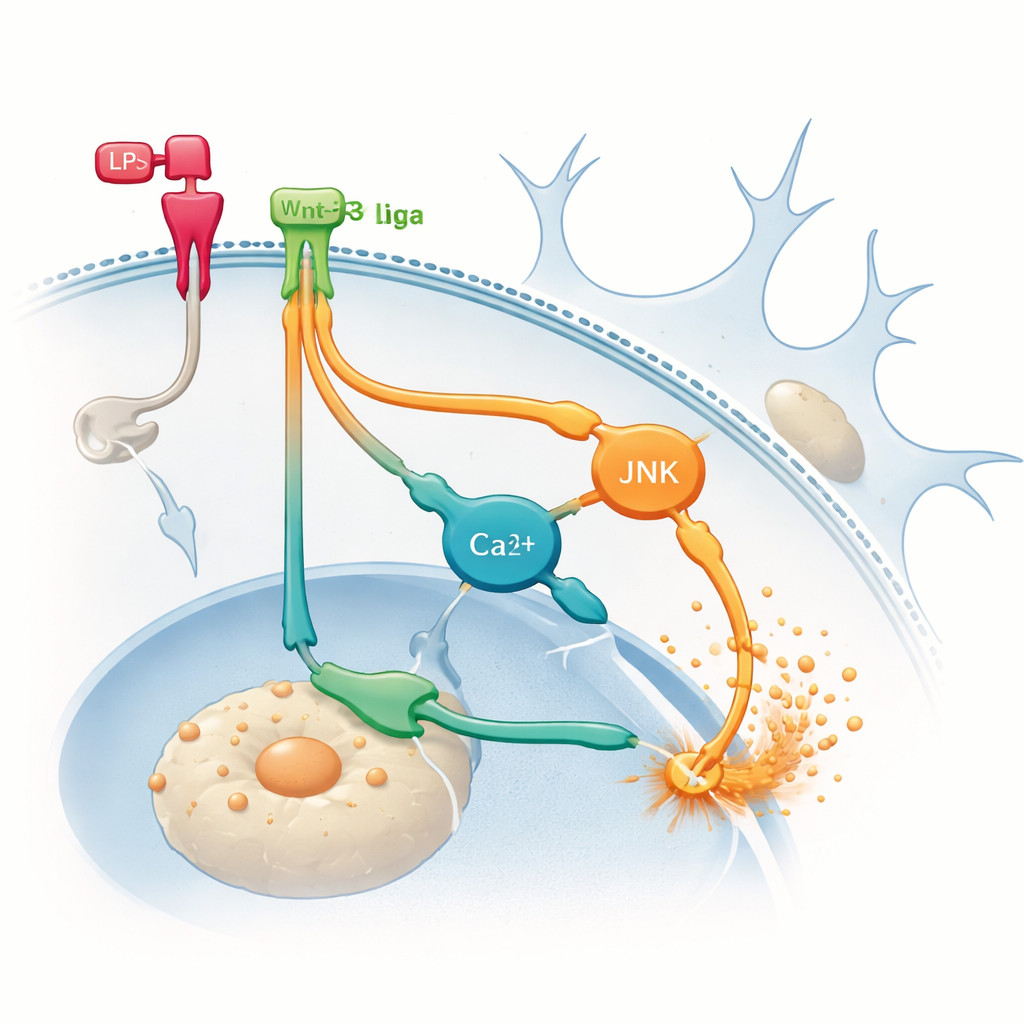
Rutas ocultas que avivan las llamas
Para localizar de dónde procedía la inflamación adicional, el equipo se enfocó en las rutas alternativas no canónicas que las Wnt pueden usar. Bloquearon farmacológicamente dos ramas de señalización dentro de la microglía: una que involucra una proteína llamada JNK y otra ligada a cambios en los niveles de calcio dentro de la célula. Inhibir cualquiera de las dos ramas redujo la producción de TNF‑α inducida por LPS y, lo que es importante, evitó que Wnt‑3a aumentara todavía más el TNF‑α. Estos resultados sugieren que, una vez que la microglía ya está inflamada, Wnt‑3a puede cambiar a usar predominantemente rutas no canónicas que amplifican las señales inflamatorias en lugar de calmarlas. En otras palabras, el mismo mensajero puede tomar una senda interna diferente según el estado inicial de la célula, con resultados muy distintos.
Pruebas en un modelo de Parkinson
Los investigadores preguntaron luego si este comportamiento de Wnt‑3a en microglía se traduciría en efectos mayores sobre las neuronas en un cerebro vivo. Infundieron Wnt‑3a directamente en los ventrículos cerebrales de ratones tratados con la toxina MPTP, un modelo ampliamente usado de daño tipo Parkinson a las neuronas dopaminérgicas y activación microglial. Como era de esperar, MPTP redujo el número de neuronas dopaminérgicas e incrementó el número de microglía en una región del mesencéfalo crítica para el movimiento. Sin embargo, la administración adicional de Wnt‑3a no empeoró más la pérdida neuronal ni cambió significativamente el recuento microglial en comparación con los animales tratados con vehículo. En este entorno in vivo complejo, Wnt‑3a no rescató ni agravó claramente los efectos dañinos de la toxina durante el periodo estudiado.
Qué significa esto para futuras terapias
En conjunto, el estudio muestra que Wnt‑3a no es un interruptor simple de encendido/apagado para la inflamación cerebral. En microglía en reposo tiene poco efecto, pero en células ya inflamadas puede aumentar selectivamente la liberación de TNF‑α a través de rutas de señalización no canónicas, independientemente de la vía clásica de β‑catenina. Al mismo tiempo, añadir Wnt‑3a en un modelo murino parecido a Parkinson no protegió ni dañó claramente a las neuronas dopaminérgicas a corto plazo. Para quienes trabajan en futuras terapias, el mensaje clave es que dirigir la señalización Wnt exigirá una apreciación cuidadosa del contexto celular. Las terapias basadas en Wnt‑3a o moléculas relacionadas pueden ayudar en algunas situaciones, pero podrían resultar contraproducentes en otras si intensifican inadvertidamente la inflamación perjudicial.
Cita: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Palabras clave: inflamación cerebral, microglía, señalización Wnt, enfermedad de Parkinson, TNF-alfa