Clear Sky Science · es
Actividad potenciada de meropenem por un péptido derivado del microbioma que apunta a la carbapenemasa oxacillinasa 48 en aislados de Klebsiella pneumoniae resistentes a carbapenémicos
Por qué esto importa para la salud cotidiana
La resistencia a los antibióticos está volviendo infecciones antes tratables más difíciles y, en ocasiones, imposibles de curar, especialmente en entornos hospitalarios. Este estudio explora una forma nueva de “rearmar” un antibiótico de último recurso ya existente, el meropenem, contra una bacteria peligrosa llamada Klebsiella pneumoniae que con frecuencia infecta a pacientes en unidades de cuidados intensivos. En lugar de inventar un fármaco completamente nuevo, los investigadores prueban una pequeña molécula auxiliar, un péptido procedente del microbioma humano, que desactiva una de las principales herramientas de resistencia de la bacteria para que el meropenem pueda volver a funcionar.
Un germen hospitalario persistente y su escudo químico
Klebsiella pneumoniae es una causa común de neumonía, infecciones sanguíneas e infecciones del tracto urinario en pacientes hospitalizados. Algunas cepas se han vuelto resistentes a los carbapenémicos, una potente clase de antibióticos que los médicos reservan normalmente para casos graves y difíciles de tratar. Muchas de estas bacterias producen una enzima especial llamada OXA-48, que actúa como un escudo químico que descompone los fármacos carbapenémicos antes de que puedan matar al microbio. En el Medio Oriente, incluida Irán, las cepas productoras de OXA-48 están especialmente extendidas, y las opciones de tratamiento se reducen a medida que aparece resistencia incluso a combinaciones de fármacos más nuevas. Esto ha convertido a OXA-48 en un objetivo prioritario para nuevas terapias.
Diseñando un péptido ayudante a partir del microbioma humano
Los investigadores utilizaron previamente modelos informáticos para rastrear bases de datos de péptidos antimicrobianos naturales humanos—fragmentos cortos de proteínas producidos por nuestro propio organismo y microbios residentes—en busca de candidatos que pudieran unirse firmemente a la enzima OXA-48. Mediante acoplamientos virtuales y largas simulaciones de dinámica molecular refinaron estos candidatos y seleccionaron uno, denominado M104, que se predijo se uniría de forma estable al sitio activo de la enzima y bloquearía su función manteniéndose soluble en agua y químicamente estable. En este estudio, pusieron a prueba M104 en el laboratorio, combinándolo con meropenem contra 20 aislados de Klebsiella obtenidos de pacientes: 10 que producían OXA-48 y eran resistentes a meropenem, y 10 que carecían de carbapenemasas y eran sensibles a los fármacos.
Hacer que un antibiótico viejo vuelva a funcionar
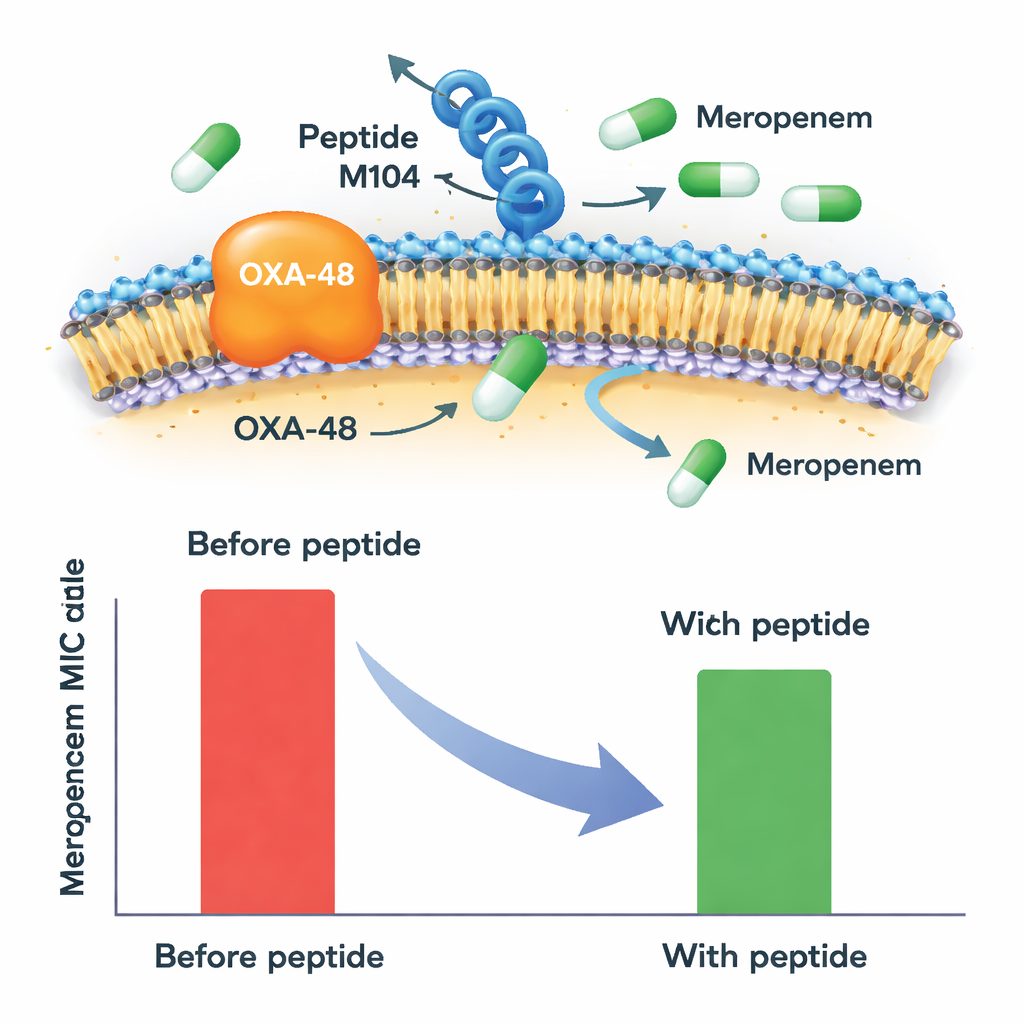
Cuando se usó meropenem solo, todos los aislados de Klebsiella positivos para OXA-48 fueron claramente resistentes. La adición del péptido M104 cambió ese panorama. En su nivel más alto probado, M104 redujo la cantidad de meropenem necesaria para detener el crecimiento bacteriano al menos a la mitad—y en algunos casos hasta seis veces—para todos los productores de OXA-48 resistentes analizados. Esto hizo que muchas cepas pasaran de claramente resistentes a un rango intermedio o incluso sensible, según los umbrales clínicos aceptados. Es importante destacar que M104 no mostró efecto bactericida por sí mismo y no potenció el meropenem cuando las bacterias carecían de la enzima OXA-48, lo que apunta a una acción muy específica sobre ese mecanismo de resistencia en lugar de una toxicidad amplia y no selectiva.
Desafíos con biopelículas viscosas y comprobaciones de seguridad
Muchas infecciones hospitalarias implican biopelículas—comunidades bacterianas en capas y viscosas que se adhieren a dispositivos y tejidos y son mucho más difíciles de erradicar que las células en suspensión. El equipo, por tanto, probó si M104 podía ayudar al meropenem a prevenir la formación de biopelículas o a eliminar las ya establecidas en cepas de Klebsiella formadoras de biopelícula robustas. Aunque la combinación péptido-meropenem generalmente redujo a la mitad la cantidad de fármaco necesaria para bloquear el crecimiento de biopelículas o empezar a aclarar biopelículas maduras, estos efectos fueron modestos y no alcanzaron una significación estadística clara en esta muestra pequeña. En cuanto a la seguridad, M104 no mostró daño detectable a los glóbulos rojos humanos y no redujo la viabilidad de fibroblastos cutáneos humanos tras 24 horas a una concentración superior a la usada en las pruebas bacterianas; solo tras 48 horas la supervivencia celular descendió alrededor de un 10 por ciento. Las comparaciones de secuencia también sugirieron poco riesgo de que el péptido afecte accidentalmente a otras proteínas bacterianas o humanas.
Qué podría significar esto para tratamientos futuros
En conjunto, los hallazgos sugieren que el péptido M104 puede desactivar específicamente la enzima de resistencia OXA-48 y restaurar buena parte del efecto del meropenem contra Klebsiella pneumoniae que de otro modo serían intratables, al menos para bacterias en estado planctónico. Aunque su impacto en biopelículas establecidas y difíciles fue limitado en las condiciones probadas, el estudio presenta el primer bloqueador basado en péptidos reportado contra OXA-48 y demuestra que este tipo de ayudantes dirigidos puede ser efectivo y relativamente poco agresivo para las células humanas a corto plazo. Con pruebas adicionales en más cepas bacterianas, otros carbapenémicos, formulaciones optimizadas y modelos animales, este tipo de terapia adyuvante de precisión podría ayudar a prolongar la vida útil de nuestros antibióticos más potentes en lugar de dejar a los médicos ante infecciones resistentes con una caja de herramientas vacía.
Cita: Sadeghi, S., Faramarzi, M.A. & Siroosi, M. Enhanced meropenem activity by a microbiome derived peptide targeting oxacillinase 48 carbapenemase in carbapenem resistant Klebsiella pneumoniae isolates. Sci Rep 16, 7589 (2026). https://doi.org/10.1038/s41598-026-37644-2
Palabras clave: resistencia a antibióticos, Klebsiella resistente a carbapenémicos, enzima OXA-48, meropenem, inhibidores peptídicos