Clear Sky Science · es
Caracterización in vitro del dominio catalítico de la histona deacetilasa 5 humana
Por qué importan los pequeños interruptores en el empaquetado de nuestro ADN
Dentro de cada célula, nuestro ADN está envuelto alrededor de proteínas que actúan como carretes, ayudando a acomodar metros de material genético en un espacio microscópico. Que un gen esté activo o reprimido depende con frecuencia de pequeñas etiquetas químicas en estas proteínas carrete. Este estudio se centra en un «interruptor» proteico específico llamado HDAC5, asociado con enfermedades cardíacas, trastornos cerebrales, cáncer y más. Al entender cómo funciona HDAC5 a nivel molecular, los investigadores esperan allanar el camino para fármacos más precisos con menos efectos secundarios.
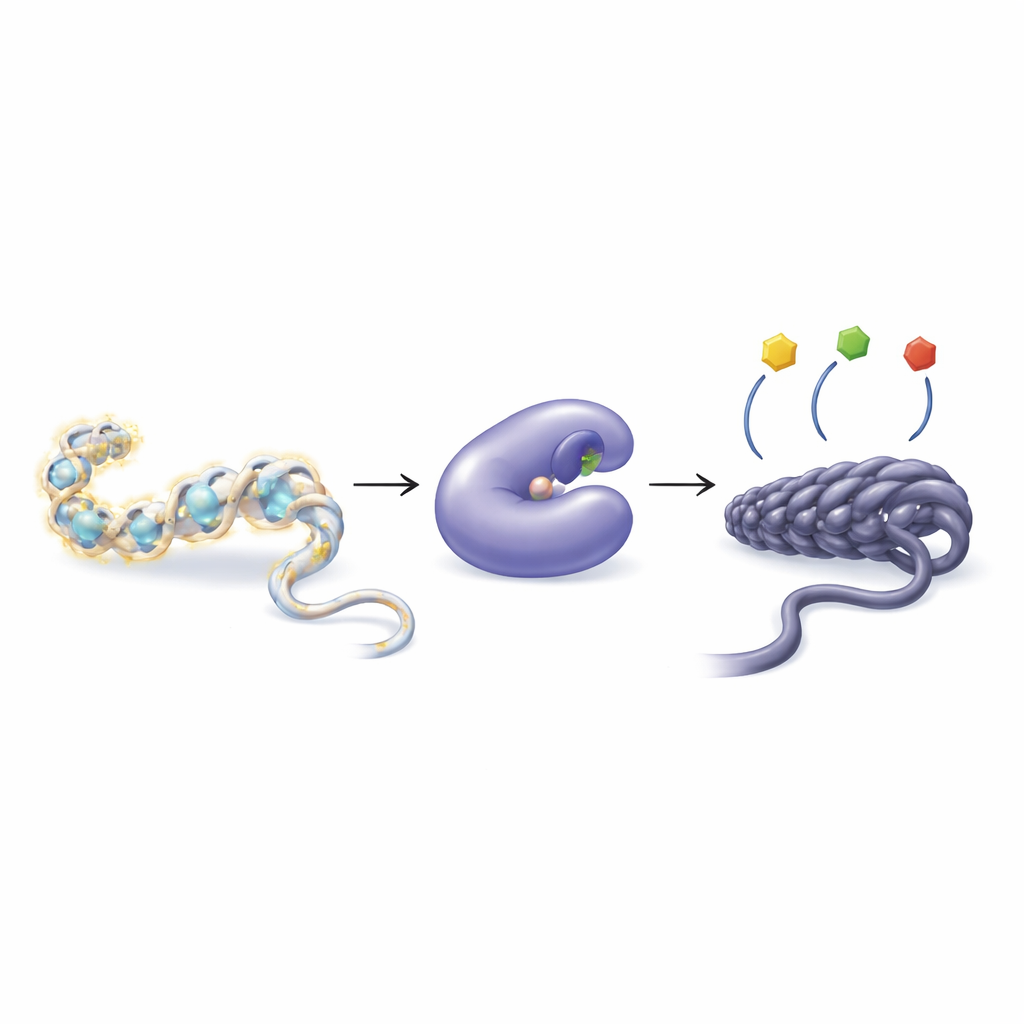
Cómo las células regulan los genes con pequeñas etiquetas químicas
Nuestro ADN no flota libremente sino que se enrolla alrededor de proteínas llamadas histonas, formando una estructura conocida como cromatina. Las células pueden añadir o eliminar pequeños grupos químicos, como grupos acetilo, de las colas de las histonas para aflojar o apretar la cromatina. Un empaquetamiento más laxo generalmente facilita la lectura de los genes; uno más compacto tiende a silenciarlos. Dos grupos de enzimas gestionan este equilibrio: las histona acetiltransferasas añaden grupos acetilo, mientras que las histona deacetilasas (HDAC) los eliminan. Cuando este equilibrio se altera, puede contribuir a una amplia variedad de enfermedades, incluyendo cáncer, problemas cardíacos, pérdida muscular y trastornos inmunitarios.
Por qué HDAC5 es un objetivo farmacológico prometedor pero complejo
Las HDAC forman una gran familia de enzimas relacionadas divididas en varias clases. Muchos de los fármacos actualmente en uso clínico bloquean varios tipos de HDAC a la vez, lo que puede inhibir funciones normales importantes y causar efectos secundarios severos. Las HDAC de la clase IIa, entre ellas HDAC5, destacan porque se concentran en tejidos específicos como el cerebro, el corazón y el músculo esquelético, y actúan en conjunto con otras proteínas para regular redes génicas clave. HDAC5 a menudo funciona como un puente, llevando una enzima socia altamente activa (HDAC3) a determinados genes para que la cromatina se compacte y esos genes queden silenciados. Debido a estos roles focalizados, HDAC5 se considera un objetivo atractivo para fármacos más selectivos, pero ha habido escasez de datos bioquímicos detallados y no existía una estructura de alta resolución de su núcleo activo, lo que dificulta el diseño racional de fármacos.
Reconstruir HDAC5 en un tubo de ensayo
Para abordar esta laguna, los investigadores produjeron solo el núcleo catalítico de la HDAC5 humana —la parte que realiza la reacción química— en bacterias, lo purificaron y confirmaron que forma una proteína estable y monomérica en solución. Luego evaluaron su actividad bajo distintos niveles de sal y acidez. La actividad de HDAC5 se mantuvo robusta en un amplio rango de sal y alcanzó su máximo en condiciones ligeramente básicas, similares a las del interior de muchas células. Usando moléculas fluorescentes especiales como sustratos de prueba, encontraron que la forma natural de HDAC5 reconoce solo un tipo particular de sustrato comúnmente utilizado para sondear enzimas de la clase IIa. Guiados por trabajos previos en HDAC relacionadas, intercambiaron un solo aminoácido (histidina) por una tirosina en un sitio crítico. Sorprendentemente, este pequeño cambio permitió que la versión mutante de HDAC5 procesara eficientemente ambos tipos de sustratos de prueba, revelando cómo un único residuo en el sitio activo dirige las preferencias químicas de la enzima.
Probar y comparar dos nuevos candidatos a fármacos
El equipo examinó a continuación dos moléculas experimentales que bloquean HDAC5, conocidas como NT160 y FFK24. Estos compuestos usan un grupo quelante de zinc más nuevo que evita parte de la toxicidad y la mala selectividad observadas con los fármacos más antiguos basados en hidroxamato. Midiendo cómo cada inhibidor reducía la actividad de HDAC5 en reacciones cuidadosamente controladas, los autores determinaron constantes de inhibición extremadamente bajas en el rango de nanomolar, lo que significa que ambos compuestos se unen firmemente a la enzima. NT160 se unió de forma consistente aproximadamente diez veces con más afinidad que FFK24. Para entender por qué, los investigadores usaron acoplamiento por ordenador (docking) con una estructura del núcleo de HDAC5 predicha por AlphaFold. Ambos inhibidores compartían una región frontal común que se alojaba en lo profundo del bolsillo activo y contactaba con el ion metálico, pero la cola de NT160 establecía contactos estabilizadores adicionales con aminoácidos específicos del bolsillo. Estas interacciones adicionales probablemente expliquen su mayor potencia.
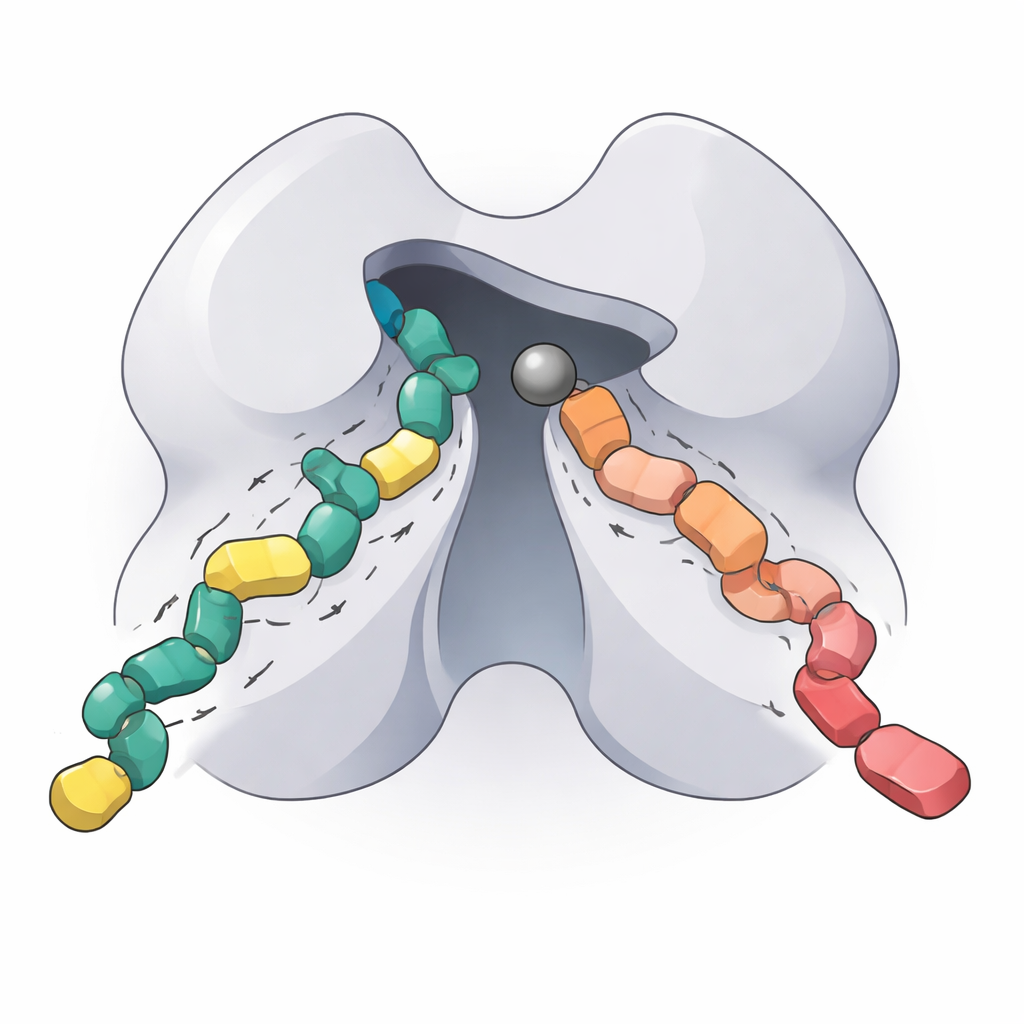
Qué significa esto para futuras terapias dirigidas
Al recomponer el núcleo funcional de HDAC5, mapear sus condiciones óptimas de trabajo, desentrañar cómo un cambio de un solo aminoácido altera su comportamiento y cuantificar cómo se unen dos inhibidores de nueva generación, este estudio ofrece una «huella» bioquímica detallada de una enzima importante pero hasta ahora poco caracterizada. Para el público general, la conclusión clave es que HDAC5 ayuda a controlar si ciertos genes están activados o desactivados, y que ajustar con precisión este interruptor podría ser valioso para tratar enfermedades cardíacas, neurodegenerativas, cáncer y trastornos inmunitarios. Los nuevos conocimientos y herramientas presentados aquí deberían ayudar a los investigadores a diseñar fármacos selectivos para HDAC5 y la clase IIa que actúen donde se necesitan, minimizando los efectos indeseados en otras partes del cuerpo.
Cita: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Palabras clave: histona deacetilasa 5, regulación epigenética, inhibidores de HDAC, terapia contra el cáncer dirigida, estructura de la cromatina