Clear Sky Science · es
Modelo para la descripción de las interacciones entre elagitaninos e iones Fe(II)
Por qué importan los compuestos vegetales en los piensos animales
Las bacterias resistentes a los antibióticos son una preocupación creciente tanto para los ganaderos como para la salud pública. Muchos de estos microbios difíciles de tratar surgen en el ganado, donde los antibióticos siguen usándose en gran medida en los piensos. Este estudio examina los taninos —compuestos naturales de las plantas— como una alternativa prometedora. En particular, explica cómo un grupo especial de taninos procedentes de la madera de castaño puede capturar hierro de maneras que podrían ayudar a privar a las bacterias de un nutriente que necesitan con urgencia para crecer.
Defensas naturales escondidas en los árboles
Los taninos son moléculas vegetales amargas que confieren a los vinos tintos su astringencia y que se han usado durante siglos en el curtido del cuero y en la fabricación de tintas. Abundan en muchos piensos y alimentos y, en general, son seguros para animales y humanos. Algunos tipos, denominados elagitaninos, son especialmente interesantes porque poseen muchas “manos” químicas pequeñas que pueden engancharse a iones metálicos como el hierro. El extracto de madera de castaño, ya usado en piensos animales, contiene varios elagitaninos, incluidos dos grandes llamados roburina A y roburina D. Trabajos anteriores mostraron que parientes más simples de estos compuestos pueden enlazar hierro y quizá impedir que las bacterias accedan a este elemento esencial.
Privar a las bacterias de su metal favorito
Las bacterias no pueden prosperar sin hierro. Lo usan para impulsar la respiración, construir ADN y ejecutar muchas reacciones enzimáticas. En el intestino animal o en medios de cultivo, normalmente obtienen hierro mediante sus propias pequeñas moléculas captadoras de hierro. Los elagitaninos interfieren con este proceso formando complejos firmes con los iones de hierro, “bloqueando” efectivamente el metal para las bacterias. Los autores se centraron en el hierro en su forma Fe(II), que es el estado que los taninos capturan rápidamente en agua antes de oxidarse lentamente a Fe(III). Al aislar la roburina A y D del extracto de castaño y estudiarlas en soluciones cuidadosamente controladas, el equipo pudo seguir con qué eficacia estos grandes taninos extraen el hierro de la fase líquida.
Investigando cómo los taninos atrapan el hierro
Para entender los detalles, los investigadores examinaron primero cómo las roburinas ganan y pierden protones (un proceso llamado equilibrio ácido–base) cuando cambia el pH. Usando espectroscopía ultravioleta–visible, siguieron cómo cambiaba la absorción de luz de las roburinas a distintos niveles de pH. Estos cambios revelaron que la roburina A y la D se comportan de forma similar a sus parientes más pequeños vescalagina y castalagina, pero con aproximadamente el doble de sitios que pueden perder un protón y luego participar en la unión del hierro. A continuación, mezclaron taninos e hierro en distintas proporciones y de nuevo emplearon la absorción de luz para crear los llamados diagramas de Job, que muestran qué proporción de mezcla produce la mayor cantidad de complejo hierro–tanino. A partir de estos datos, concluyeron que cada molécula de roburina puede enlazar seis iones Fe(II), el doble de la capacidad de los elagitaninos más pequeños.
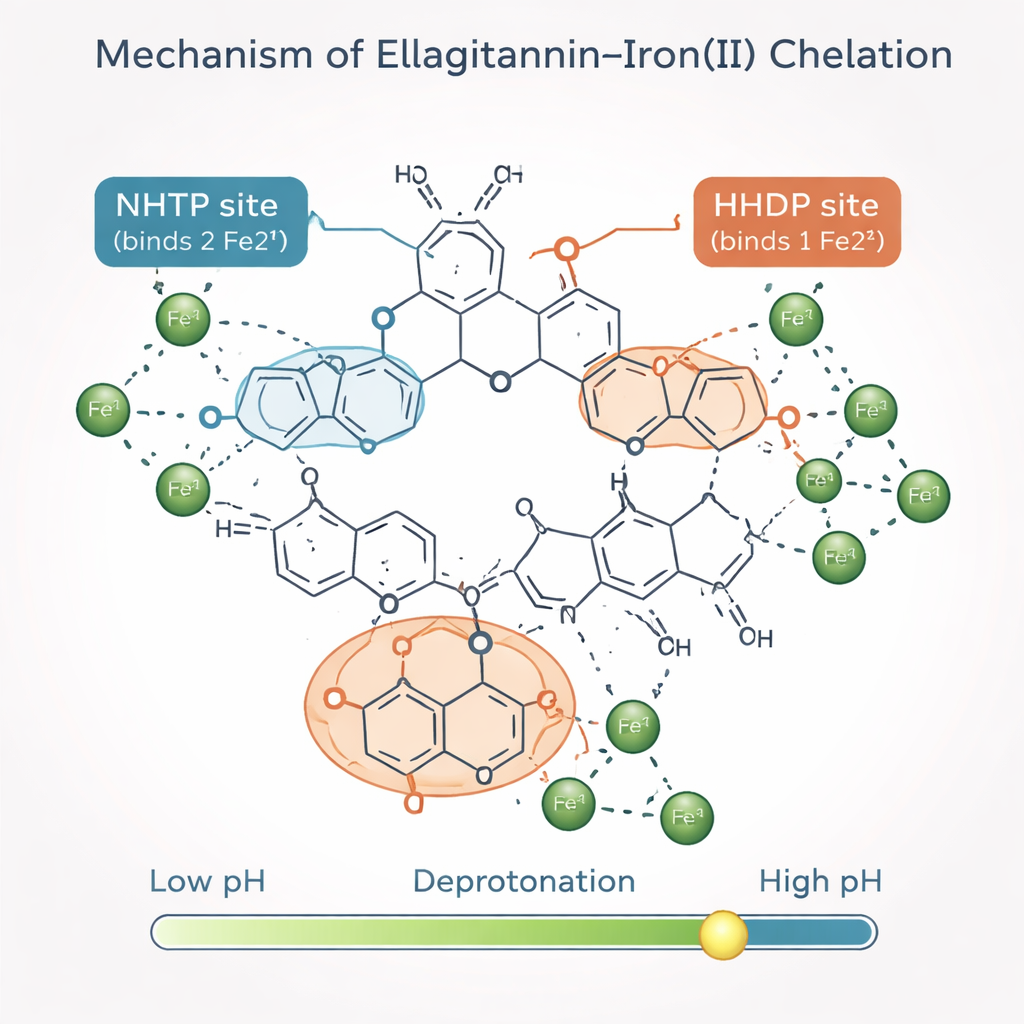
Un mapa predictivo de los puntos calientes de unión al hierro
Más allá de contar cuántos iones de hierro pueden capturarse, los autores quisieron saber qué “módulos” estructurales de los elagitaninos realizan el trabajo. Construyeron un modelo matemático que trata cada molécula de elagitanino como una colección de bloques repetitivos. Dos módulos clave, llamados grupos NHTP y HHDP, ofrecen cada uno sitios específicos de unión al hierro una vez que han perdido sus protones más ácidos. Combinando sus nuevas mediciones con datos previos de resonancia magnética nuclear y espectroscopía, el equipo demostró que cada grupo NHTP normalmente une dos iones de hierro, mientras que cada grupo HHDP une uno. Con apenas unos pocos parámetros ajustables, su modelo reprodujo con precisión los diagramas de Job experimentales no solo para los elagitaninos más simples, sino también para las roburinas más grandes que no se usaron para entrenar el modelo.
Implicaciones para una agricultura más ecológica
En términos sencillos, este trabajo convierte la compleja química de los taninos y el hierro en un manual utilizable. Muestra que, contando las unidades NHTP y HHDP en un elagitanino, los científicos pueden predecir cuántos iones de hierro capturará una molécula dada en un rango de condiciones ligeramente ácidas. Dado que los extractos de castaño ricos en roburinas secuestran más hierro que los taninos más pequeños o los ácidos vegetales simples, son candidatos fuertes para limitar el suministro de hierro disponible para bacterias intestinales dañinas en animales de granja. Aunque se necesita más investigación—especialmente sobre otras estructuras de taninos y sobre el hierro en diferentes formas—este modelo ayuda a orientar el diseño y la selección de aditivos vegetales para piensos que podrían reducir la dependencia de los antibióticos convencionales y favorecer una producción ganadera más sostenible y «más verde».
Cita: Frešer, F., Hostnik, G. & Bren, U. Model for the description of interactions between ellagitannins and Fe(II) ions. Sci Rep 16, 6631 (2026). https://doi.org/10.1038/s41598-026-37616-6
Palabras clave: elagitaninos, quelación de hierro, taninos en piensos animales, alternativas a los antibióticos, extracto de madera de castaño