Clear Sky Science · es
La inactivación de LIMK2 suprime la diferenciación de los fibroblastos dérmicos inducida por estimulación mecánica y la resistencia a la apoptosis
Por qué algunas cicatrices crecen sin control
La mayoría de los cortes y las heridas quirúrgicas dejan una línea delgada y plana. Pero en algunas personas, el proceso de curación se acelera en exceso, formando cicatrices gruesas y elevadas llamadas cicatrices hipertróficas o queloides, que pueden picar, doler y limitar el movimiento. Este estudio explora por qué las células cutáneas ordinarias a veces se convierten en formadoras de cicatrices hiperactivas y señala a un único interruptor molecular, llamado LIMK2, que podría atenuarse para evitar que las cicatrices crezcan sin control.
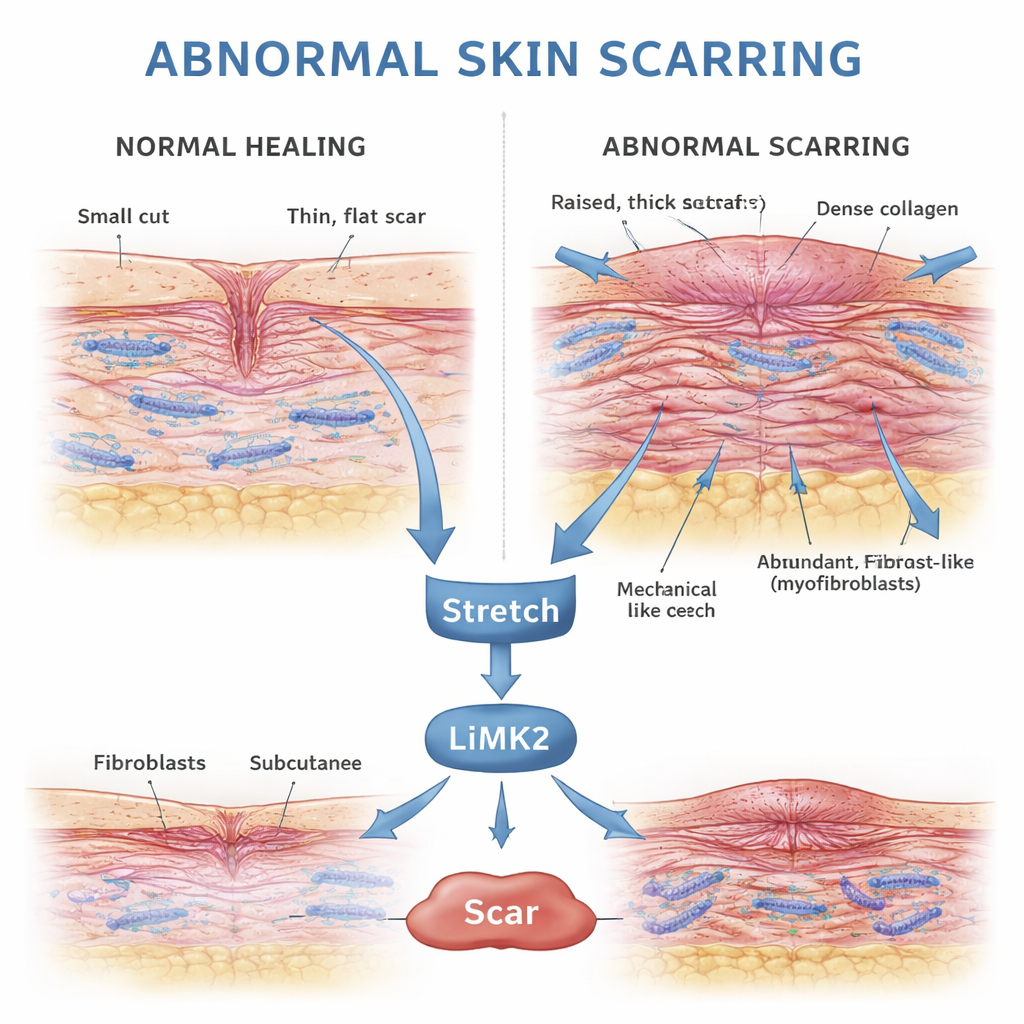
Cómo sana la piel normalmente tras una lesión
Cuando la piel se lesiona, el organismo pone en marcha un programa de reparación cuidadosamente cronometrado. Los fibroblastos —células obreras en la capa profunda de la piel— se desplazan hacia la herida, se multiplican y depositan colágeno, la estructura proteica del tejido nuevo. Muchos de estos fibroblastos se transforman temporalmente en una forma más fuerte y contráctil llamada miofibroblastos, que ayudan a aproximar los bordes de la herida. Una vez que la superficie está cerrada y el tejido nuevo se ha estabilizado, estos miofibroblastos deberían morir mediante un proceso controlado conocido como apoptosis, dejando tras de sí una cicatriz modesta y flexible.
Cuando las fuerzas cotidianas empeoran las cicatrices
Las cicatrices anormales suelen aparecer donde la piel está constantemente estirada —sobre el pecho, los hombros o la parte baja del abdomen. Esa observación ha llevado a los investigadores a sospechar que las fuerzas mecánicas, como el tirón y la tensión a lo largo de una herida en curación, pueden empujar a los fibroblastos a permanecer activos durante demasiado tiempo. Trabajos anteriores mostraron que estirar estas células en el laboratorio aumenta una proteína llamada α-SMA, un marcador de miofibroblastos, y activa genes que ayudan a las células a resistir la apoptosis. El nuevo estudio se centra en LIMK2, una pieza clave de una cadena de señalización mecánica dentro de las células que conecta el estiramiento físico con cambios en el armazón interno formado por filamentos de actina.
Un interruptor clave para las células formadoras de cicatrices
Para probar el papel de LIMK2, los investigadores usaron fibroblastos dérmicos humanos de piel normal y de tejido queloide. Introdujeron una versión inactivada de LIMK2 en algunas células, dejando otras sin alterar o dándoles una versión siempre activa como controles. Cuando las células se estiraron mecánicamente, los fibroblastos normales respondieron como se esperaba: un aumento rápido de cofilina fosforilada y fibras de actina más fuertes, incremento de α-SMA, mayor producción de colágeno y niveles superiores de Bcl-2, una proteína que protege contra la muerte celular, junto con niveles reducidos de la proteína pro-muerte BAX. En contraste llamativo, los fibroblastos con LIMK2 inactivo apenas cambiaron bajo estiramiento. No aumentaron α-SMA, no elevaron Bcl-2 ni redujeron BAX, y mostraron menos colágeno. Estas células también contraían geles de colágeno con menos fuerza y se desplazaban más lentamente en un ensayo similar a una herida, lo que sugiere menor fuerza de tracción y menor capacidad para invadir el tejido circundante.
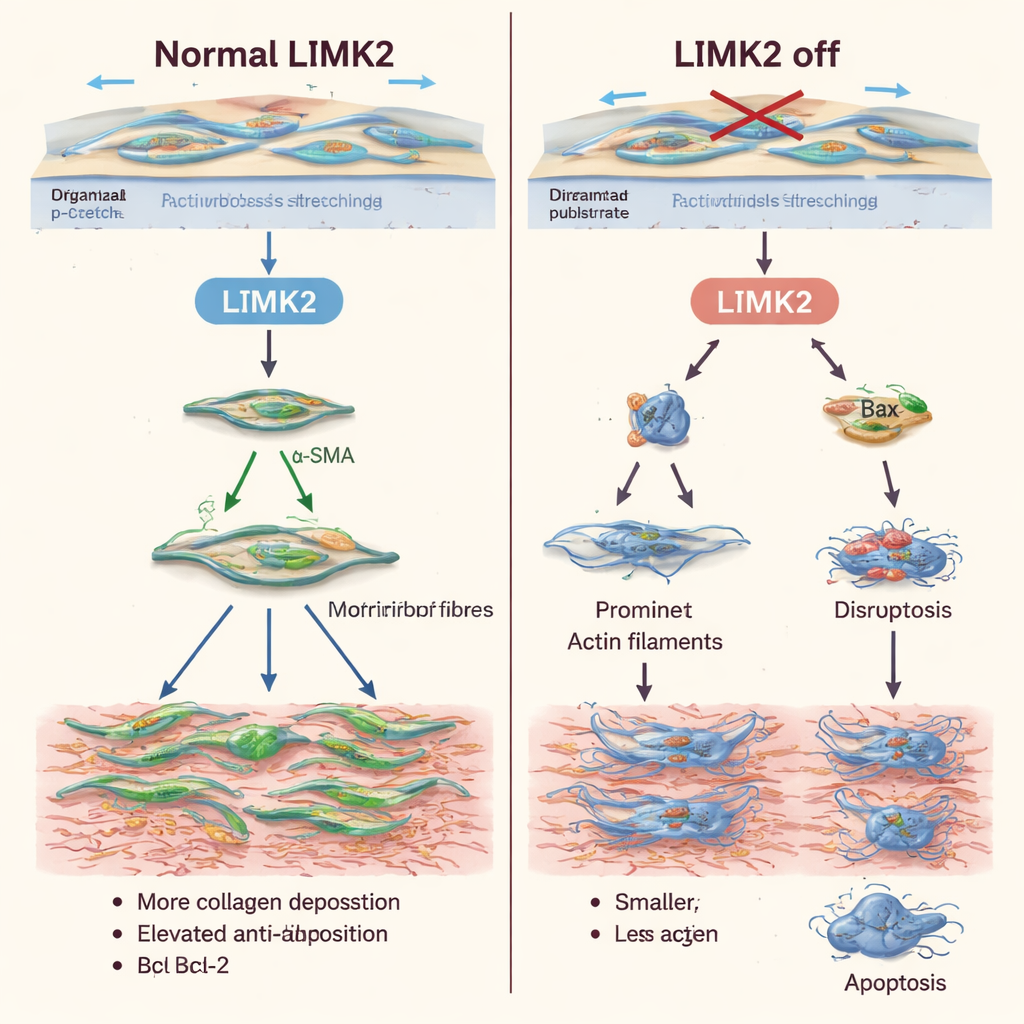
Hacer que las células cicatriciales resistentes sean más fáciles de eliminar
Además de cambiar el comportamiento de los fibroblastos frente al estiramiento, apagar LIMK2 hizo que fueran más propensos a morir y menos propensos a multiplicarse. Las células con LIMK2 inactivo mostraron niveles basales más altos de apoptosis, y el estiramiento mecánico —normalmente una señal de supervivencia— dejó de protegerlas. La citometría de flujo y las tinciones fluorescentes confirmaron que más células estaban en etapas tempranas o tardías de muerte programada. Al mismo tiempo, los recuentos celulares y las pruebas de marcado del ADN revelaron que estas células se dividían mucho menos que las normales. Patrones similares aparecieron cuando el equipo usó latrunculina A, un fármaco que altera los filamentos de actina, lo que respalda la idea de que LIMK2 actúa principalmente controlando el andamiaje interno de la célula.
Qué podría significar esto para futuros tratamientos de cicatrices
Los hallazgos sugieren que LIMK2 se sitúa en una encrucijada donde confluyen fuerzas mecánicas, supervivencia celular y actividad formadora de cicatrices. Cuando LIMK2 está activa, el estiramiento empuja a los fibroblastos hacia un estado de miofibroblasto resistente y persistente: contraen con fuerza, resisten la muerte y producen colágeno adicional, todo lo cual favorece cicatrices gruesas y elevadas. Apagar LIMK2 revierte gran parte de esto: los fibroblastos se vuelven menos contráctiles, menos móviles, menos prolíficos y más proclives a la apoptosis. Para los pacientes, esto apunta a un futuro en el que cremas, inyecciones o apósitos que bloqueen de forma suave LIMK2 o sus cambios en la actina aguas abajo podrían ayudar a que las heridas de alto riesgo sanen con cicatrices más planas y cómodas.
Cita: Ishii, M., Kuroda, K., Otani, N. et al. LIMK2 inactivation suppresses mechanical stimulation-induced dermal fibroblast differentiation and resistance to apoptosis. Sci Rep 16, 7453 (2026). https://doi.org/10.1038/s41598-026-37610-y
Palabras clave: cicatrices queloides, cicatrización de heridas, fibroblastos, tensión mecánica, apoptosis