Clear Sky Science · es
Ubiquitinación de SMAD2 a través del motivo PY regula la masa muscular esquelética y la degeneración fibrótica
Por qué importa este estudio sobre el músculo
A medida que envejecemos, muchos notamos que nuestros músculos se debilitan y disminuyen de tamaño, y en enfermedades crónicas o tras lesiones el músculo puede ser gradualmente reemplazado por tejido cicatricial rígido. Este estudio aborda una cuestión básica detrás de esos cambios: ¿cómo evitan las células musculares que una potente señal reguladora del crecimiento, llamada TGF‑beta, se descontrole y provoque pérdida muscular y fibrosis (formación de cicatrices)? Al descubrir un diminuto "interruptor de apagado" incorporado en una proteína clave de la vía TGF‑beta, los autores revelan un mecanismo nuevo que ayuda a preservar la masa muscular y la estructura sana del tejido.
Un freno incorporado en una señal potente
TGF‑beta es una molécula señalizadora que indica a las células cuándo frenar el crecimiento, cambiar de identidad o producir tejido conectivo. En el músculo esquelético, un exceso de TGF‑beta reduce el diámetro de las fibras y favorece la fibrosis; niveles muy bajos pueden alterar el control normal del crecimiento. Dentro de las células, TGF‑beta actúa principalmente a través de una proteína transmisora llamada SMAD2. Tras la unión de TGF‑beta a sus receptores en la superficie celular, SMAD2 se activa y se desplaza al núcleo para modificar la actividad génica. Para evitar que esto se vuelva permanente, las células marcan químicamente a SMAD2 con pequeñas moléculas de ubiquitina, señalando su eliminación. Una secuencia corta en SMAD2, conocida como motivo PY, es el sitio de anclaje para las enzimas que añaden estas etiquetas de ubiquitina. Los investigadores se preguntaron: si se elimina este sitio de anclaje en un animal vivo, ¿falla el freno sobre SMAD2 y qué le ocurre a los músculos con el tiempo?
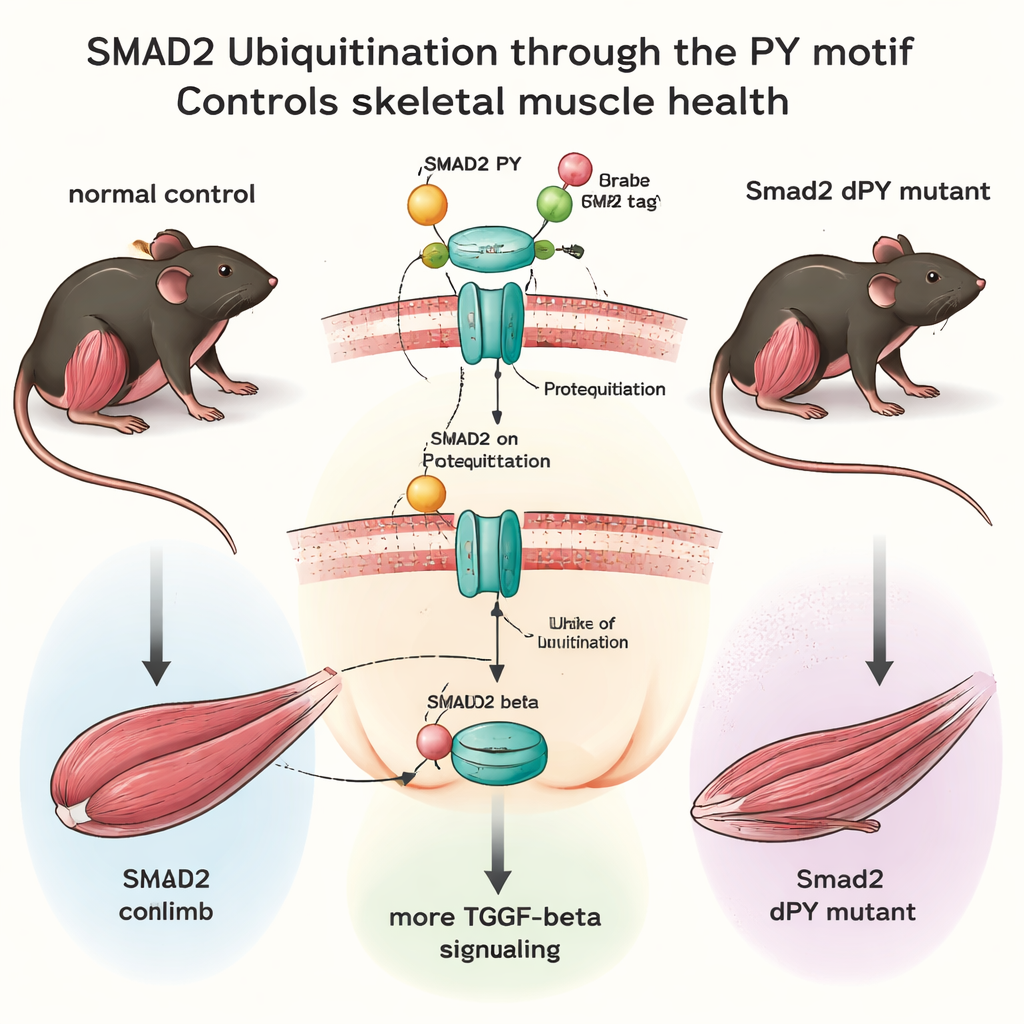
Ratones diseñados sin una etiqueta de seguridad
Usando herramientas modernas de edición génica, el equipo creó ratones en los que se eliminaron solo 15 "letras" de ADN del gen Smad2, suprimiendo con precisión el motivo PY sin alterar el resto de la proteína. Estos ratones Smad2dPY nacieron normalmente, crecieron hasta la edad adulta y eran fértiles, lo que indica que este ajuste fino no es esencial para el desarrollo básico en condiciones de laboratorio estándar. Sin embargo, al examinar sus músculos con más detalle surgió otra imagen. Los ratones adultos jóvenes mostraron solo cambios sutiles, pero a los 12 meses—aproximadamente la mediana de la vida útil de un ratón—los músculos principales de las patas traseras pesaban menos y las fibras individuales eran más pequeñas en comparación con sus compañeros normales. En el interior de estos músculos, los niveles de la proteína SMAD2 eran mayores, mientras que su ubiquitinación estaba reducida, confirmando que la ausencia del motivo PY hacía a SMAD2 más estable y menos degradable.
Células musculares hipersensibles y reparación estancada
Para entender qué significaba esto a nivel celular, los investigadores aislaron células precursoras musculares (mioblastos) de los ratones mutantes. Cuando se expusieron a TGF‑beta en cultivo, estos mioblastos mostraron una activación más intensa de SMAD2 y una mayor inducción de genes sensibles a TGF‑beta que las células de ratones normales. Al mismo tiempo, su capacidad para fusionarse en largas fibras musculares multinucleadas—un paso clave en el crecimiento y la regeneración muscular—estaba impedida. Cambios similares se observaron en fibroblastos, las células del tejido conectivo que se sitúan entre las fibras musculares: los fibroblastos mutantes respondían con mayor intensidad a TGF‑beta y expresaban con mayor facilidad genes asociados a miofibroblastos formadores de cicatriz. En conjunto, estos hallazgos sugieren que sin el motivo PY, tanto las células formadoras de músculo como las células de soporte se vuelven hipersensibles a TGF‑beta, desequilibrando la balanza hacia fibras más pequeñas y más tejido fibrótico.
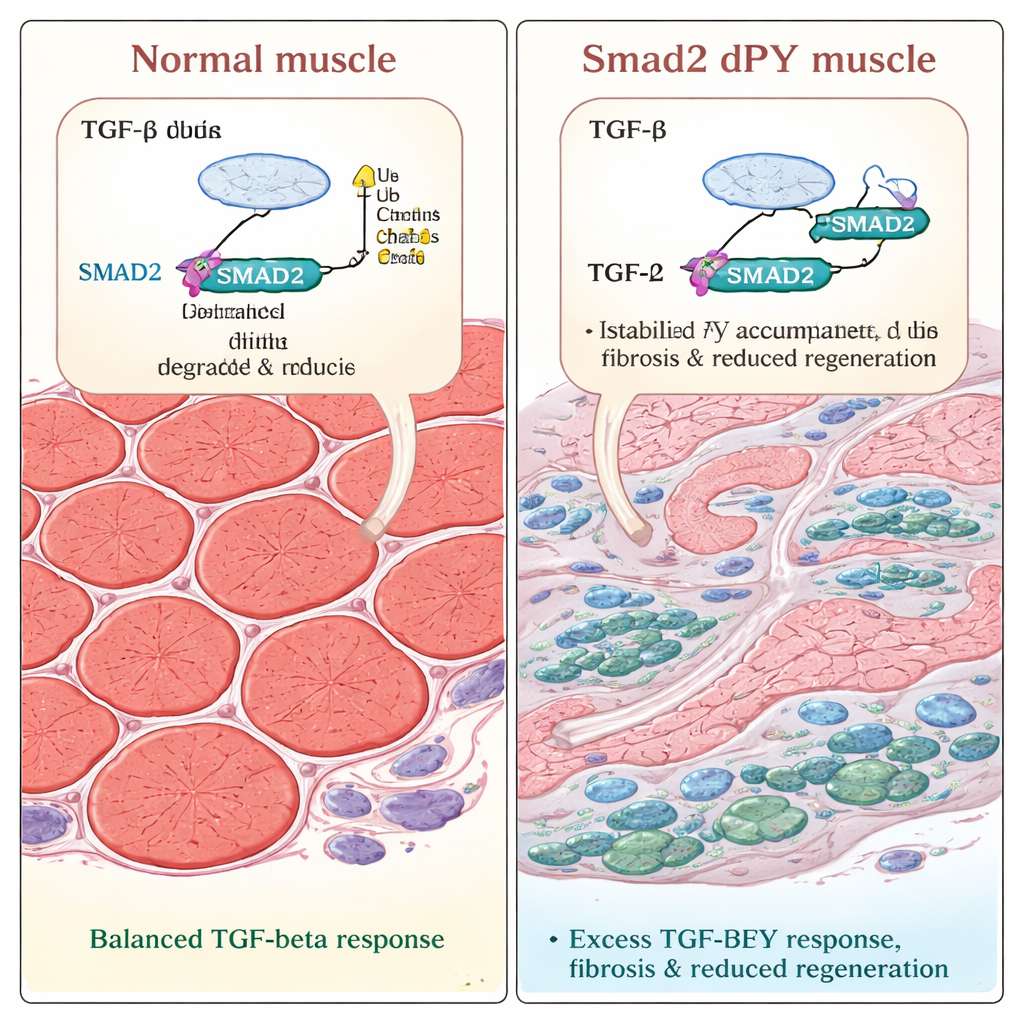
Cuando ocurre una lesión, la cicatrización gana
El equipo probó entonces cómo afrontaban estas alteraciones los músculos dañados. Inyectaron una toxina en los músculos de la pierna para provocar lesión y reparación, un modelo bien establecido de regeneración. En ratones normales y mutantes, las fibras dañadas inicialmente se descomponían y luego empezaban a regenerarse. Pero tres semanas después de la lesión, las fibras regeneradas en los ratones Smad2dPY eran notablemente más delgadas. La microscopía reveló áreas mayores llenas de colágeno, el componente principal del tejido cicatricial, y un aumento en el número de miofibroblastos positivos para actina alfa de músculo liso, células conocidas por impulsar la fibrosis. Estos resultados muestran que cuando SMAD2 no puede ser adecuadamente etiquetado y eliminado, el proceso de reparación se inclina: en lugar de reconstruir músculo fuerte por completo, el tejido sana con exceso de cicatrización y menor masa contráctil.
Qué significa esto para la salud muscular
Para quienes no son especialistas, el mensaje principal es que una característica molecular muy pequeña—el motivo PY en SMAD2—actúa como una salvaguarda discreta pero importante en el músculo esquelético. Permite que las células atenúen la señalización de TGF‑beta promoviendo la eliminación de SMAD2, ayudando a mantener el tamaño muscular normal y a limitar la fibrosis, sobre todo cuando los niveles de TGF‑beta aumentan con la edad o tras lesiones crónicas. Cuando esta salvaguarda se desactiva en ratones, los músculos se vuelven gradualmente más pequeños y propensos a la cicatrización, y no logran recuperarse completamente después del daño. Aunque este trabajo aún se ha realizado en animales, subraya la ubiquitinación de SMAD2 como una vía diana potencial para estrategias futuras destinadas a preservar la masa muscular y prevenir la degeneración fibrótica en el envejecimiento o la enfermedad.
Cita: Yamasaki, Y., Sakamoto, K., Yashiro, S. et al. SMAD2 ubiquitination through PY motif regulates skeletal muscle mass and fibrotic degeneration. Sci Rep 16, 6666 (2026). https://doi.org/10.1038/s41598-026-37582-z
Palabras clave: músculo esquelético, señalización TGF-beta, SMAD2, ubiquitinación, fibrosis