Clear Sky Science · es
Cambios en la actividad de EGFR tras la edición CRISPR/Cas9 del dominio de unión a EGF
Por qué importa reconectar una señal del cáncer
El cáncer de cérvix a menudo depende de un potente interruptor de crecimiento llamado receptor del factor de crecimiento epidérmico (EGFR). Muchos tumores presentan cantidades enormes de estos receptores, pero los fármacos destinados a apagarlos solo han beneficiado a una fracción de los pacientes. Este estudio planteó una cuestión fundamental con importantes implicaciones terapéuticas: ¿qué ocurre si se elimina la capacidad de EGFR para captar su señal de crecimiento favorita, el factor de crecimiento epidérmico (EGF), sin eliminar el propio receptor?
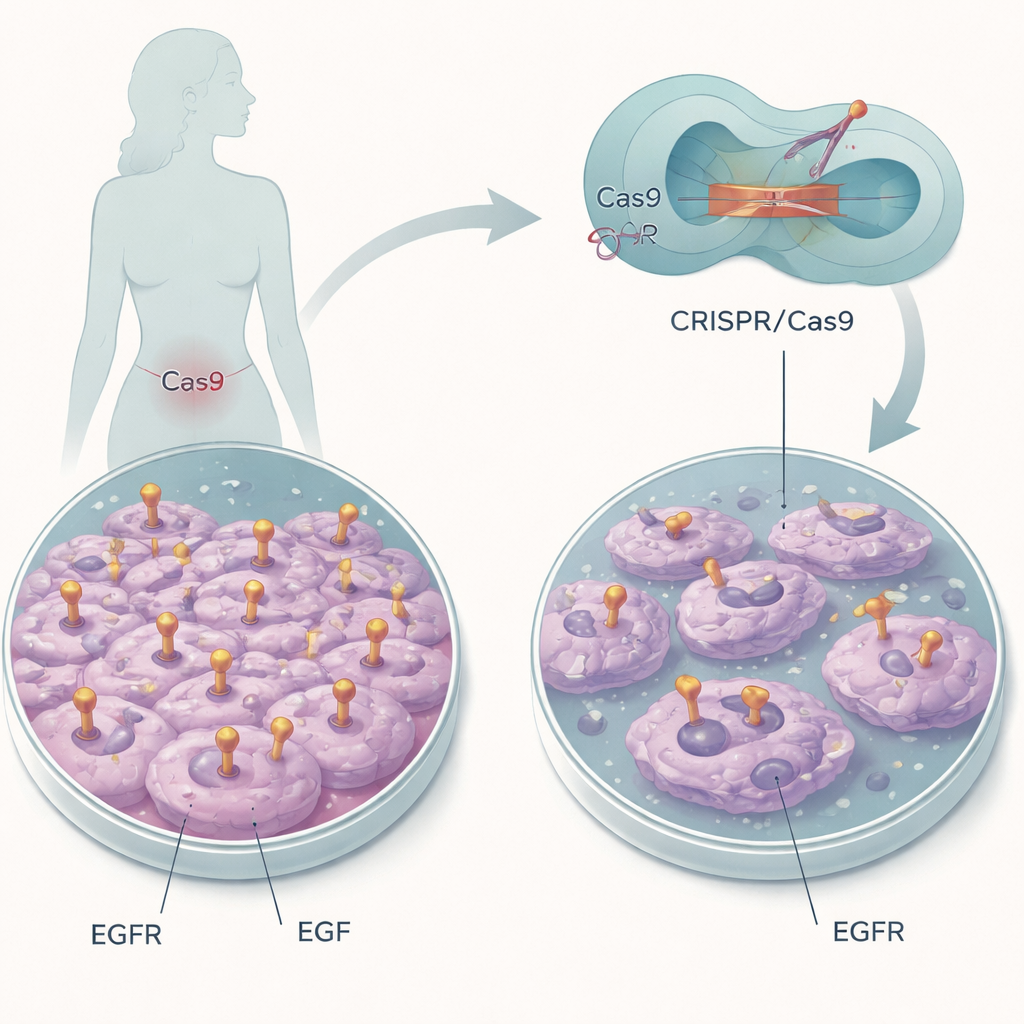
Apagar un “interruptor” molecular
Los investigadores se centraron en una línea celular de cáncer de cérvix que porta grandes cantidades de EGFR pariente normal. En lugar de destruir el gen, utilizaron la edición del genoma CRISPR/Cas9 como un bisturí molecular para cambiar solo unos pocos aminoácidos en el bolsillo de unión a EGF de EGFR. Dos posiciones concretas, denominadas L14 e Y45, ayudan a que EGF se ancle al receptor. Sustituyendo estos bloques constructores por otros distintos, el equipo pretendía mantener EGFR presente pero ciego al EGF, lo que les permitía aislar el papel de esta única interacción en el comportamiento de las células cancerosas.
Construir líneas celulares cancerosas a medida
En un primer paso, el equipo probó estas mutaciones en células usando plásmidos que producían de forma transitoria EGFR normal o alterado. Un EGF marcado con fluorescencia reveló que todas las formas mutantes unían mucho menos ligando que el receptor normal, sobre todo cuando L14 e Y45 se cambiaban juntos. A continuación, los investigadores introdujeron directamente estos cambios en el genoma de las células cancerosas con CRISPR/Cas9, generando varios nuevos clones celulares. Algunos portaban una sola mutación, otros la doble mutación en una copia de EGFR y cambios inactivadores en la otra. Los modelos computacionales de las formas proteicas resultantes mostraron que estas alteraciones deformaban el sitio de unión lo suficiente como para debilitar o abolir el anclaje de EGF, coherente con las pruebas de unión.
Cuando el receptor se desplaza pero las células sobreviven
Imágenes detalladas revelaron que los receptores editados se comportaban de forma muy distinta dentro de la célula. En las células cancerosas no editadas, EGFR se sitúa en la superficie celular, captura EGF y luego se internaliza mientras se activa químicamente mediante fosforilación. En los clones con la doble mutación, la unión de EGF desapareció prácticamente y EGFR dejó de verse en la membrana; en cambio, la pequeña cantidad de receptor restante se acumuló en el interior celular. Incluso un solo cambio en Y45 redujo sustancialmente la unión y disminuyó los niveles totales de EGFR. Sin embargo, a pesar de esta alteración de la vía clásica EGF–EGFR, las células cancerosas siguieron viables y continuaron proliferando en cultivo con solo cambios modestos en sus patrones del ciclo celular.
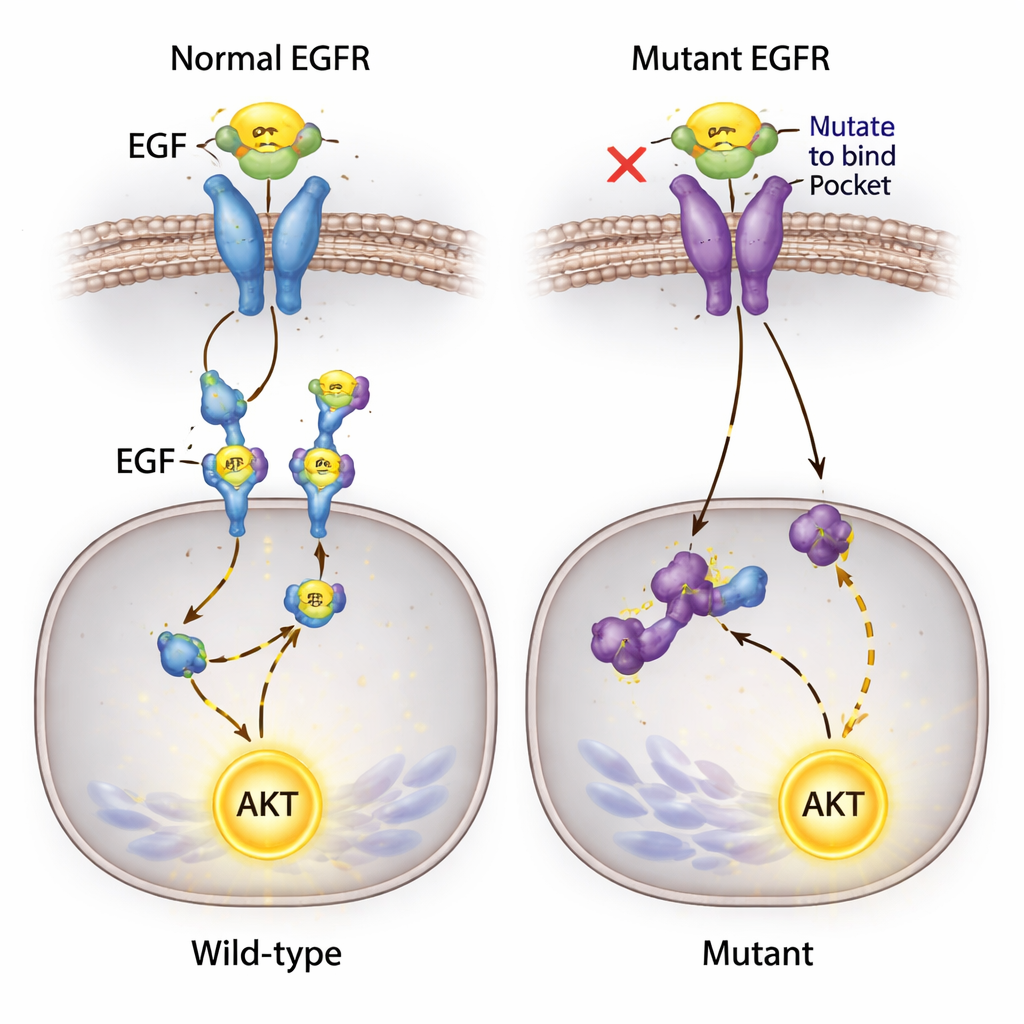
Una señal inesperada que no se rinde
Uno de los hallazgos más sorprendentes implicó a AKT, una proteína clave que promueve la supervivencia celular y que suele activarse aguas abajo de EGFR. Los investigadores esperaban que bloquear la unión EGF–EGFR silenciara esta vía. En cambio, al añadir EGF al medio, AKT se activó con fuerza en todas las líneas celulares, incluidas aquellas en las que EGF ya no podía unirse a EGFR y donde la fosforilación del receptor era indetectable. Dado que estas células portan una mutación conocida en otro gen de señalización, PIK3CA, el equipo sospecha que rutas alternativas pueden permitir que EGF alimente la activación de AKT, posiblemente a través de otras proteínas de superficie o mutaciones de fondo, eludiendo el EGFR editado.
Cambios genéticos ocultos y terapias futuras
Para asegurarse de que CRISPR no causaba ediciones involuntarias generalizadas, los científicos secuenciaron los genomas completos de las nuevas líneas celulares. Confirmaron que estaban presentes las mutaciones deseadas en EGFR y no encontraron evidencia de cortes en los sitios fuera de objetivo predichos para las guías CRISPR. Sin embargo, detectaron muchas mutaciones espontáneas dispersas por el genoma, algunas de las cuales podrían influir en el comportamiento celular. Esto subraya que, incluso cuando CRISPR acierta su dirección prevista, el ADN naturalmente inestable de las células cancerosas puede complicar la interpretación de los resultados experimentales y el diseño de terapias génicas precisas.
Qué significa esto para los pacientes
Para un público general, la conclusión es que bloquear simplemente el apretón de manos entre EGF y EGFR —incluso con precisión atómica— no detiene automáticamente que las células cancerosas reciban órdenes de “crecer y sobrevivir”. El estudio muestra que las células cancerosas pueden redirigir señales clave como la activación de AKT alrededor de un receptor bloqueado, y que la propia edición con CRISPR debe evaluarse con cuidado en genomas tan inestables. Estas líneas celulares diseñadas proporcionan ahora un potente modelo de laboratorio para buscar vías de respaldo que sostienen tumores dependientes de EGFR, información que podría conducir finalmente a tratamientos combinados que apunten tanto a EGFR como a sus cómplices ocultos.
Cita: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Palabras clave: EGFR, cáncer de cérvix, CRISPR, señalización EGF, vía AKT