Clear Sky Science · es
La amplificación del número de copias impulsa la sobreexpresión de IFI30 y la activación inmune coordinada, identificando un nuevo objetivo diagnóstico y terapéutico en el adenocarcinoma gástrico
Por qué importa una proteína del estómago
El cáncer gástrico es uno de los más mortales del mundo, en gran parte porque con frecuencia se detecta tarde y puede ser difícil de tratar. Este estudio se centra en una proteína poco conocida llamada IFI30, presente en células que ayudan al sistema inmune a reconocer amenazas. Al rastrear cómo se altera IFI30 en los tumores de estómago y cómo moldea las defensas del organismo, los investigadores sugieren que podría convertirse en una herramienta potente para un diagnóstico más temprano y para elegir tratamientos más efectivos y personalizados.
Una señal oculta en los tumores gástricos
El equipo comenzó planteando una pregunta básica: ¿está IFI30 presente en niveles distintos en el tejido gástrico sano frente al canceroso? Utilizando grandes conjuntos de datos públicos que combinan la actividad génica de miles de muestras, encontraron que IFI30 es sistemáticamente mucho más alto en el adenocarcinoma gástrico—el tipo más común de cáncer de estómago—que en la mucosa gástrica normal. Esto se mantuvo cierto en múltiples cohortes independientes de pacientes y tanto a nivel de ARN como de proteína. Cuando los autores evaluaron qué tan bien IFI30 por sí solo podía distinguir tejido tumoral de tejido sano, su rendimiento fue notable: una precisión diagnóstica (AUC) de 0,92, considerada excelente para un marcador único. Las imágenes microscópicas también ubicaron a IFI30 dentro del sistema interno de reciclaje celular, donde se procesan los antígenos para el reconocimiento inmune.
Cambios en el ADN que elevan IFI30
A continuación, los investigadores investigaron por qué IFI30 está tan elevado en estos tumores. Al examinar genomas tumorales del Cancer Genome Atlas, encontraron que copias extra del gen IFI30—conocidas como amplificaciones del número de copias—eran el principal impulsor de su sobreexpresión. Los tumores con amplificación de IFI30 tendían a mostrar mayor inestabilidad genómica general y con frecuencia portaban mutaciones tumorales conocidas como TP53 y PIK3CA. A medida que aumentaba el número de copias de IFI30, también se elevaban sus niveles de ARN, lo que sugiere un vínculo directo entre los cambios estructurales del ADN y la mayor producción de esta proteína. Esto presenta a IFI30 no como un espectador pasivo, sino como parte de un patrón más amplio de biología tumoral agresiva.
Interacción inmune alrededor del tumor
Dado que IFI30 participa en el procesamiento del material que las células inmunes presentan como “carteles de búsqueda” a los linfocitos T, el equipo exploró dónde, exactamente, se sitúa dentro del microambiente tumoral. La secuenciación unicelular, que lee la expresión génica en células individuales, mostró que IFI30 está especialmente enriquecido en células dendríticas, macrófagos y linfocitos T CD8—actores clave en el inicio y mantenimiento de la inmunidad antitumoral. Los análisis de redes revelaron una comunicación densa entre las células inmunes ricas en IFI30 y las células tumorales y de soporte circundantes. Los tumores con alto IFI30 mostraron una fuerte activación de vías relacionadas con la presentación de antígenos, señales inflamatorias y moléculas de comunicación que atraen y organizan células inmunes. Al mismo tiempo, estos tumores exhibieron rasgos de invasión y estrés, como aceleración del ciclo celular, remodelado tisular y adaptación a baja oxigenación, lo que subraya el papel de IFI30 en la intersección entre ataque y defensa dentro del cáncer.
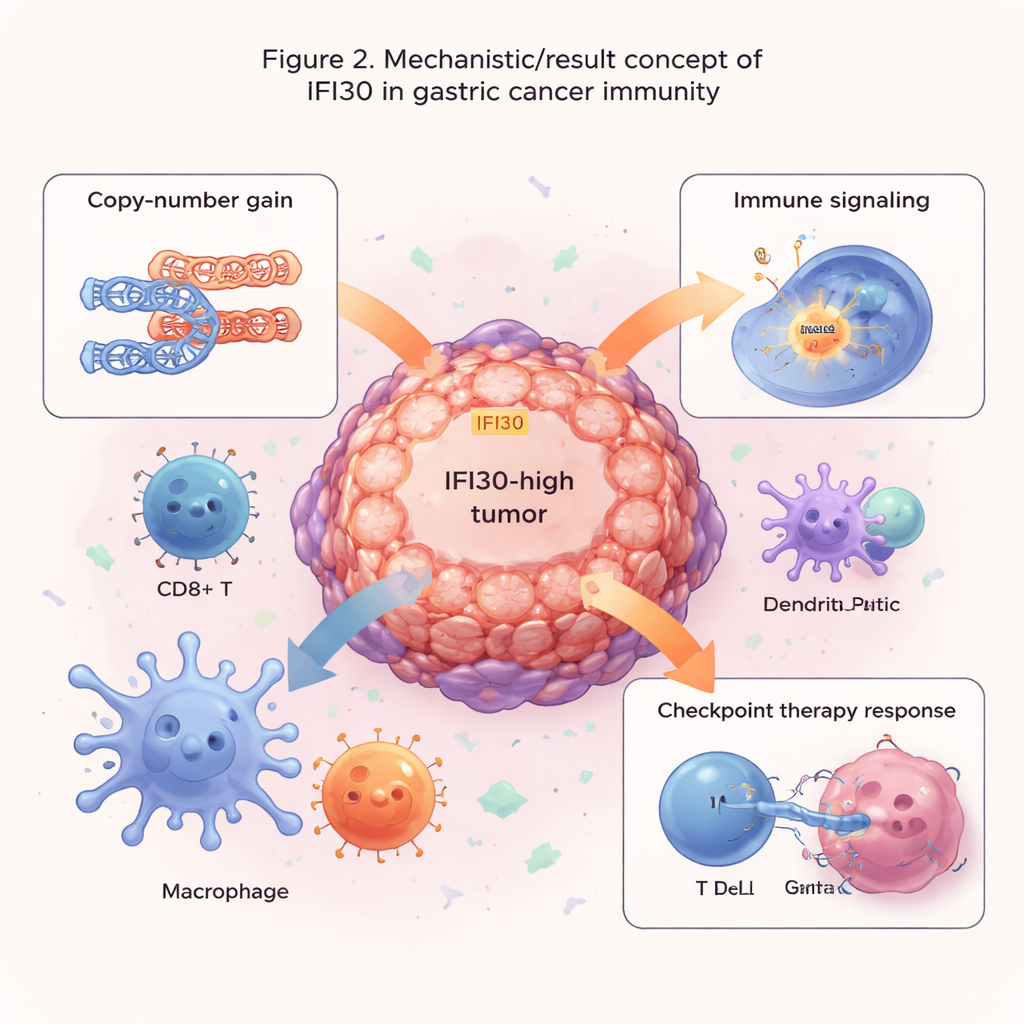
Pistas para la elección de fármacos y la inmunoterapia
Los autores preguntaron luego si IFI30 podría ayudar a predecir cómo responden los tumores al tratamiento. Al combinar los niveles de IFI30 con grandes conjuntos de datos de respuesta a fármacos, encontraron que los tumores con alta expresión de IFI30 tienden a resistir algunos medicamentos que apuntan a la división celular o a una vía de crecimiento común (MAPK), pero parecen más sensibles a fármacos que bloquean la señalización EGFR y PI3K/AKT. Es notable que los niveles de IFI30 se correlacionaron estrechamente con PD-L1, un freno principal sobre los linfocitos T que es diana de los inhibidores de puntos de control actuales. En varios estudios de inmunoterapia, los pacientes cuyos tumores presentaban mayor expresión de IFI30 tenían más probabilidades de responder al bloqueo de puntos de control que aquellos con niveles bajos. Una puntuación basada en IFI30 superó a medidas establecidas como la carga mutacional tumoral y PD-L1 por sí sola, y se enriqueció especialmente en tumores con alta inestabilidad de microsatélites, un subgrupo ya conocido por responder mejor a la inmunoterapia.
Del banco de laboratorio a un posible nuevo objetivo
Para comprobar si IFI30 es solo un marcador o también contribuye al crecimiento tumoral, el equipo redujo sus niveles en líneas celulares de cáncer gástrico mediante herramientas genéticas. Cuando se silenció IFI30, las células cancerosas crecieron más despacio, lo que apunta a un papel directo en el mantenimiento de la proliferación tumoral. En conjunto, los datos sugieren que IFI30 es tanto un reflejo de la actividad inmune como un contribuyente al comportamiento maligno. Para los pacientes, esto significa que una medida sencilla de IFI30 podría algún día ayudar a los médicos a detectar el cáncer gástrico con mayor fiabilidad, predecir quién podría beneficiarse de ciertos fármacos dirigidos o inmunoterapias, y quizá guiar nuevos tratamientos que bloqueen directa o indirectamente las acciones promotoras del tumor de IFI30.
Cita: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Palabras clave: cáncer gástrico, IFI30, biomarcador, inmunidad tumoral, inmunoterapia