Clear Sky Science · es
Análisis computacional de los hidruros X2CaZnH6 (X = K, Rb y Cs) para el almacenamiento de hidrógeno
Hidrógeno en una caja
El hidrógeno suele presentarse como un combustible limpio del futuro, pero almacenarlo de forma segura y compacta sigue siendo un gran desafío. Este estudio explora una nueva familia de materiales cristalinos que pueden retener hidrógeno dentro de su armazón atómico, de manera similar al agua en una esponja. Al diseñar estos compuestos por ordenador antes de que se fabriquen en el laboratorio, los autores muestran cómo podrían funcionar como combustibles sólidos para tecnologías futuras alimentadas por hidrógeno.
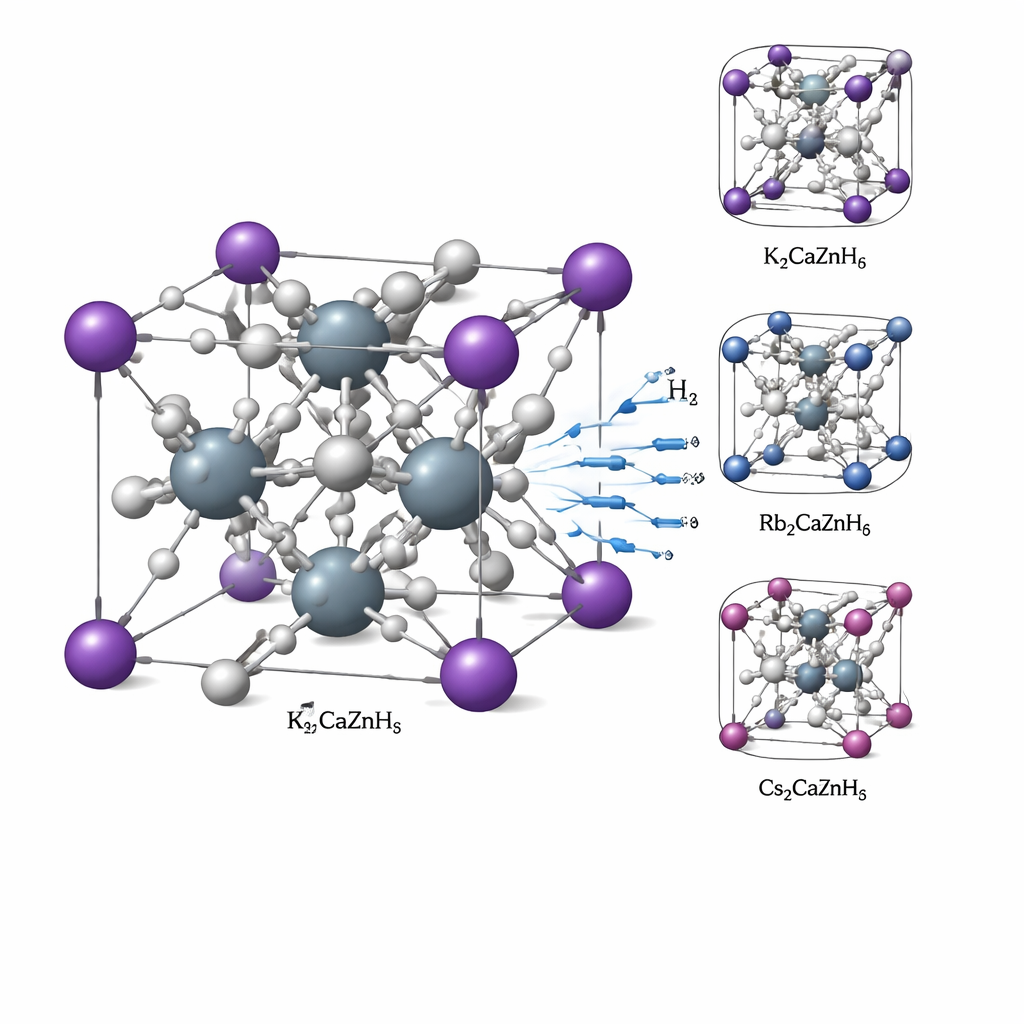
Un cristal construido como una red 3D
Los materiales estudiados se denominan hidruros de perovskita doble, con la fórmula X2CaZnH6, donde X puede ser potasio (K), rubidio (Rb) o cesio (Cs). Los tres forman una estructura sencilla tipo cubo en la que los átomos pesados ocupan posiciones bien definidas y los átomos de hidrógeno se sitúan alrededor de ellos. Mediante cálculos cuántico-mecánicos, los autores confirman que estos cristales son estructuralmente estables: los átomos encajan con el tamaño adecuado, la energía global del material es lo bastante baja como para formarse de manera natural, y las vibraciones atómicas no indican inestabilidades ocultas. Pruebas mecánicas realizadas in silico muestran que los cristales son rígidos pero no excesivamente frágiles, un equilibrio que les permite mantener su forma a la vez que admite pequeños reajustes cuando se absorbe o libera hidrógeno.
¿Cuánto hidrógeno pueden contener?
Para cualquier material de almacenamiento, dos cifras clave son la cantidad de hidrógeno que puede contener por peso (capacidad gravimétrica) y por volumen (capacidad volumétrica), así como la temperatura a la que se puede liberar el hidrógeno. Los tres compuestos estudiados almacenan entre aproximadamente 1,6 y 3,2 % de su masa en forma de hidrógeno, y alrededor de 15 a 18 kilogramos de hidrógeno por metro cúbico de material. La versión a base de potasio, K2CaZnH6, contiene la mayor cantidad de hidrógeno pero requiere temperaturas más altas (alrededor de 658 K, o 385 °C) para liberarlo. La versión con cesio almacena algo menos de hidrógeno y también necesita temperaturas bastante elevadas. El compuesto de rubidio, Rb2CaZnH6, destaca: libera hidrógeno a unos 385 K (aprox. 110 °C), un rango mucho más próximo a lo que se considera práctico para dispositivos reales, manteniendo además una densidad de almacenamiento respetable.
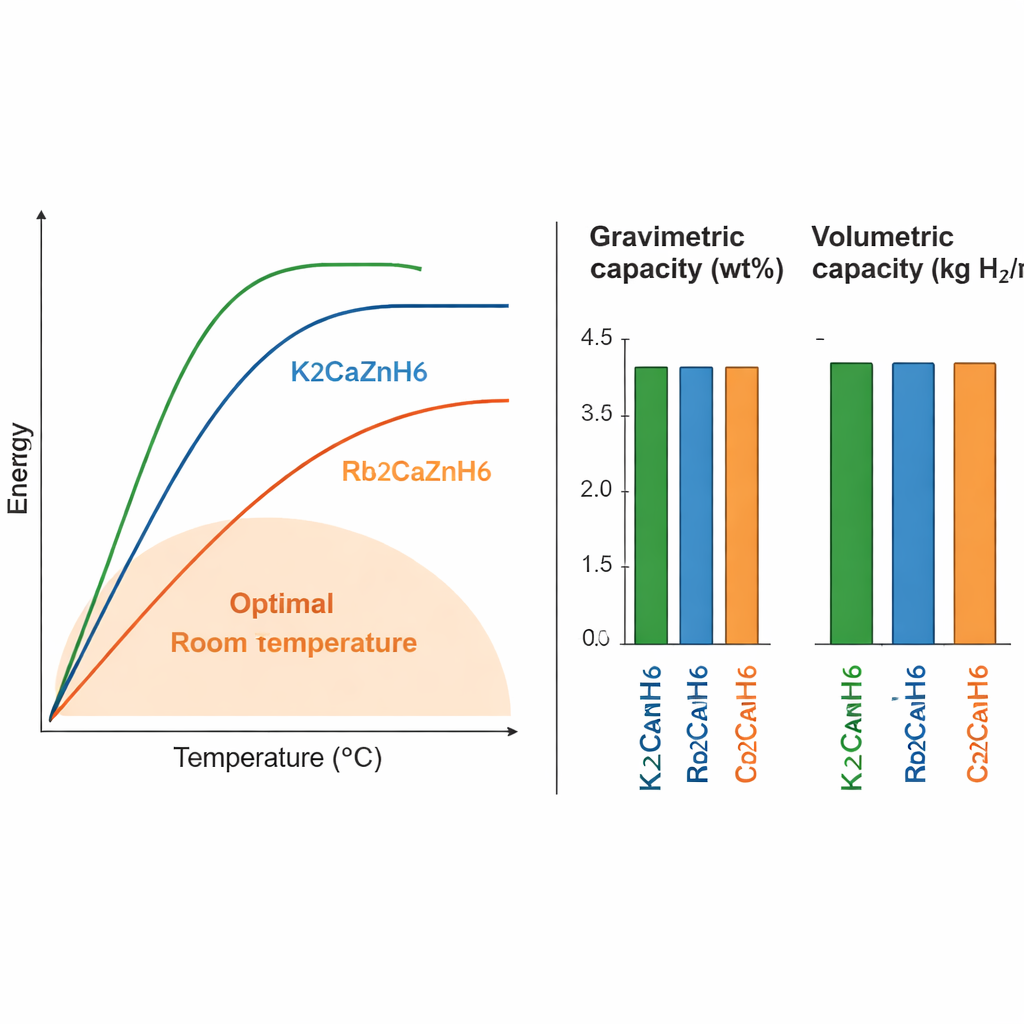
Por qué importan los átomos y los electrones
Para entender por qué estos materiales se comportan así, los autores examinan cómo se comparten los electrones entre los átomos y cómo esto afecta al enlace químico. En los tres compuestos, el potasio, el rubidio o el cesio actúan como donantes de electrones, mientras que el zinc, el calcio y el hidrógeno atraen electrones. Los átomos de hidrógeno adquieren una carga parcial negativa, y sus enlaces con calcio y zinc son en gran medida iónicos con un matiz de carácter covalente. Este tipo de enlaces tiende a retener el hidrógeno con suficiente fuerza como para que no se escape fácilmente, pero lo bastante débil como para que el calentamiento lo libere cuando se necesita. Es importante que los átomos de hidrógeno no formen enlaces H–H fuertes dentro del cristal, lo que significa que el hidrógeno se almacena como átomos separados en lugar de como moléculas preformadas, lo cual es favorable para una liberación controlada.
Luz, electricidad y resistencia
Estos cristales también son semiconductores, con una brecha de energía moderada entre estados electrónicos ocupados y vacantes. Eso significa que pueden interactuar con la luz en un amplio rango de colores, especialmente en las regiones visible y ultravioleta del espectro. Los cálculos muestran fuerte absorción de luz y una conductividad óptica significativa, lo que abre la posibilidad de que la luz pueda ayudar a desencadenar la liberación de hidrógeno, una especie de almacenamiento asistido por energía solar. Al mismo tiempo, los materiales cumplen criterios estándar de estabilidad mecánica: resisten compresión, corte y fractura dentro de límites razonables, y sus vibraciones atómicas a temperatura ambiente se mantienen bien comportadas en pruebas de calentamiento simuladas por ordenador. En conjunto, estas características apuntan a una estructura robusta capaz de soportar ciclos repetidos de carga y descarga de hidrógeno.
Qué significa esto para los sistemas energéticos del futuro
En términos cotidianos, el estudio identifica tres nuevos materiales tipo “esponja de hidrógeno” que son estables, razonablemente resistentes y capaces de empaquetar hidrógeno en un sólido compacto. Aunque su contenido de hidrógeno por peso todavía no alcanza los objetivos más ambiciosos, su almacenamiento volumétrico es prometedor, y el compuesto a base de rubidio en particular opera a temperaturas compatibles con muchos sistemas prácticos. Debido a que su comportamiento puede afinarse simplemente sustituyendo un elemento alcalino por otro, estos hidruros de perovskita doble ofrecen una plataforma flexible para diseñar combustibles sólidos de hidrógeno mejores y, potencialmente, para combinar el almacenamiento con un control impulsado por la luz en futuras tecnologías de energía limpia.
Cita: Al-Zoubi, N., Almahmoud, A., Almahmoud, A. et al. Computational analysis of X2CaZnH6 (X = K, Rb and Cs) hydrides for hydrogen storage. Sci Rep 16, 6889 (2026). https://doi.org/10.1038/s41598-026-37564-1
Palabras clave: almacenamiento de hidrógeno, hidruros metálicos, perovskita doble, energía en estado sólido, combustibles limpios