Clear Sky Science · es
Identificación computacional de fitoquímicos de Terminalia arjuna como posibles inhibidores de 3α-HSD3
Por qué importa esta investigación
El cáncer de mama es el tumor más frecuente en mujeres, y muchos tumores crecen en respuesta a hormonas. Este estudio plantea una pregunta oportuna: ¿pueden sustancias naturales procedentes de un árbol usado en la medicina tradicional, Terminalia arjuna, convertirse en candidatas farmacológicas modernas que «reduzcan» de forma sutil la actividad de una enzima clave en el procesamiento hormonal vinculada al crecimiento tumoral? Empleando simulaciones computacionales avanzadas en lugar de ensayo en animales, los investigadores buscan compuestos vegetales que algún día puedan complementar o mejorar las terapias hormonales actuales.
Hormonas, una sola enzima y el crecimiento tumoral
En ciertos cánceres de mama, especialmente en la línea muy estudiada MCF-7, el crecimiento está fuertemente impulsado por la hormona femenina estrógeno. Normalmente, los andrógenos (frecuentemente asociados con hormonas masculinas) pueden contrarrestar los efectos del estrógeno. La enzima que centra este trabajo, denominada 3α-HSD3, ayuda a convertir un andrógeno potente en formas más débiles. Cuando 3α-HSD3 está sobreactiva, elimina esa influencia androgénica protectora y deja un entorno dominado por estrógenos que favorece la multiplicación de células tumorales y la resistencia al tratamiento. Bloquear esta enzima podría, por tanto, desplazar el equilibrio hormonal de nuevo hacia la contención del crecimiento del cáncer.
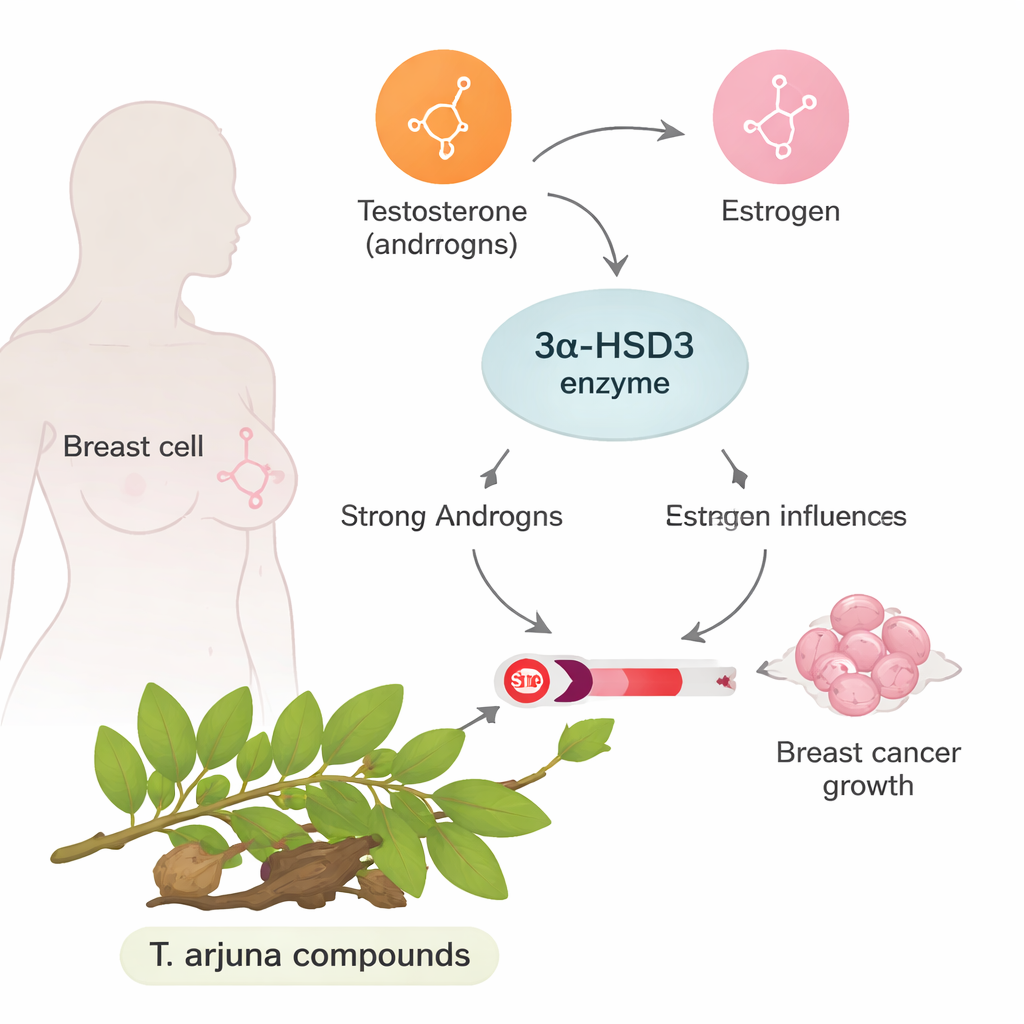
La promesa de un árbol de la medicina tradicional
Terminalia arjuna es un árbol empleado desde hace mucho en la medicina tradicional del sur de Asia, especialmente para la salud cardiaca. Su corteza y otras partes contienen numerosos compuestos vegetales con propiedades reportadas antioxidantes y anticancerígenas. Sin embargo, ninguno se había examinado detenidamente frente a 3α-HSD3. Los autores seleccionaron nueve moléculas bien conocidas de este árbol, incluidas flavonoides y taninos, basándose en informes previos sobre efectos anticancerígenos y protectores. En lugar de pasar de inmediato a animales de laboratorio o pacientes, primero utilizaron un conjunto de herramientas de diseño de fármacos asistido por ordenador para preguntar: ¿cuáles de estas moléculas naturales son más propensas a encajar y bloquear la enzima, comportarse como fármacos reales en el organismo y evitar toxicidades evidentes?
Simular cómo las moléculas vegetales encuentran su objetivo
El equipo partió de la estructura tridimensional humana de 3α-HSD3, resuelta previamente por cristalografía de rayos X, y verificó su calidad con pruebas estructurales estándar. A continuación construyeron y «relajaron» digitalmente las conformaciones de cada molécula vegetal para reflejar las formas realistas que adoptarían en el organismo. Siguió el acoplamiento virtual: el ordenador probó muchas posiciones de cada molécula en el bolsillo activo de la enzima y puntuó la afinidad y favorabilidad de la unión. Varios compuestos de Terminalia mostraron una unión predicha fuerte, a menudo mejor que un inhibidor sintético de referencia conocido. Cuatro destacaron en particular: luteolina, leucocianidina, ácido gálico y ácido elágico. Estos no sólo predijeron una unión estrecha, sino también la formación de múltiples enlaces de hidrógeno y otros contactos estabilizadores con aminoácidos clave que controlan la actividad enzimática.
Probar estabilidad, comportamiento y seguridad in silico
El acoplamiento ofrece una instantánea; los investigadores preguntaron entonces si esos complejos permanecerían estables a lo largo del tiempo en un entorno acuoso similar al corporal. Ejecutaron simulaciones de dinámica molecular de 100 nanosegundos—esencialmente, películas basadas en física de átomos que vibran a temperatura corporal. Medidas de cuánto se movieron la proteína y los ligandos mostraron que las cuatro moléculas vegetales permanecieron firmemente alojadas en el bolsillo de la enzima, estabilizándola a menudo más que el fármaco de control. Cálculos adicionales estimaron energías de unión y confirmaron que luteolina, leucocianidina y ácido gálico, en particular, establecían interacciones fuertes y favorables. Modelos computacionales paralelos predijeron que los cuatro candidatos deberían absorberse razonablemente bien por el intestino, distribuirse adecuadamente en tejidos, evitar problemas importantes con enzimas hepáticas y presentar baja probabilidad de toxicidad genética u orgánica en dosis terapéuticas.
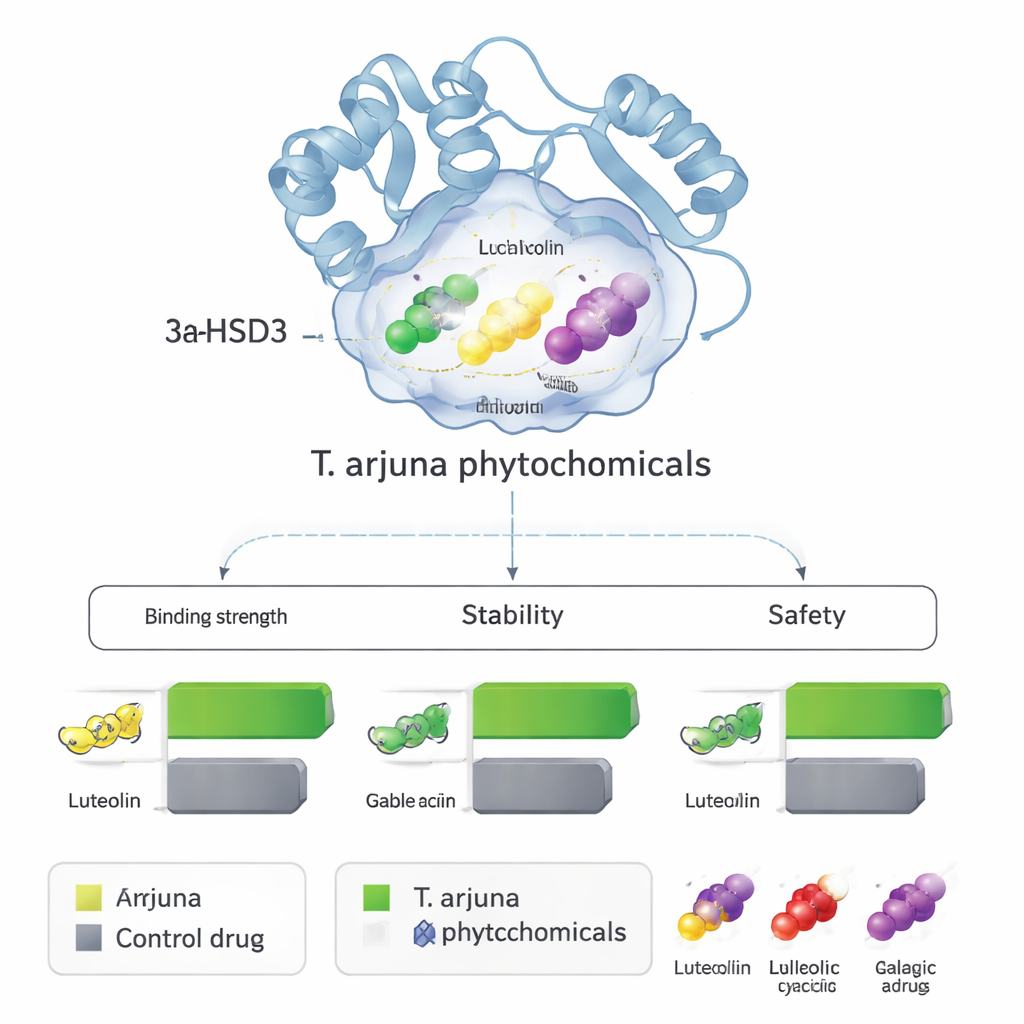
De las predicciones computacionales a futuras terapias
Para un público no especializado, el mensaje clave es que este trabajo no afirma haber descubierto una cura nueva, pero sí proporciona una lista concentrada de moléculas naturales prometedoras. La luteolina, la leucocianidina, el ácido gálico y el ácido elágico de Terminalia arjuna parecen, según múltiples pruebas computacionales independientes, unirse y potencialmente bloquear 3α-HSD3, una enzima que contribuye a crear un entorno rico en estrógenos en células de cáncer de mama sensibles a hormonas. También parecen tener propiedades parecidas a las de fármacos y ser relativamente seguras sobre el papel. Los siguientes pasos esenciales serán los experimentos de laboratorio para comprobar si estas predicciones se sostienen: ¿estos compuestos inhiben realmente la enzima en tubos de ensayo, y frenan el crecimiento de células de cáncer de mama sin dañar tejido sano? Si es así, podrían guiar el diseño de derivados mejorados o inspirar nuevas terapias combinadas que aprovechen tanto el saber tradicional vegetal como la ciencia molecular moderna.
Cita: Al Mashud, M.A., Rahman, M.A., Kumer, A. et al. Computational identification of Terminalia arjuna phytochemicals as potential 3α-HSD3 inhibitors. Sci Rep 16, 8045 (2026). https://doi.org/10.1038/s41598-026-37558-z
Palabras clave: hormonas y cáncer de mama, Terminalia arjuna, inhibidores naturales de enzimas, diseño de fármacos asistido por ordenador, luteolina ácido gálico