Clear Sky Science · es
Un enfoque con ligasa de biotina dividida revela proteínas asociadas con alfa-sinucleína oligomérica durante la agregación
Por qué importan las proteínas agrupadas en el cerebro
En la enfermedad de Parkinson y trastornos relacionados, una proteína cerebral que normalmente es útil, llamada alfa‑sinucleína, puede agruparse en depósitos adhesivos conocidos como cuerpos de Lewy. Estos depósitos aparecen décadas antes de los síntomas y son una característica definitoria observada en la autopsia, pero todavía no sabemos qué otras proteínas ayudan a impulsar a la alfa‑sinucleína desde un estado inofensivo hacia agregados dañinos. Este estudio utiliza una ingeniosa “etiqueta de proximidad” molecular para mapear qué proteínas se sitúan cerca de la alfa‑sinucleína cuando pasa de moléculas individuales a pequeños acúmulos, ofreciendo nuevas pistas sobre cómo comienza la enfermedad y qué vías podrían dirigirse para ralentizarla o prevenirla.
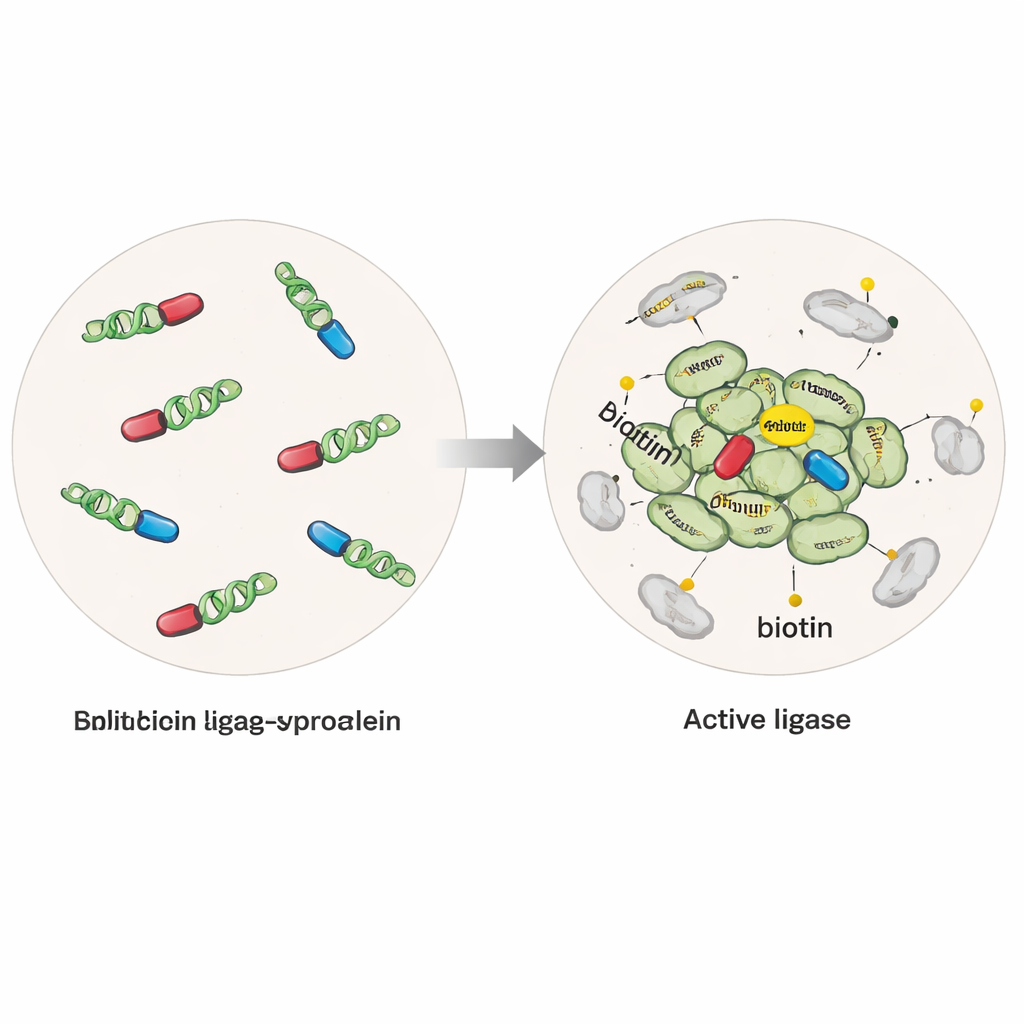
Una “etiqueta” molecular que ilumina a los vecinos
Los investigadores diseñaron células humanas para producir alfa‑sinucleína fusionada a una enzima modificada que puede unir una pequeña etiqueta de biotina a cualquier proteína situada a unos pocos nanómetros. En una versión, la enzima estaba intacta y activa siempre que la alfa‑sinucleína estuviera presente, capturando proteínas cercanas tanto a moléculas individuales como a acúmulos. En una segunda versión más selectiva, la “dividida”, la enzima se cortó en dos mitades inactivas, cada una unida a una molécula distinta de alfa‑sinucleína. Solo cuando las moléculas de alfa‑sinucleína se juntaban en multímeros u oligómeros las mitades se reunían para formar una enzima activa, activando el marcaje específicamente alrededor de estos agregados tempranos. Al añadir fibrillas purificadas de alfa‑sinucleína a las células, el equipo también pudo inducir agregación parecida a la patológica y comparar estados normales frente a patológicos.
Construyendo un mapa de proteínas cercanas
Tras permitir tiempo para el marcado, el equipo aisló todas las proteínas etiquetadas con biotina y las identificó mediante espectrometría de masas, una técnica que pesa y cuenta proteínas con alta precisión. En todas las condiciones hallaron 1.277 proteínas distintas y, tras un filtrado cuidadoso, las redujeron a 581 que probablemente estaban genuinamente cerca de la alfa‑sinucleína. Comparando los sistemas de enzima intacta y dividida, pudieron distinguir proteínas que se asocian principalmente con moléculas individuales de aquellas que prefieren multímeros. También compararon células con y sin fibrillas añadidas para ver cómo cambia el entorno proteico local de la alfa‑sinucleína una vez que se desencadena la agregación.
Vías celulares clave atraídas hacia los acúmulos
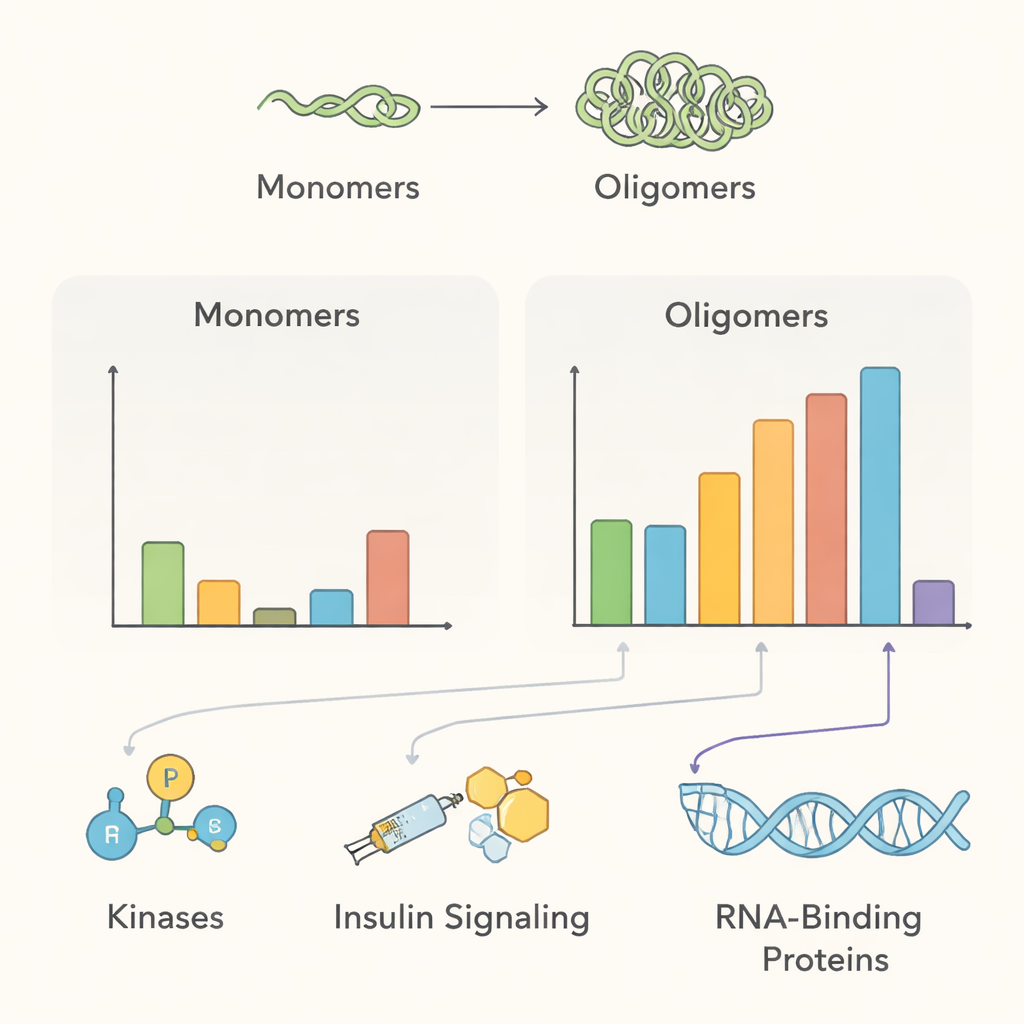
El esbozo del interactoma resultante señala varios temas biológicos principales. En condiciones normales, la alfa‑sinucleína multimérica se situaba cerca de muchas proteínas de tráfico de membranas y enzimas modificadoras de proteínas, coherente con su papel propuesto en ayudar a las neuronas a gestionar las vesículas sinápticas y mantener el control de calidad proteico. Varias enzimas que añaden grupos fosfato, incluidas las quinasas PAK4, RIPK2 y MAP4K4, se enriquecieron cerca de los multímeros saludables pero parecieron perder contacto una vez formados los agregados, lo que sugiere que la alteración de estas relaciones podría favorecer formas de la proteína vinculadas a la enfermedad. El equipo también detectó proteínas relacionadas con la señalización del factor de crecimiento similar a la insulina, apoyando los vínculos clínicos entre resistencia a la insulina y la enfermedad de Parkinson, y encontró que la agregación recluta proteínas implicadas en la eliminación de proteínas dañadas, como la familia de chaperonas 14‑3‑3 y componentes específicos de las vías de degradación celular.
Puentes inesperados hacia otros trastornos cerebrales
Más allá de la enfermedad de Parkinson, los datos subrayan una conexión sorprendente con la esclerosis lateral amiotrófica (ELA) y la demencia frontotemporal (DFT). Una proteína unión al ARN llamada FUS, que se deslocaliza y agrega en esas condiciones, apareció cerca de la alfa‑sinucleína multimérica tanto en condiciones normales como bajo agregación inducida. Otras proteínas relacionadas con ARN también cambiaron su proximidad a medida que la alfa‑sinucleína se agregaba. Estos hallazgos plantean la posibilidad de que pequeños ensamblajes de alfa‑sinucleína puedan atrapar proteínas manejadoras de ARN en lugares inadecuados dentro de las células, lo que potencialmente vincula la biología de las enfermedades con cuerpos de Lewy con la de la ELA y la DFT, aunque aún deben verificarse las interacciones físicas directas.
Qué significa esto para entender la enfermedad
Para lectores no especializados, la idea principal es que este trabajo ofrece una “lista de contactos” en etapa temprana de proteínas que viajan con la alfa‑sinucleína cuando pasa de ser un ayudante normal a un agregado dañino. El estudio sugiere que perder ciertas relaciones protectoras —como con quinasas específicas o enzimas de control de calidad— puede ser tan importante como ganar nuevos socios tóxicos. Si bien los experimentos se realizaron en un modelo celular simplificado y aún no prueban causalidad, destacan candidatos y vías concretas para ensayos futuros en neuronas y tejido cerebral. A la larga, mapear estos vecindarios proteicos cambiantes podría guiar estrategias para restaurar interacciones protectoras, apoyar la señalización relacionada con la insulina o prevenir la captura de proteínas unión al ARN, con el potencial de frenar la progresión desde cambios moleculares sutiles hasta enfermedades con cuerpos de Lewy plenamente desarrolladas.
Cita: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Palabras clave: alfa-sinucleína, enfermedad de cuerpos de Lewy, agregación de proteínas, proteómica de proximidad, enfermedad de Parkinson