Clear Sky Science · es
Perspectivas sobre las diferencias estructurales entre homo- y heterodímeros enriquecidos a partir de un cóctel de anticuerpos monoclonales contra SARS-CoV-2
Por qué mezclar anticuerpos puede generar sorpresas
Durante la pandemia de COVID-19, fármacos basados en anticuerpos como el cóctel REGEN-COV se emplearon para bloquear el virus causante de la enfermedad, SARS-CoV-2. Estos medicamentos se diseñan con precisión, pero una vez mezclados en un vial pueden formarse apareamientos raros denominados heterodímeros: dos anticuerpos distintos unidos en pareja. Este estudio plantea una pregunta práctica con grandes implicaciones para la seguridad y la eficacia: cuando se forman estos pares inusuales, ¿se comportan de manera diferente a los pares más familiares de anticuerpos idénticos, y podría eso modificar la efectividad del fármaco?
Pares inusuales en un potente fármaco contra la COVID-19
REGEN-COV combina dos anticuerpos monoclonales, casirivimab e imdevimab, cada uno diseñado para unirse a la proteína Spike de SARS-CoV-2 de forma distinta. Cuando ambos se formulan juntos, una fracción muy pequeña de los anticuerpos se asocia en pares. Algunos pares son homodímeros (dos copias del mismo anticuerpo); otros son heterodímeros (un casirivimab más un imdevimab). Los heterodímeros se consideran una impureza porque no forman parte del diseño original del medicamento, y su comportamiento en el organismo ha sido en gran medida desconocido. Los autores utilizaron primero un proceso de purificación en varios pasos para aislar varias especies de homodímeros distintas y el heterodímero a partir del mismo lote de REGEN-COV, lo que les brindó una rara oportunidad de comparar todas estas ensambladuras lado a lado.
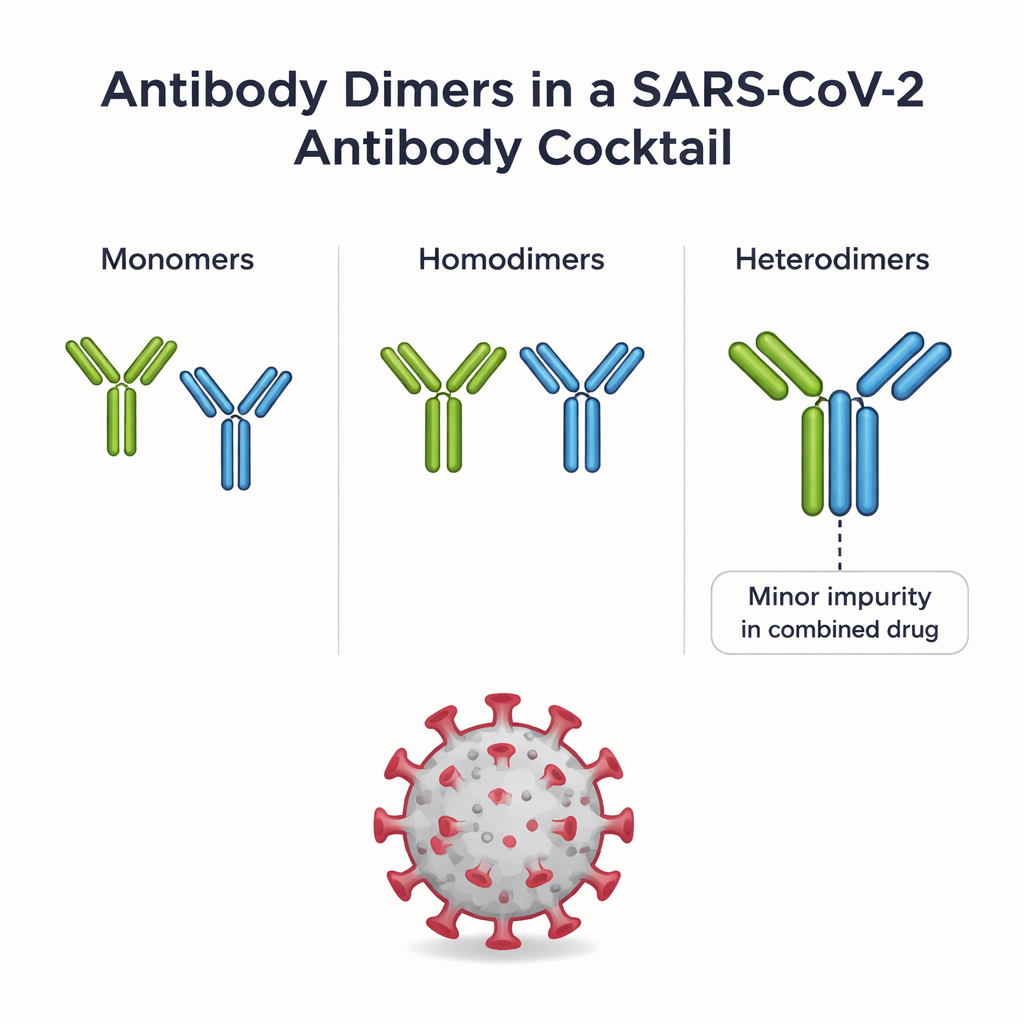
Explorando forma, adherencia y enlaces químicos
Para entender qué hace único a cada tipo de dímero, el equipo combinó varias herramientas analíticas de alto nivel. Experimentos de cromatografía revelaron cómo difieren los dímeros en la “adherencia” superficial (hidrofobicidad), mientras que electroforesis capilar y una forma especializada de espectrometría de masas mostraron si los dos anticuerpos en un dímero se mantienen juntos por atracciones débiles o por enlaces covalentes más fuertes. La microscopía electrónica y la ultracentrifugación analítica aportaron entonces información sobre la forma global: si un dímero es alargado y flexible o compacto y muy empaquetado. En conjunto, estos métodos mostraron que casirivimab e imdevimab forman varios homodímeros distintos con diferentes formas y patrones de enlace, y que el heterodímero es especialmente compacto y está enriquecido en enlaces covalentes que involucran distintas partes de los brazos y el tallo del anticuerpo.
Cómo la estructura se conecta con bloqueo viral y muerte celular
Los investigadores preguntaron a continuación cómo estas diferencias estructurales afectan lo que realmente importa: detener el virus y activar al sistema inmunitario. Probaron cada dímero en un ensayo de neutralización con pseudovirus, que mide lo bien que los anticuerpos bloquean la entrada de una partícula similar al virus, y en un ensayo de citotoxicidad celular dependiente de anticuerpos (ADCC), que evalúa cuán eficazmente los anticuerpos reclutan células inmunitarias para destruir objetivos infectados. Sorprendentemente, la mayoría de las formas dímeras fueron al menos tan buenas como, y en ocasiones mejores que, sus contrapartes monoméricas individuales en la neutralización del virus. En particular, los homodímeros de imdevimab mostraron una neutralización “hiperpotente”, probablemente porque su geometría les permite unir varios picos (spikes) en la superficie viral. Algunos homodímeros de casirivimab produjeron señales de ADCC especialmente fuertes, aparentemente porque su orientación deja las regiones de cola (las porciones Fc) bien expuestas a los receptores de las células inmunitarias.
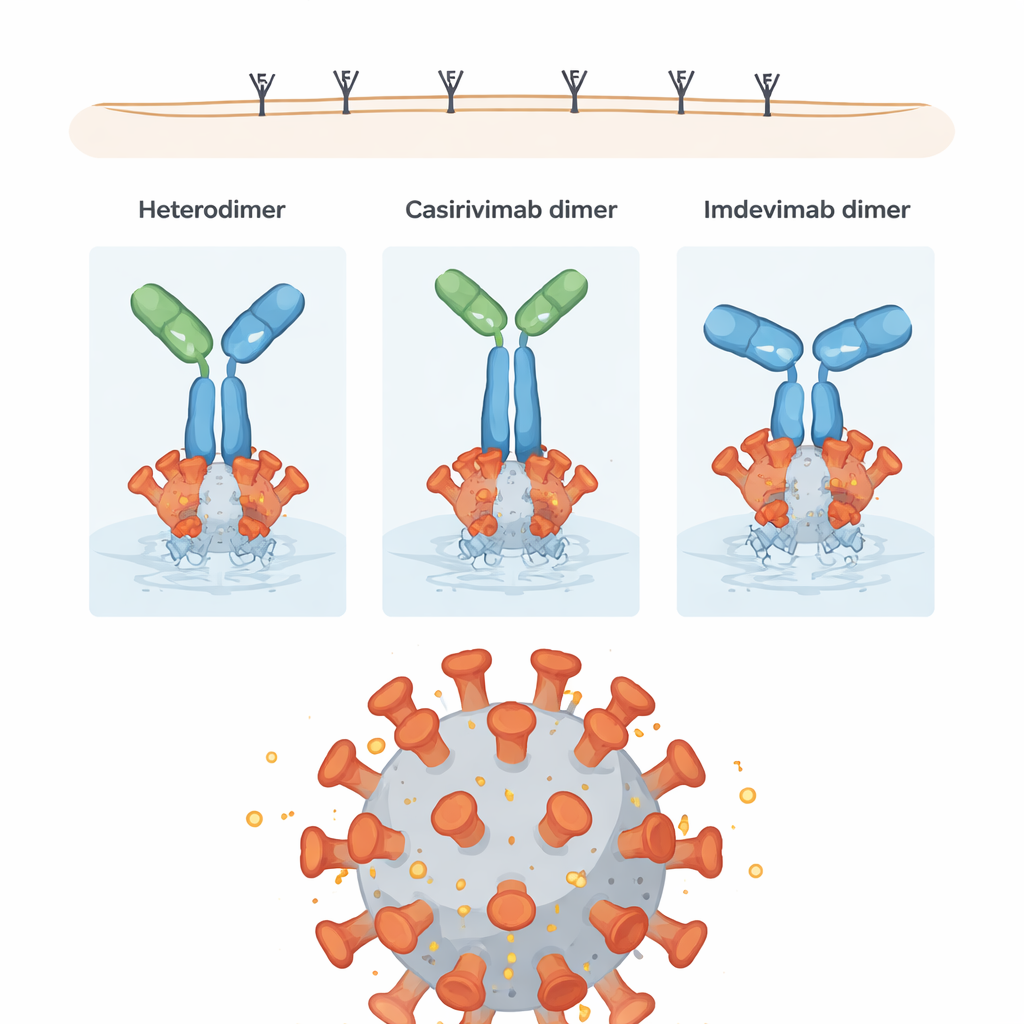
Una impureza compacta con rendimiento mixto
El heterodímero, a pesar de ser rico en conexiones fuertes y compactas entre sus dos anticuerpos distintos, mostró un rendimiento algo reducido: alrededor del 70% de la actividad neutralizante y de ADCC de la mezcla coformulada prevista. El extenso entrecruzamiento entre sus brazos y tallos parece restringir la libertad de rotación y reorientación de la molécula cuando se une a la espícula viral, lo que a su vez puede limitar tanto el bloqueo del virus como la señalización a las células inmunitarias. Aun así, muchos de sus enlaces son de un tipo que puede romperse lentamente en condiciones fisiológicas, lo que hace que el heterodímero sea relativamente inestable con el tiempo y propenso a volver a convertirse en anticuerpos individuales.
Qué significa esto para los medicamentos basados en anticuerpos
Para pacientes y desarrolladores de fármacos, la conclusión es tranquilizadora pero matizada. Este análisis en profundidad de los dímeros en REGEN-COV sugiere que la mayoría de las formas dímeras, incluida la inusual impureza heterodímera, conservan una actividad antivírica sustancial, y no hay una señal clara de riesgo adicional de seguridad por agregados de orden superior en este sistema. Al mismo tiempo, el trabajo muestra que los detalles finos —dónde se tocan los anticuerpos, qué tan fuertemente están entrecruzados y cuán compactos o alargados son— pueden modificar de manera significativa la potencia. Los autores sostienen que un perfil estructural y funcional similar de los dímeros en otros fármacos de anticuerpos podría convertirse en una herramienta no clínica potente para comprender y gestionar impurezas, y podría incluso inspirar nuevos anticuerpos multiméricos diseñados deliberadamente que aprovechen la geometría para ajustarse mejor y neutralizar virus.
Cita: Nguyen, J.B., Liu, S., Yan, Y. et al. Insights into the structural differences between homo- and heterodimers enriched from a cocktail of monoclonal antibodies against SARS-CoV-2. Sci Rep 16, 7024 (2026). https://doi.org/10.1038/s41598-026-37545-4
Palabras clave: dímeros de anticuerpos, REGEN-COV, espícula de SARS-CoV-2, cócteles de anticuerpos monoclonales, agregados proteicos