Clear Sky Science · es
Inmovilización covalente de la peroxidasa de Lepidium draba en nanopartículas magnéticas recubiertas de quitosano y su aplicación en biosensores de glucosa
Por qué importan los imanes diminutos para la glucemia
Mantener el nivel de azúcar en sangre bajo control es crucial para gestionar la diabetes y prevenir daños a largo plazo en el corazón, los riñones, los ojos y los nervios. Las pruebas de glucosa actuales funcionan bien, pero las enzimas que contienen pueden ser frágiles, de vida corta y difíciles de reutilizar, lo que aumenta los costes y los residuos. Este estudio explora una forma ingeniosa de hacer que una enzima vegetal sea más resistente y duradera al fijarla sobre micropartículas magnéticas, abriendo la puerta a pruebas de glucosa más rápidas, fiables y potencialmente más baratas.
Un aliado vegetal inspirado en el rábano picante
Muchas pruebas médicas se basan en enzimas—proteínas que aceleran reacciones químicas. Un pilar en los laboratorios diagnósticos es la peroxidasa de rábano picante, utilizada para convertir cambios químicos invisibles en variaciones de color claras que pueden verse a simple vista. Los investigadores trabajaron con un pariente vegetal cercano de esta enzima, llamada peroxidasa de Lepidium draba, producida en bacterias para poder obtenerla en grandes cantidades. Por sí sola, esta enzima libre es potente pero delicada: pierde actividad con el calor, el almacenamiento y el uso repetido, lo que limita su utilidad en sensores industriales y kits clínicos.
Convertir enzimas en herramientas magnéticas
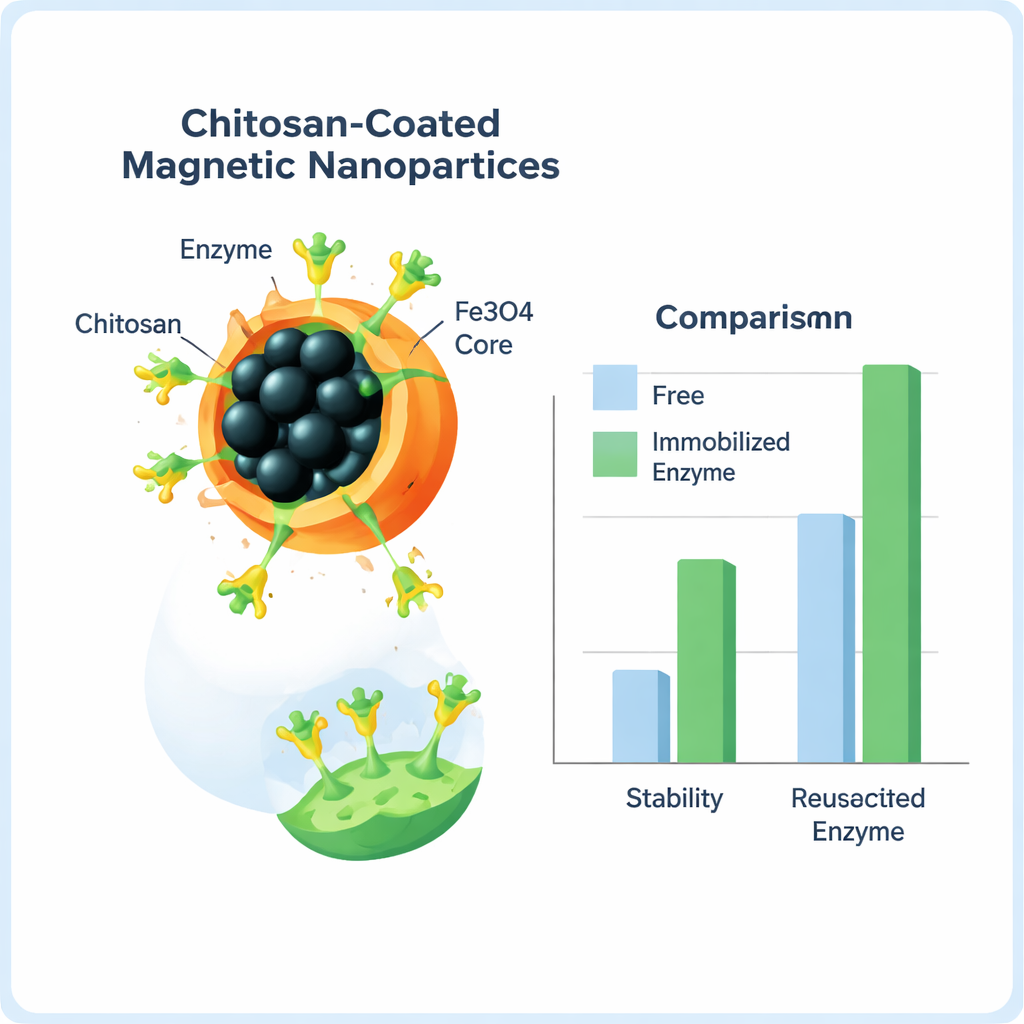
Para proteger y reutilizar la enzima, el equipo la fijó a nanopartículas de óxido de hierro—minúsculos granos de material magnético—recubiertas con un polímero natural llamado quitosano, derivado de caparazones de crustáceos. El quitosano proporciona una capa suave y biocompatible llena de “mangos” químicos que pueden sujetar enzimas. Empleando una pequeña molécula entrecruzante, glutaraldehído, formaron enlaces covalentes fuertes entre la enzima y las partículas recubiertas. Los científicos ajustaron luego la cantidad de entrecruzante, la duración de la reacción y la cantidad de material soporte añadido, adoptando condiciones que ofrecieron el mejor equilibrio entre la cantidad de enzima inmovilizada y la actividad que conservaba.
Comprobar estructura, robustez y permanencia
Tras la inmovilización, el equipo confirmó que la enzima estaba realmente sobre las partículas usando varias técnicas estructurales que detectan vibraciones de enlace, patrones cristalinos y la morfología superficial. Más importante para el uso real, la enzima inmovilizada se comportó mejor que su forma libre. Se unió con mayor afinidad a su sustrato colorimétrico y lo convirtió en producto coloreado con mucha más eficiencia—hasta 11 veces mayor eficiencia catalítica en algunas pruebas. La enzima fijada también toleró un rango más amplio de acidez, mantuvo mayor actividad en temperaturas útiles y resistió el calentamiento a 50 °C durante mucho más tiempo. Su vida media a esa temperatura se más que duplicó y, tras dos meses en frigorífico, conservó aproximadamente el doble de actividad que la enzima libre. Como las partículas son magnéticas, pudieron extraerse de la solución con un imán y reutilizarse; incluso tras 11 ciclos de reacción, se mantuvo alrededor del 40% de la actividad inicial.
Cambio de color más nítido para pruebas de glucosa
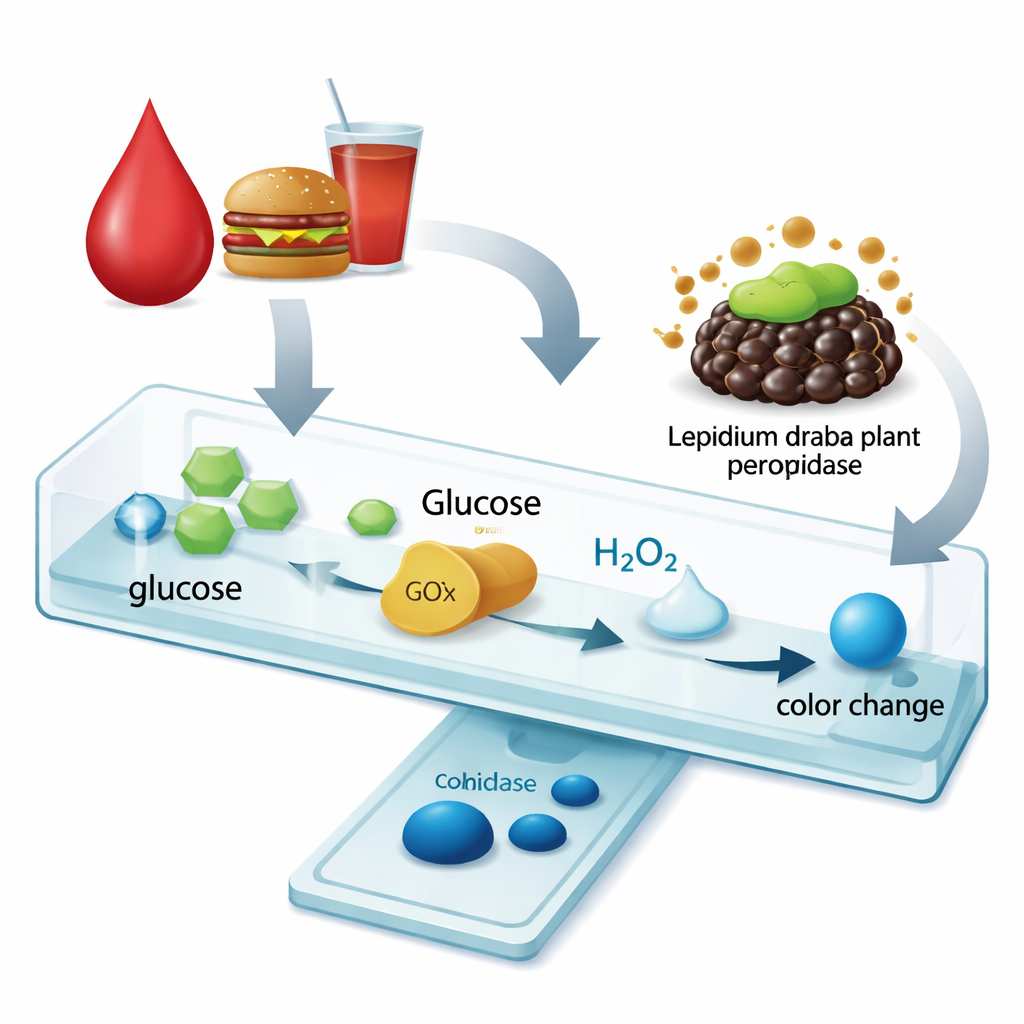
Para comprobar si esta enzima más resistente realmente mejora una prueba práctica, los investigadores construyeron un ensayo colorimétrico sencillo para glucosa. Primero, una enzima estándar, la glucosa oxidasa, convierte la glucosa en peróxido de hidrógeno. Luego la peroxidasa de Lepidium draba, ya sea libre o inmovilizada en las perlas de quitosano magnéticas, utiliza ese peróxido para transformar un tinte incoloro en azul intenso. Con la forma inmovilizada, el rango útil de medida para glucosa se amplió drásticamente—pasando de cubrir solo 0,1 a 1 milimol por litro con la enzima libre a 0,1 a 10 milimoles por litro cuando estaba inmovilizada. Al mismo tiempo, el tiempo de reacción necesario para el ensayo se redujo a aproximadamente un tercio, mientras que el límite mínimo detectable de glucosa se mantuvo muy bajo y clínicamente relevante.
Qué significa esto para la salud cotidiana
Al anclar una enzima vegetal sobre nanopartículas magnéticas recubiertas de quitosano, los autores crearon un componente de sensor de glucosa colorimétrico robusto, reutilizable y muy sensible. Para un público general, esto significa que en el futuro las tiras reactivas, los kits de laboratorio o incluso el envasado inteligente de alimentos podrían volverse más estables, más precisos en un rango más amplio de azúcares y potencialmente más baratos porque la enzima activa puede recuperarse y reutilizarse. Aunque se necesita trabajo adicional para aumentar la cantidad de enzima que las partículas pueden soportar y para extender el enfoque a otros marcadores sanguíneos como el colesterol o la urea, este estudio muestra cómo los nanomateriales y los polímeros naturales pueden combinarse para mejorar herramientas bioquímicas familiares, haciéndolas más resistentes, limpias y versátiles para diagnósticos.
Cita: Sepahi-Baghan, M., Asoodeh, A. & Riahi-Madvar, A. Covalent immobilization of Lepidium draba peroxidase on chitosan-coated magnetic nanoparticles and its application in glucose biosensing. Sci Rep 16, 7035 (2026). https://doi.org/10.1038/s41598-026-37542-7
Palabras clave: biosensor de glucosa, inmovilización de enzimas, nanopartículas magnéticas, detección colorimétrica, peroxidasa