Clear Sky Science · es
Interacción del campo electromagnético pulsado de baja frecuencia (PEMF) con las mitocondrias
Campos suaves y las centrales energéticas de la célula
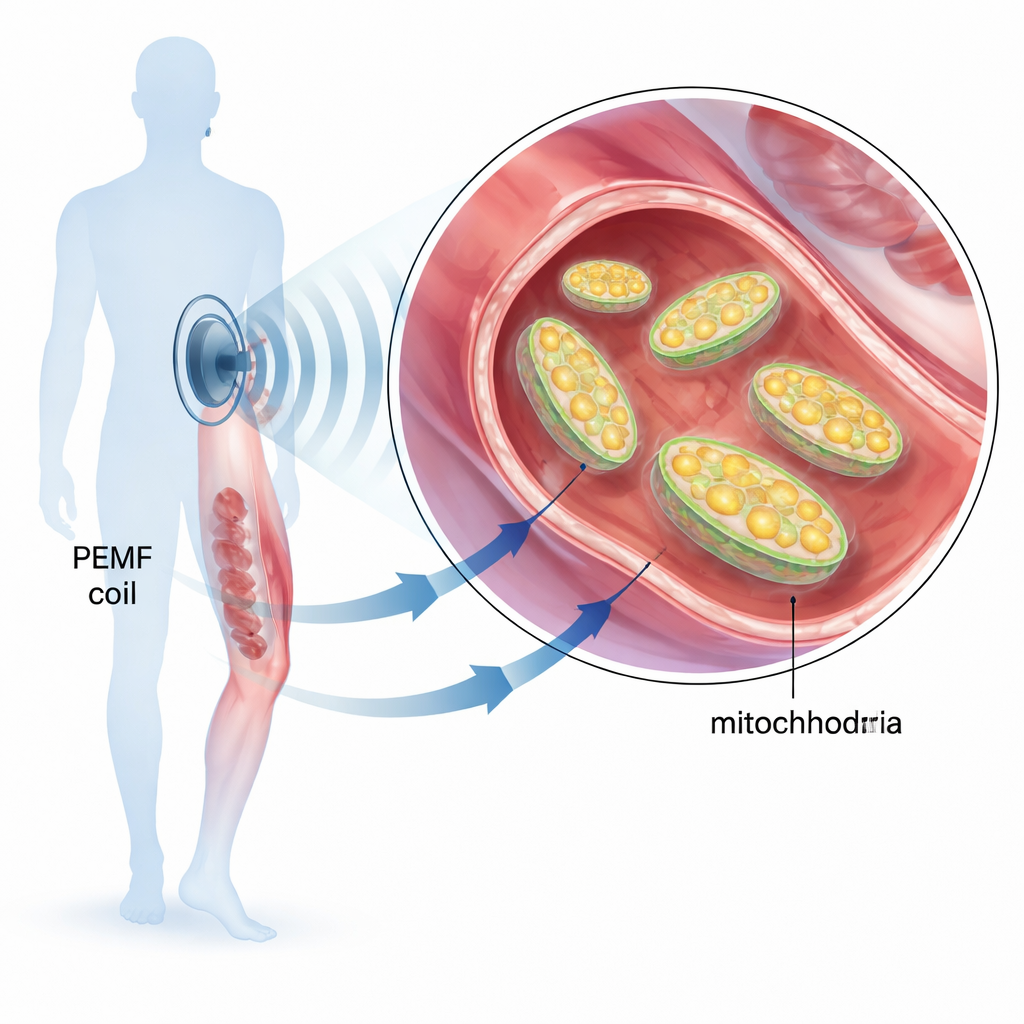
La terapia con campo electromagnético pulsado (PEMF) ya se emplea en clínicas para ayudar a soldar fracturas, aliviar el dolor articular y acelerar la recuperación tras cirugías. Aun así, no comprendemos por completo cómo actúan estos campos suaves de baja frecuencia dentro de nuestro organismo. Este estudio plantea una pregunta simple pero importante: ¿influyen directamente las señales PEMF sobre las mitocondrias, las pequeñas centrales energéticas de las células que generan la mayor parte de nuestra energía, y en caso afirmativo, cómo lo hacen?
Por qué las mitocondrias importan para la salud cotidiana
Las mitocondrias convierten los alimentos y el oxígeno en ATP, la “moneda energética” universal de las células. Cuando las mitocondrias fallan, los tejidos se reparan más lentamente, los músculos se fatigan antes y pueden agravarse enfermedades asociadas a un metabolismo deficiente. Dado que trabajos previos sugirieron que los tratamientos con PEMF mejoran el metabolismo energético y favorecen la reparación tisular, los autores se centraron en si un dispositivo PEMF específico podía afinar la actividad mitocondrial. Usaron una señal magnética bien definida: pulsos cortos de milisegundos de una onda senoidal de 30 kHz con baja energía de entrada, aplicada a células musculares en cultivo, a tejidos de rata y a mitocondrias purificadas.
Mirando más de cerca dentro de las células vivas
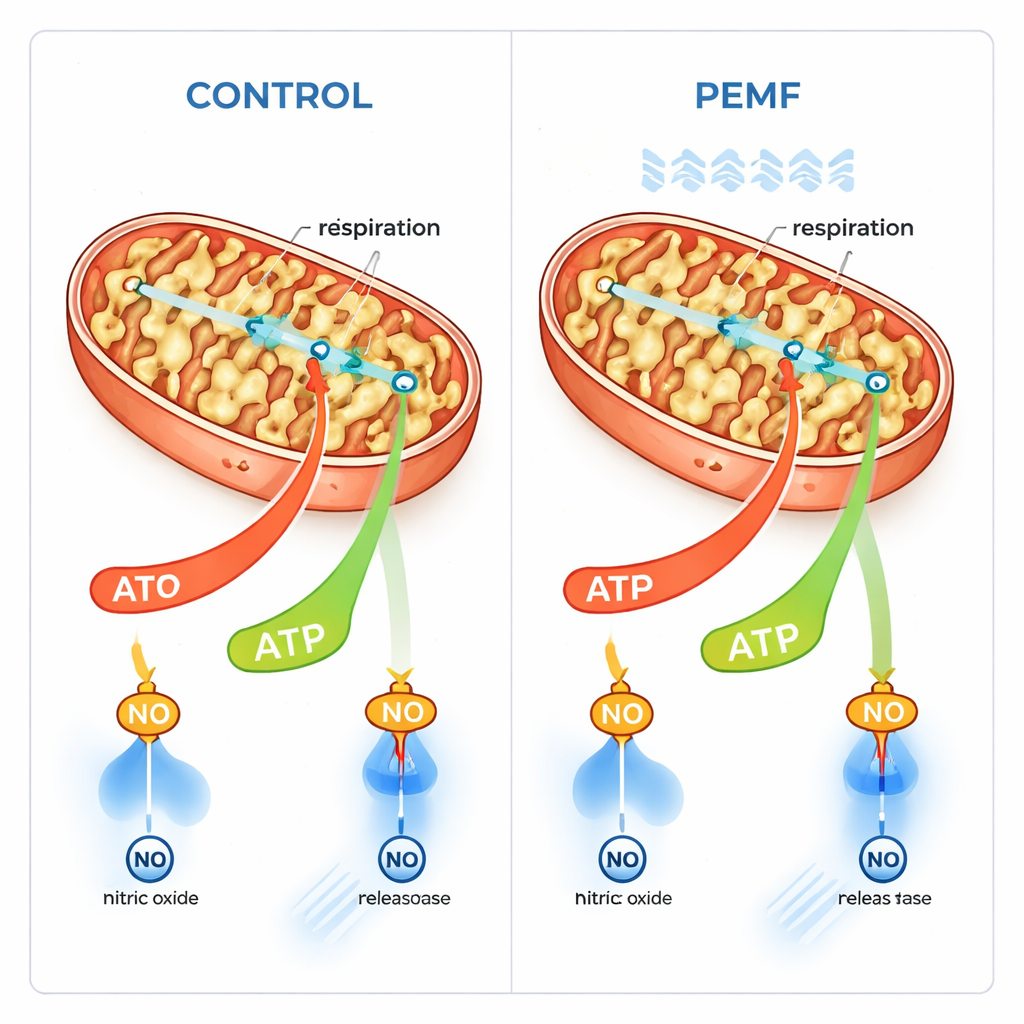
En células musculares humanas cultivadas en el laboratorio, el equipo midió tres indicadores clave tras la exposición a PEMF: el potencial eléctrico a través de la membrana interna mitocondrial (una especie de diminuta batería), los niveles de especies reactivas de oxígeno (altos niveles pueden ser dañinos) y el óxido nítrico, un gas que puede bloquear temporalmente la respiración mitocondrial. Unos 90 minutos después del tratamiento, el potencial de membrana mitocondrial era modestamente menor, mientras que los niveles de óxido nítrico se reducían; las especies reactivas de oxígeno no aumentaron. Una ligera caída del potencial de membrana puede indicar ya sea daño o una mayor actividad en la producción de ATP. Puesto que las células no mostraron signos de estrés, los autores sospecharon que las mitocondrias estaban simplemente trabajando un poco más y consumiendo el voltaje almacenado en su membrana interna.
Poniendo a prueba cómo “respiran” las mitocondrias
Para probar esta idea de forma más directa, los investigadores perforaron suavemente la membrana celular externa para poder suministrar con precisión distintos combustibles a las mitocondrias y medir el consumo de oxígeno. Consistentemente observaron una tendencia hacia una respiración mayor asociada a la producción de ATP tras el PEMF, especialmente cuando estaba presente glutamato, un combustible mitocondrial habitual. El análisis estadístico de muchas muestras sugirió que la combinación de la exposición a PEMF y la elección del combustible configuraba de forma significativa la velocidad con la que las mitocondrias consumían oxígeno. Importante: no hubo indicios de que el PEMF dañara las células ni sus mitocondrias. En cambio, los campos parecieron estimular selectivamente el modo “acoplado” de respiración, donde el consumo de oxígeno está estrechamente ligado a la fabricación de ATP, sin aumentar la quema poco eficiente e desacoplada del combustible.
Inflamación, óxido nítrico y una sorpresa de la luz azul
Dado que el óxido nítrico puede acumularse durante la inflamación y bloquear un paso clave en la respiración mitocondrial, el equipo preguntó si el PEMF podría ayudar a las mitocondrias a recuperarse de tal inhibición. Añadieron un donador químico de óxido nítrico a homogenizados de tejido muscular y hepático y a mitocondrias hepáticas aisladas, lo que ralentizó fuertemente la respiración. En estas condiciones, el PEMF no restauró la función mitocondrial, ni siquiera cuando las mitocondrias estaban altamente concentradas. Para comprobar si el bloqueo era reversible en absoluto, iluminaron con luz azul las mitocondrias inhibidas por óxido nítrico, usando un método conocido por desprender el óxido nítrico de su sitio de unión. La luz azul rescató parcialmente la respiración, confirmando que el sistema podía recuperarse, pero el PEMF no aportó ningún beneficio adicional. Esto mostró que los efectos positivos del PEMF no se deben a la eliminación del óxido nítrico en condiciones tipo inflamatorias.
Compuertas de membrana y flujo de energía
Trazando una analogía entre células y circuitos eléctricos, los autores sugieren que el PEMF podría actuar principalmente sobre las membranas biológicas. Las mitocondrias están envueltas por una membrana externa que contiene una proteína de pasaje clave llamada VDAC, que permite el paso de moléculas relacionadas con la energía. A diferencia del voltaje muy alto de la membrana interna, la membrana externa tiene un voltaje menor y más fácilmente influenciable. Los autores proponen que el PEMF altera sutilmente este potencial de la membrana externa, cambiando la frecuencia de apertura de las compuertas de VDAC y, con ello, facilitando el flujo de combustible y de ATP consumido a través de la membrana. Esto aumentaría de forma natural el modo acoplado de respiración que produce ATP sin modificar la capacidad máxima de la propia maquinaria de transporte de electrones.
Qué significa esto para terapias futuras
En conjunto, el estudio no encuentra evidencia de que este tipo de PEMF sea perjudicial para las mitocondrias. Al contrario, el PEMF mejora suavemente la parte de la respiración mitocondrial que produce ATP, mientras deja sin cambios la capacidad respiratoria máxima y el estrés oxidativo. Sin embargo, no rescata a las mitocondrias bloqueadas por altos niveles de óxido nítrico, lo que sugiere que sus beneficios en tejidos inflamados deben surgir por otras vías. Para pacientes y clínicos, estos resultados respaldan la idea de que campos electromagnéticos cuidadosamente ajustados pueden empujar a las centrales celulares hacia un estado más eficiente de producción de energía, ofreciendo una explicación mecanística plausible para algunos de los efectos curativos reportados en la reparación ósea, el cuidado de heridas y la recuperación postoperatoria.
Cita: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Palabras clave: terapia con campo electromagnético pulsado, mitocondrias, energía celular, óxido nítrico, producción de ATP