Clear Sky Science · es
Validación de un nuevo biomarcador genómico de la escalabilidad de células madre mesenquimales e implicaciones del estado genotípico en fenotipos de senescencia celular
Por qué cultivar células madre se vuelve más difícil con el tiempo
Las células madre procedentes de la médula ósea adulta son una pieza central de muchas terapias experimentales, desde reparar huesos dañados hasta reducir la inflamación. Pero hay un inconveniente: para tratar a un paciente, los laboratorios deben ampliar estas células fuera del cuerpo, y cuanto más se expanden, más ralentizan su crecimiento y se comportan como células “envejecidas”. Este estudio explora por qué las células madre de algunas personas envejecen más despacio en el cultivo y si un pequeño fragmento de ADN ausente puede ayudar a los científicos a seleccionar las células más robustas para futuros tratamientos.
Un gen ausente que cambia las reglas
Los investigadores se centraron en un gen llamado GSTT1, que ayuda a las células a desintoxicar moléculas dañinas producidas durante el metabolismo y el estrés. Sorprendentemente, una fracción considerable de la población carece por completo de este gen: son “GSTT1 nulos”. Trabajos previos sugerían que las células madre de médula ósea de estos individuos podrían proliferar más rápido y conservar más tiempo las vainas protectoras de los cromosomas, llamadas telómeros. En este proyecto, el equipo examinó células madre de seis donantes sanos, las agrupó en GSTT1-positivas y GSTT1-nulas, y luego siguió su comportamiento durante muchas rondas de expansión y después de la exposición a radiación de rayos X, un fuerte desencadenante de envejecimiento celular.
Células de rápido crecimiento que resisten señales de envejecimiento
Cuando los científicos midieron el número de células a lo largo de varios días, las células madre GSTT1-nulas se multiplicaron más rápidamente en pasajes tempranos que las células portadoras del gen. Tras una expansión muy prolongada, las tasas de crecimiento entre los grupos se hicieron más parecidas, pero la ventaja inicial quedó clara. Para sondear el envejecimiento directamente, el equipo usó una tinción clásica que vuelve azules a las células senescentes, o “envejecidas”. Tras muchas rondas de división y de nuevo después de la irradiación, los cultivos GSTT1-nulos contenían de forma consistente menos células azules y senescentes que los cultivos GSTT1-positivos. Es importante destacar que esta diferencia no se debió a un acortamiento más lento de los telómeros ni a una mayor actividad de la enzima que los mantiene (hTERT); ambas medidas fueron similares independientemente del estado GSTT1, lo que sugiere que opera otro mecanismo.
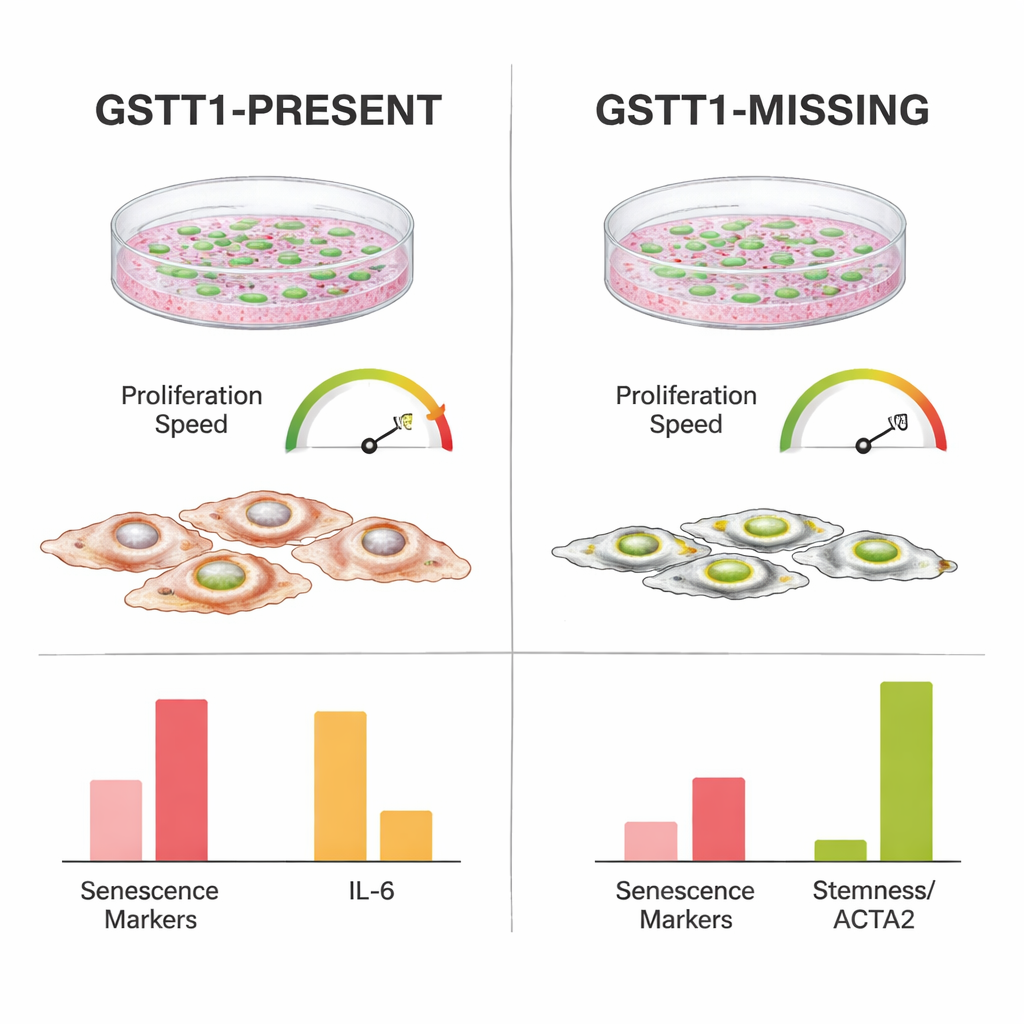
Menos estrés e inflamación en el cultivo
Para comprender qué hacía a las células GSTT1-nulas más resistentes, los investigadores midieron la actividad de genes relacionados con la detención del ciclo celular, el daño del ADN y el denominado fenotipo secretor asociado a la senescencia —un cóctel de señales inflamatorias y de estrés que liberan las células envejecidas. Las células con GSTT1 mostraron niveles más altos de señales clave de “paro” como p21 y p14, especialmente en pasajes tardíos y tras la irradiación. También aumentaron más fuertemente IL‑6, una potente molécula inflamatoria, y otros genes relacionados con el estrés que las células GSTT1-nulas. En contraste, las células madre GSTT1-nulas mantuvieron niveles más bajos de estos marcadores de envejecimiento e inflamación, a la vez que conservaron niveles más altos de ACTA2 y TWIST1, genes asociados con la integridad estructural y un comportamiento más parecido al de células madre. Cabe destacar que ambos genotipos conservaron una capacidad similar para especializarse en células óseas y adiposas, lo que sugiere que el efecto protector no se debía simplemente a la pérdida de la función normal de las células madre.
Qué podría significar esto para futuras terapias celulares
En conjunto, los hallazgos sugieren que las células madre de médula ósea que carecen de GSTT1 están parcialmente protegidas del desgaste habitual de la expansión en laboratorio y de la radiación. Crecen más rápido al principio, acumulan menos células visiblemente envejecidas y mantienen un perfil menos inflamatorio, aunque sus cromosomas se acortan a ritmos similares. Para empresas y clínicas que fabrican grandes cantidades de células madre, el estado GSTT1-nulo podría servir como un marcador genético práctico para identificar donantes cuyas células toleran mejor la expansión, lo que podría producir terapias más consistentes y potentes. Por supuesto, el estudio usó una cohorte pequeña y condiciones de cultivo no clínicas, por lo que se necesitan estudios más amplios y controlados. Aun así, el trabajo subraya cómo una sola diferencia heredada puede inclinar la balanza entre un comportamiento juvenil y uno envejecido en células madre cultivadas para medicina regenerativa.
Cita: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Palabras clave: células madre mesenquimales, senescencia celular, biomarcadores, fabricación de terapias celulares, polimorfismo GSTT1