Clear Sky Science · es
Nuevas perspectivas sobre la base molecular de la gametogénesis en la rana de agua hibridogenética Pelophylax esculentus
Por qué importan estas ranas singulares
La mayoría de los animales, incluidos los humanos, reordenan sus genes cada generación cuando se unen el espermatozoide y el óvulo. Pero algunas criaturas inusuales doblan esas reglas y transmiten genomas enteros como clones listos para funcionar. Las ranas de agua europeas pertenecen a este grupo selecto. Son experimentos vivientes sobre cómo el sexo, la asexualidad y la hibridación pueden entrelazarse. Entender cómo estas ranas fabrican sus óvulos y espermatozoides no solo satisface la curiosidad por un anfibio peculiar: también arroja luz sobre cómo se controlan, reparan y, a veces, editan implacablemente los genomas en todos los vertebrados.
Ranas que rompen las reglas de la herencia
En muchas charcas europeas coexisten tres ranas de agua estrechamente relacionadas. Dos son especies sexuales ordinarias, denominadas aquí simplemente L y R. Cuando se reproducen, pueden producir un híbrido, LR, conocido como Pelophylax esculentus. Este híbrido hace algo notable: en su línea germinal —las células que se convertirán en óvulos o espermatozoides— expulsa un genoma parental y copia el otro sin mezclarlo. El resultado es un gameto clonal que porta ya sea un genoma L intacto o un genoma R intacto, que luego es fertilizado por un gameto normal de una de las especies parentales. Dependiendo del “sistema poblacional” local, los híbridos pueden excluir rutinariamente el genoma R, el genoma L o, en algunos lugares, ambos en distintos individuos. El estudio plantea la pregunta: ¿qué genes ayudan a orquestar esta exclusión dirigida del genoma y la herencia clonal?
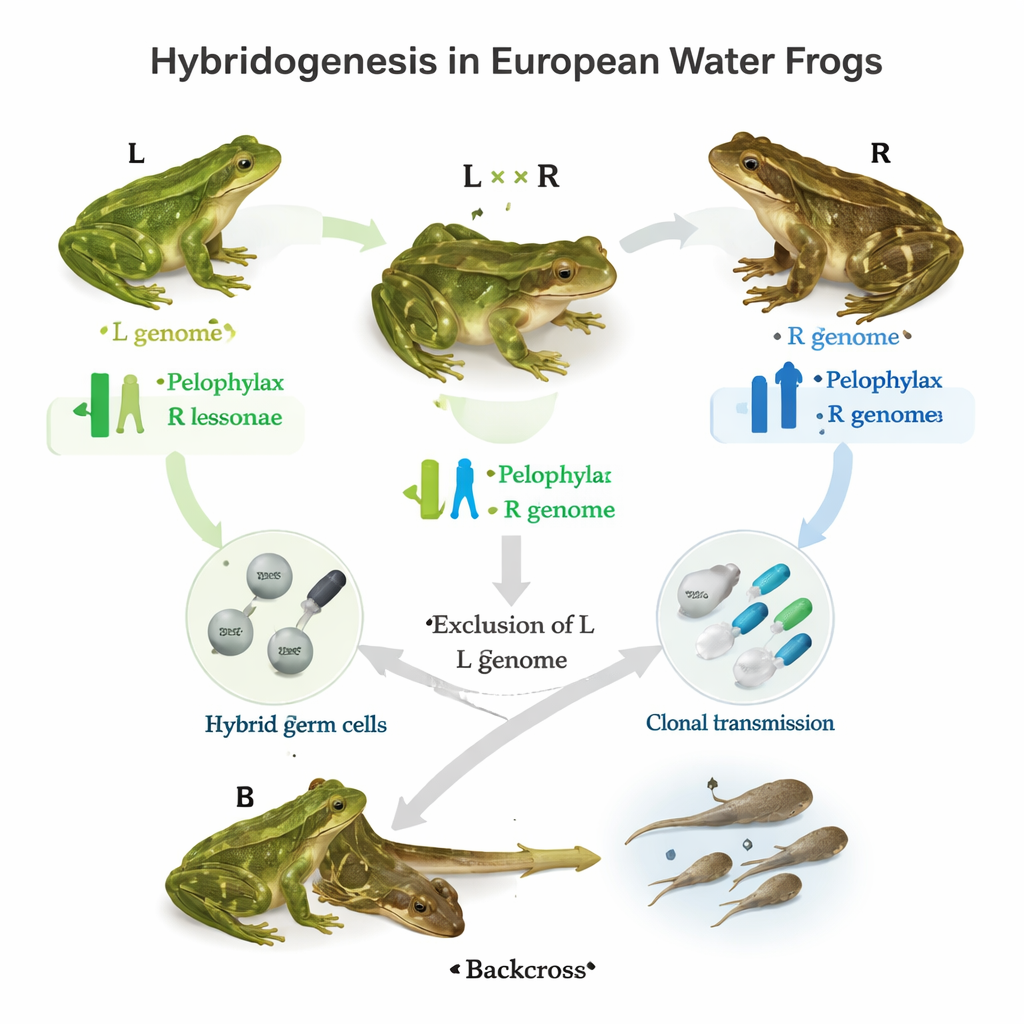
En busca de los genes detrás del sexo clonal
Los autores primero elaboraron un catálogo de 160 genes conocidos en otros animales por participar en la gametogénesis —el proceso de formar óvulos y espermatozoides. Secuenciaron estos genes a partir de testículos de ranas L y R y compararon sus propiedades básicas, como longitud, estructura y composición de bases de ADN. La mayoría de estos genes resultaron estar muy conservados entre las dos especies, lo que sugiere que desempeñan funciones importantes que toleran pocos cambios. A continuación, el equipo se concentró en 52 de estos genes y los escaneó en busca de diferencias de una sola letra en el ADN, conocidas como polimorfismos de nucleótido único (SNP), en más de 650 ranas recogidas por Europa. Estos individuos procedían de distintos sistemas poblacionales: aquellos donde coexisten solo L y híbridos, aquellos con solo R y híbridos, sistemas exclusivamente híbridos ricos en ranas triploides, y poblaciones puramente R.
Señales de flujo génico y estructura oculta
Al examinar los patrones de variación de los SNP, los investigadores desenterraron evidencia de introgresión —flujo génico— entre los reservorios genéticos L y R. En varios genes, las versiones R eran casi indistinguibles de sus contrapartes L, lo que se explica mejor por hibridación pasada y retrocruzamiento. Aunque las tasas globales de flujo génico eran bajas, eran más altas hacia R que hacia L, coincidiendo con trabajos genéticos previos. Cuando el equipo comparó las frecuencias de SNP entre sistemas poblacionales, hallaron que ciertas variantes genéticas se agrupaban fuertemente con sistemas particulares. Por ejemplo, los híbridos LR de poblaciones totalmente híbridas eran genéticamente más similares a LR de sistemas R–híbrido que a LR de sistemas diploides L–híbrido puros, revelando una estructura oculta vinculada a cómo se organiza la reproducción a escala local.
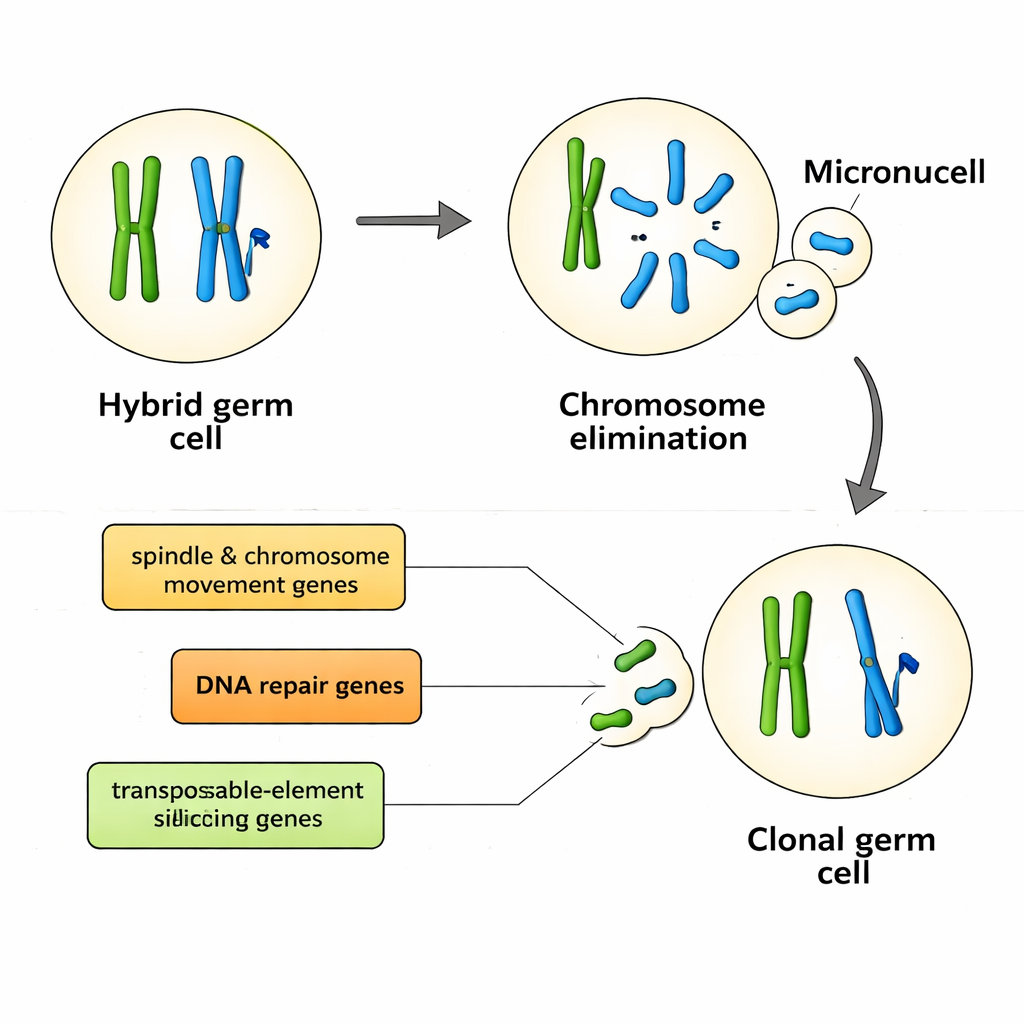
Actores clave en el control cromosómico y la defensa del genoma
Diez genes, en particular, mostraron asociaciones fuertes con el sistema poblacional y, por tanto, con la manera en que se excluyen los genomas y se transmiten de forma clonal. Se agrupan en varias funciones. Algunos, como kif22 y nusap1, ayudan a construir y controlar el huso, la maquinaria celular que mueve los cromosomas durante la división celular. Otros, incluidos hormad1, rad50, rad51ap1 y sfr1, son centrales para generar y reparar roturas de doble cadena en el ADN —cortes controlados que normalmente promueven la recombinación pero que también podrían desencadenar la eliminación dirigida de cromosomas. Otro gen, henmt1, estabiliza pequeños ARN que silencian elementos transponibles, los fragmentos de ADN móviles que pueden dañar los genomas o remodelar los centrómeros, los puntos de anclaje necesarios para una segregación cromosómica adecuada. En conjunto, estos genes dibujan un panorama en el que la exclusión del genoma surge de la interacción entre el transporte cromosómico, la reparación del ADN y las vías de defensa del genoma, no de un único interruptor maestro.
Evolución en el filo de la estabilidad
El estudio sugiere que la recombinación rara y el flujo génico bidireccional entre L y R han ayudado a generar variantes genómicas distintas que favorecen diferentes modos de herencia no mendeliana. Algunas líneas híbridas pueden acumular mutaciones dañinas a medida que sus genomas clonales avanzan en una especie de trinquete, mientras que la recombinación esporádica y la introgresión ocasionalmente los renuevan, a costa de problemas de desarrollo en algunos descendientes. En lugar de encajar en una regla simple basada en cuánto se han divergido dos especies, el sistema Pelophylax parece estar regido por una red compleja de factores interaccionantes que afinan si un híbrido se convierte en una línea clonal estable o en un callejón sin salida.
Qué significa esto más allá de las ranas
Para el lector general, la conclusión es que la herencia puede ser mucho más flexible de lo que sugieren los diagramas mendelianos de libro de texto. Estas ranas de agua revelan que los genomas de los vertebrados pueden ser eliminados selectivamente, copiados y reutilizados como bloques modulares, según el contexto. Al identificar genes reales ligados a este proceso, el estudio transforma un truco reproductivo inusual en un problema molecular abordable. Experimentos futuros, guiados por este nuevo catálogo de genes, pondrán a prueba cómo pequeñas modificaciones en las vías de manejo cromosómico y defensa del genoma pueden hacer que una población pase del sexo ordinario a la reproducción híbrida clonal —una visión que, en última instancia, podría iluminar la fertilidad, la estabilidad genómica y la evolución del sexo en muchos otros animales.
Cita: Plötner, M., Meixner, M., Poustka, A.J. et al. New insights into the molecular basis of gametogenesis in the hybridogenetic water frog Pelophylax esculentus. Sci Rep 16, 5012 (2026). https://doi.org/10.1038/s41598-026-37515-w
Palabras clave: hibridogénesis, ranas de agua, herencia clonal, exclusión del genoma, gametogénesis