Clear Sky Science · es
Bloqueo excepcionalmente selectivo del sensor de voltaje de los canales NaV1.5 por Mg-protoporfirina perjudica la migración de células cancerosas
Un pigmento vegetal apunta a una nueva estrategia contra el cáncer
Nuestros corazones y nuestros tumores pueden compartir una vulnerabilidad inesperada: un tipo especial de puerta eléctrica en la membrana celular llamada NaV1.5. Este estudio muestra que un pariente natural de los bloques constructores de la clorofila en las plantas, la magnesio‑protoporfirina IX (MgPpIX), puede cerrar esta puerta con una precisión extraordinaria. Al hacerlo, ralentiza de forma marcada el movimiento de ciertas células cancerosas, lo que sugiere que una molécula inspirada en la química de la fotosíntesis podría ayudar a domar la metástasis sin perturbar en gran medida el cerebro o los músculos.
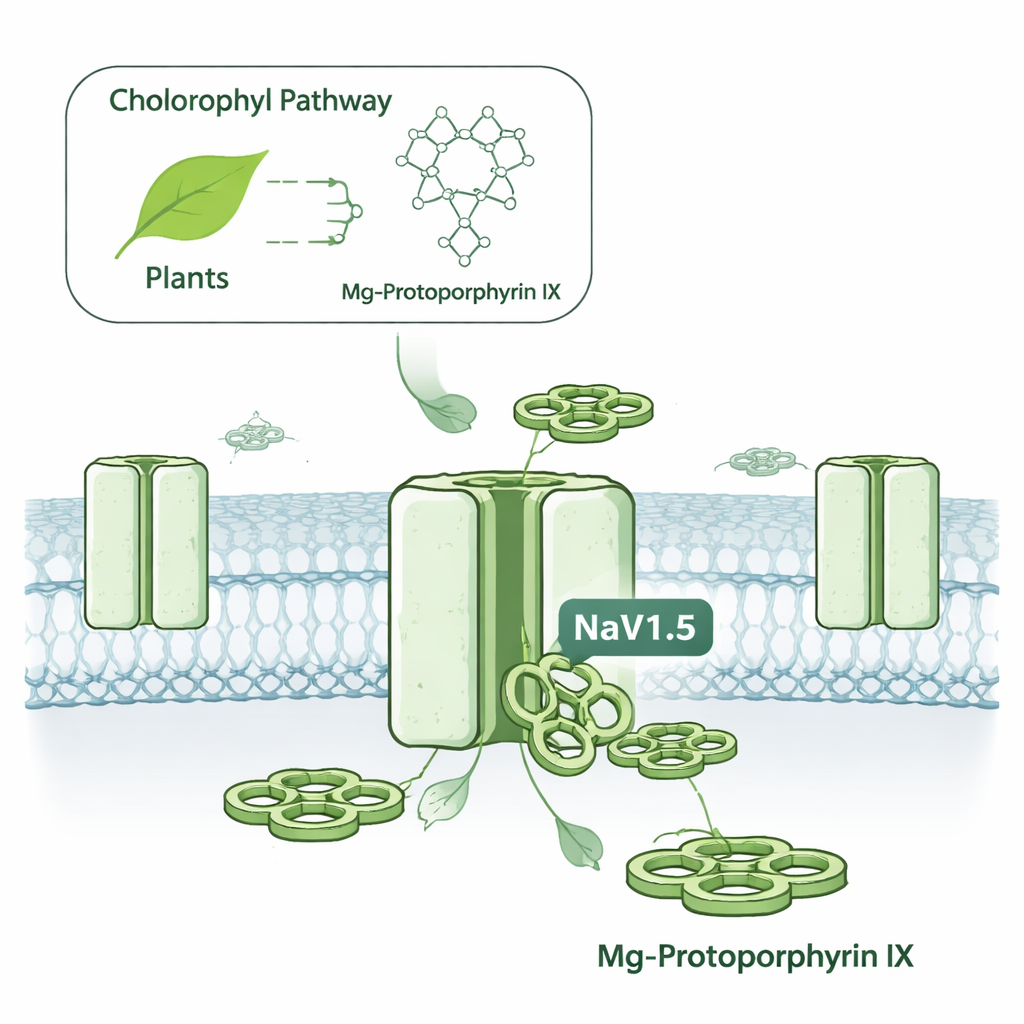
Un interruptor eléctrico oculto en las células cancerosas
Las células usan canales de sodio dependientes de voltaje como pequeñas puertas que se abren y cierran para permitir el paso de partículas cargadas, generando señales eléctricas. NaV1.5 es más conocida por su papel en los latidos cardíacos, donde ayuda a desencadenar cada contracción. Pero el mismo canal también se encuentra en varios cánceres, incluidos tumores de mama y colon, donde su actividad se ha relacionado con un aumento de la movilidad celular y la invasividad. Dirigirse a NaV1.5 ha sido difícil porque la mayoría de los fármacos para canales de sodio también afectan a canales emparentados en los nervios y el músculo esquelético, con el riesgo de efectos secundarios como convulsiones, entumecimiento o debilidad muscular. Los autores se propusieron descubrir si alguna molécula pequeña podía distinguir a NaV1.5 de sus parientes con mucha mayor selectividad.
Un bloqueador inspirado en plantas con precisión récord
El equipo examinó una familia de moléculas en forma de anillo llamadas protoporfirinas metálicas, que recuerdan al núcleo del hemo en la sangre y de la clorofila en las plantas pero contienen distintos átomos metálicos centrales. Cuando aplicaron varias versiones a canales humanos NaV1.5 expresados en células en cultivo, un compuesto destacó: MgPpIX. Redujo la corriente eléctrica a través de NaV1.5 en aproximadamente un 99% a concentraciones nanomolares, unas 100 veces más potente que un análogo con hierro (hemina). Otras versiones metálicas, como las que contienen níquel o cobre, fueron esencialmente inactivas. De forma notable, MgPpIX dejó varios otros tipos de canales de sodio humanos (empleados por el cerebro, los nervios periféricos y el músculo esquelético) completamente sin afectar a las mismas dosis, lo que hace que su selectividad sea de las más agudas jamás reportadas para esta familia de canales.
Cómo la molécula bloquea una pequeña palanca de voltaje
Para entender esta precisión inusual, los investigadores combinaron manipulación genética con simulaciones por ordenador. Los canales de sodio tienen cuatro partes repetidas, cada una con un “sensor de voltaje” que cambia de posición cuando varía el potencial de membrana. Al intercambiar aminoácidos individuales entre NaV1.5 y sus parientes insensibles, el equipo trazó la acción de MgPpIX hasta el sensor de voltaje del segundo dominio, sobre todo dos residuos expuestos hacia el exterior de la célula. Simulaciones de dinámica molecular en un entorno de membrana realista sugirieron que MgPpIX se acomoda junto a este sensor cuando está en su posición de reposo, «hacia abajo». El centro metálico cargado positivamente de MgPpIX es atraído por una cadena lateral cargada negativamente en el canal, mientras que el anillo plano interacciona con los lípidos circundantes. Esta unión parece bloquear el sensor de voltaje en su lugar, impidiendo que se mueva a la conformación activa «hacia arriba» y manteniendo así el canal cerrado. Curiosamente, despolarizaciones fuertes —como las que ocurren durante un latido cardíaco— pueden desalojar temporalmente la molécula, un comportamiento que los autores describen como «dependencia inversa del uso».
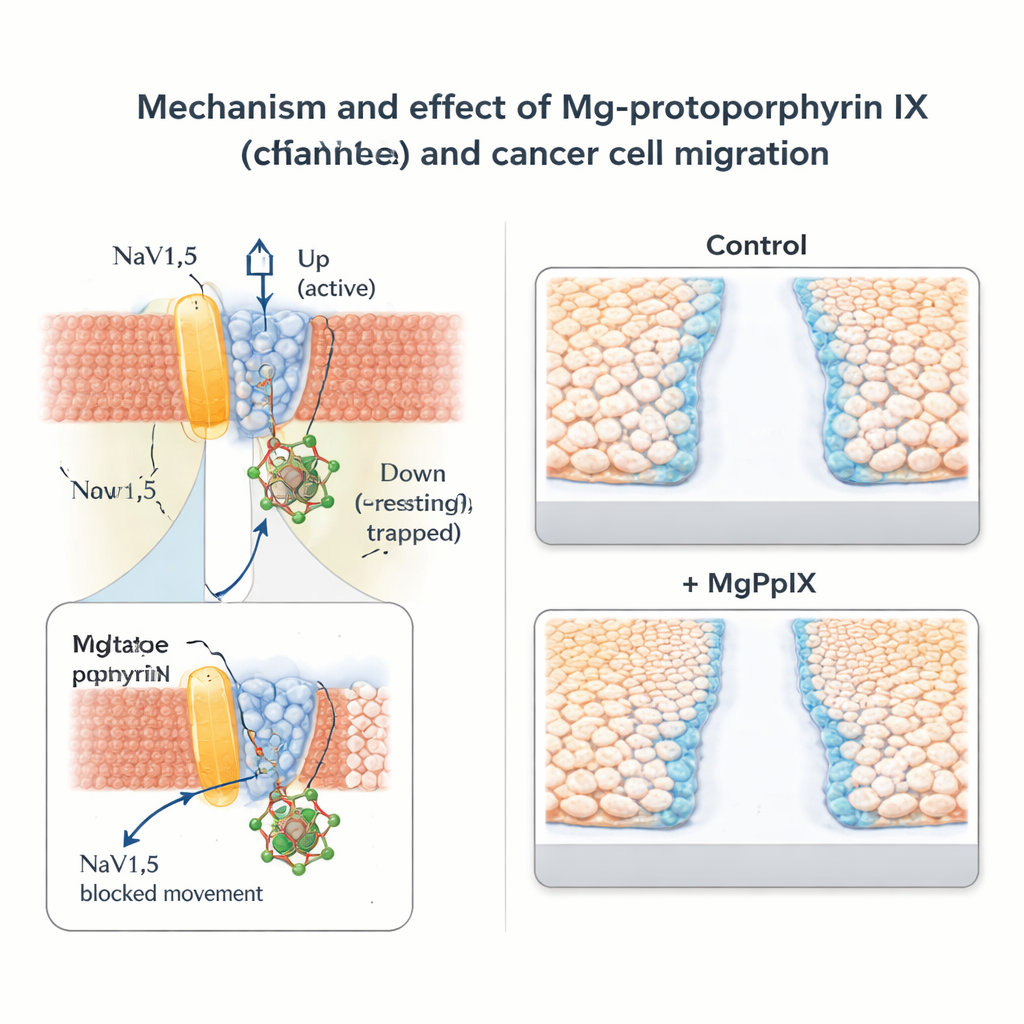
Ralentizar el movimiento de células cancerosas sin bloqueo nervioso general
El equipo exploró luego qué significa este freno molecular para el comportamiento del cáncer. En líneas celulares de cáncer de mama (MDA-MB-231) y cáncer de colon (SW-480) que expresan NaV1.5 de forma natural, MgPpIX redujo drásticamente las corrientes de sodio y ralentizó la migración celular en ensayos estándar de «raspado» y de transwell. Cuanto más bloqueaba un protoporfirina metálica dado a NaV1.5, más obstaculizaba el movimiento celular, reforzando el vínculo entre la actividad del canal y la motilidad. En contraste, líneas celulares cancerosas que carecían de NaV1.5 no mostraron respuesta a MgPpIX ni eléctricamente ni en pruebas de migración, lo que apoya la idea de que el efecto es altamente específico y no tóxico de forma general. Comparado con la toxina clásica de canales de sodio tetrodotoxina, MgPpIX logró una supresión mayor de la migración a concentraciones mucho más bajas.
Promesa y cautela para futuros fármacos anti‑metastásicos
Para un lector no especialista, el mensaje central es que los investigadores han hallado una molécula relacionada con plantas que actúa como una abrazadera de precisión sobre una puerta eléctrica de tipo cardíaco secuestrada por algunos cánceres. Al atrapar la pequeña palanca de voltaje de la puerta en su posición de reposo, MgPpIX puede frenar con fuerza la movilidad de las células cancerosas en el laboratorio mientras preserva otros canales de sodio cruciales para la sensación y el movimiento. Debido a que la rápida actividad eléctrica del corazón puede aliviar parcialmente este bloqueo, podría existir incluso una ventana de seguridad en la que las células tumorales queden más inhibidas que las cardíacas. Si bien MgPpIX en sí puede que no esté listo como medicamento, su sitio y mecanismo de unión únicos proporcionan un plano poderoso para diseñar futuros fármacos dirigidos a detener la propagación del cáncer atacando NaV1.5 con una selectividad sin precedentes.
Cita: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Palabras clave: canales de sodio, Nav1.5, migración de células cancerosas, moléculas derivadas de la clorofila, fármacos dirigidos a canales iónicos