Clear Sky Science · es
El correpresor de receptores nucleares 1 es un posible biomarcador diagnóstico y pronóstico en el carcinoma de células claras de riñón
Por qué una proteína renal importa para los pacientes con cáncer
El carcinoma de células claras renal es la forma más común de cáncer de riñón en adultos, y muchas personas se diagnostican solo después de que la enfermedad ha avanzado de forma silenciosa. Este estudio se centra en una proteína llamada correpresor de receptores nucleares 1 (NCOR1) y plantea una pregunta práctica: ¿podrían los niveles de esta proteína ayudar a los médicos a detectar el cáncer renal antes, predecir cómo evolucionará un paciente y, quizá, orientar tratamientos futuros?
Un protector silencioso dentro de las células renales
NCOR1 actúa normalmente dentro de las células como una especie de freno molecular sobre la actividad génica. Al asociarse con interruptores sensibles a hormonas en el ADN, ayuda a mantener bajo control procesos como el crecimiento celular y el metabolismo. Trabajos previos en otros cánceres sugerían que cuando NCOR1 se pierde o reduce, los tumores se vuelven más agresivos. Dado que el cáncer renal de células claras está fuertemente impulsado por cambios en el control génico, el metabolismo y el sistema inmune, los autores sospecharon que NCOR1 podría ser una pieza importante que falta en esta enfermedad también.
Los niveles de NCOR1 disminuyen en los tumores renales
El equipo recurrió primero a grandes bases de datos públicas sobre cáncer, incluidas The Cancer Genome Atlas y dos conjuntos de datos de expresión génica independientes, y comparó los niveles de NCOR1 en tumores y en tejido normal circundante. A lo largo de 33 tipos de cáncer, NCOR1 fue con frecuencia más bajo en los tumores, y esta caída fue evidente en los cánceres renales. Luego confirmaron el patrón directamente en muestras de tejido de pacientes mediante inmunohistoquímica, una técnica de tinción que muestra dónde se localiza una proteína en las células. En los tumores renales de células claras, NCOR1 era mucho menos abundante que en el riñón normal, donde se encuentra principalmente a lo largo de las membranas celulares. Los pacientes cuyos tumores tenían niveles más bajos de NCOR1 tendían a presentar cánceres más grandes y más avanzados y grados tumorales más altos, características asociadas con peores resultados.
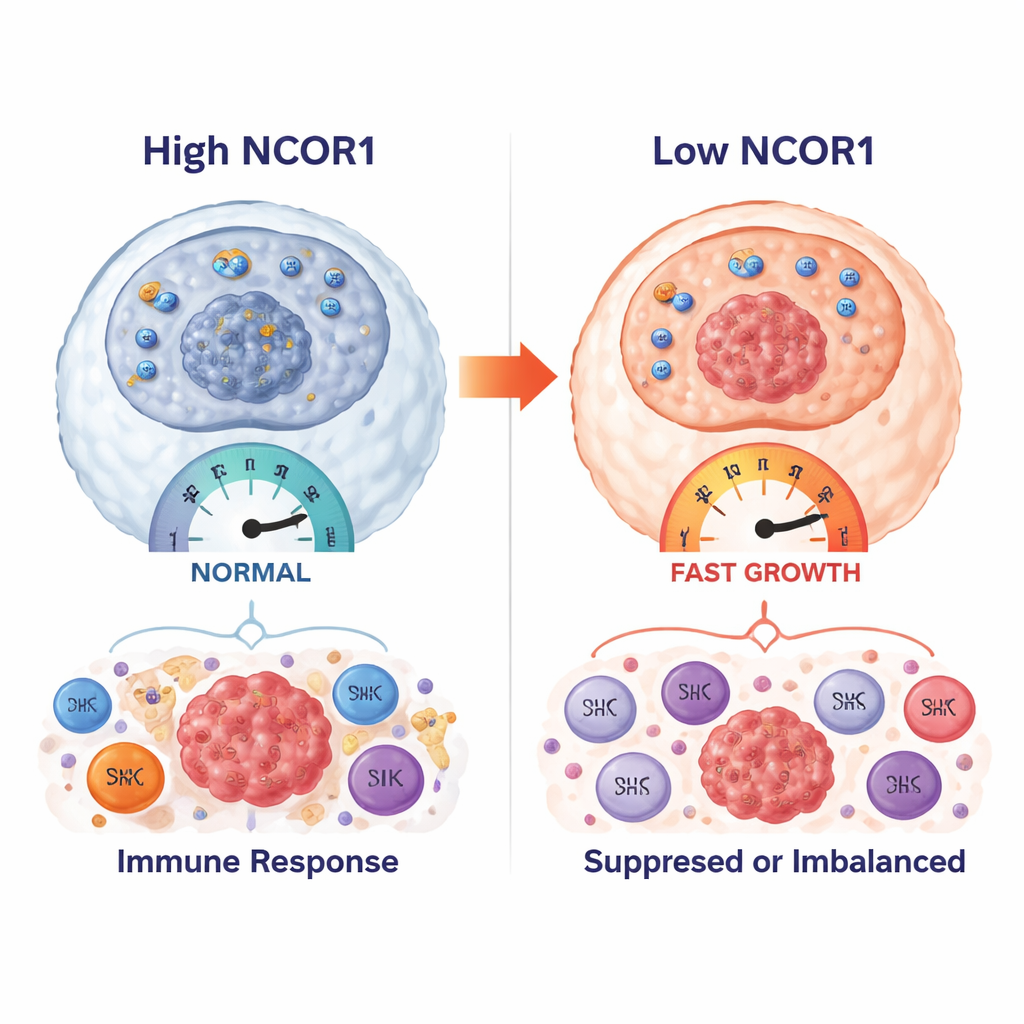
División celular más rápida y un vecindario inmune remodelado
Para entender qué podría estar provocando la baja de NCOR1 dentro de los tumores, los autores compararon los genes que se activaban o desactivaban en pacientes con NCOR1 alto frente a bajo. Los genes que se asociaban con los niveles de NCOR1 estaban fuertemente ligados al ciclo celular —el programa interno que impulsa la división celular. Cuando NCOR1 era bajo, las vías que controlan los puntos de control entre fases de la división celular parecían más activas, consistente con un tumor que progresa más rápido. Al mismo tiempo, los niveles de NCOR1 se relacionaron con qué células inmunitarias estaban presentes en el microambiente tumoral. Una expresión más alta de NCOR1 iba acompañada de una mayor infiltración de varios tipos de células inmunitarias que pueden apoyar respuestas antitumorales, como ciertas poblaciones de células T de memoria, mientras que se observó una relación inversa con células supresoras como las células T reguladoras. Esto sugiere que la pérdida de NCOR1 puede no solo permitir que las células cancerosas se multipliquen con mayor libertad, sino también ayudarles a escapar del ataque inmunitario.
Marcas en el ADN y vínculos con moléculas de control inmunitario
Los investigadores también investigaron por qué NCOR1 está reducido. Encontraron que marcas químicas específicas en el ADN, conocidas como marcas de metilación, en regiones del gen NCOR1 se asociaban con la supervivencia de los pacientes. Una metilación más intensa en varios sitios CpG tendía a ir de la mano con una peor supervivencia global, lo que respalda la idea de que el silenciamiento epigenético de NCOR1 es clínicamente relevante. En contraste, las mutaciones reales en el gen NCOR1 eran raras en los tumores renales y no predecían el resultado. De forma intrigante, la expresión de NCOR1 se correlacionó con los niveles de varios genes clave relacionados con puntos de control inmunitario y con el tumor, incluidos TIGIT, CTLA-4, TP53 y PTEN, lo que sugiere que NCOR1 podría situarse en la intersección del control del crecimiento celular y la regulación inmunitaria. Combinar los niveles de NCOR1 con características clínicas estándar en una carta predictiva, o nomograma, mejoró las estimaciones de supervivencia a 1, 3 y 5 años para los pacientes.
Qué podría significar esto para la atención futura
Para un lector no especializado, el mensaje principal es que NCOR1 se comporta como un guardián protector en el carcinoma de células claras de riñón. Cuando sus niveles bajan —a menudo por silenciamiento químico más que por daño del propio gen—, las células tumorales se dividen más rápidamente, las defensas inmunitarias circundantes se alteran y los pacientes tienden a tener peor pronóstico. Medir NCOR1 en muestras tumorales, y quizá en el futuro en sangre u orina, podría ayudar a los médicos a diagnosticar el cáncer renal con mayor precisión, identificar a pacientes de mayor riesgo que necesitan vigilancia más estrecha o terapias más intensivas, y diseñar nuevos tratamientos que restauren su función de freno o exploten sus vínculos con el sistema inmune. Aunque se necesitan más estudios de laboratorio y clínicos antes de que NCOR1 pueda utilizarse de forma rutinaria, este trabajo lo sitúa como un biomarcador prometedor y un posible diana terapéutica en la atención del cáncer renal.
Cita: Bao, Lr., Gao, Wn., Wang, Xf. et al. Nuclear receptor corepressor 1 is a potential diagnostic and prognostic biomarker in clear cell renal cell carcinoma. Sci Rep 16, 6303 (2026). https://doi.org/10.1038/s41598-026-37486-y
Palabras clave: cáncer renal de células claras, NCOR1, biomarcadores de cáncer, microambiente inmunitario tumoral, metilación del ADN