Clear Sky Science · es
MiniPromoters Ple384 (TH) y Ple388 (PITX3) para dirigir neuronas dopaminérgicas del mesencéfalo en ratones y monos
Por qué esta investigación importa para la salud cerebral
Las células cerebrales que producen dopamina nos ayudan a movernos, aprender a partir de recompensas y mantener la motivación. También son las células que mueren en la enfermedad de Parkinson. Científicos y médicos desean entregar genes útiles o herramientas moleculares específicamente a estas neuronas vulnerables, tanto en animales de laboratorio como, algún día, en personas. Pero dirigir la terapia génica para que se active solo en las células adecuadas, y no en todo el cerebro, ha sido un gran obstáculo. Este estudio describe dos “interruptores” de ADN nuevos y compactos que pueden encender genes casi exclusivamente en las neuronas dopaminérgicas del mesencéfalo de ratones y monos, abriendo el camino a tratamientos más precisos y potencialmente más seguros.
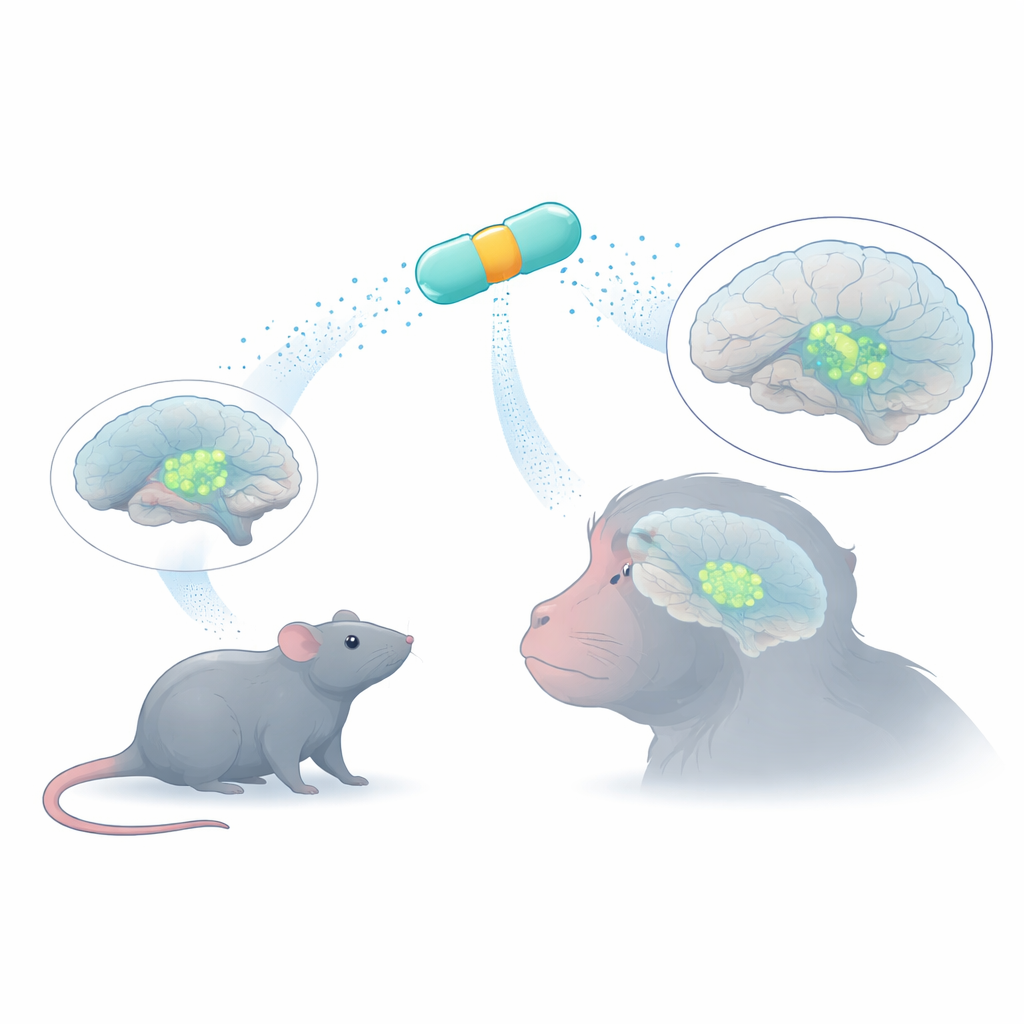
Pequeños interruptores genéticos con una gran tarea
Para introducir un gen terapéutico en las células cerebrales, los investigadores suelen usar virus adenoasociados (AAV), vehículos inofensivos que solo pueden transportar una cantidad limitada de ADN. Dentro de cada virus, una secuencia promotora corta actúa como un interruptor de encendido/apagado, decidiendo dónde ese gen será activo. Muchos promotores naturales son demasiado grandes o poco específicos, activando genes en demasiados tipos celulares. El equipo usó bioinformática para diseñar ocho «MiniPromoters» muy compactos a partir de ADN humano: combinaciones cortas de elementos de control tomados de genes conocidos por marcar neuronas productoras de dopamina. Su objetivo era obtener un conjunto de interruptores que cupieran dentro de AAV y, sin embargo, condujeran una expresión potente y enfocada por tipo celular.
Encontrar los objetivos adecuados en el cerebro del ratón
Los ocho MiniPromoters candidatos se probaron primero en ratones. Cada promotor se colocó en un AAV que llevaba una proteína fluorescente verde, lo que permitió a los científicos ver dónde el interruptor estaba activo. Entregaron los virus ya sea en el torrente sanguíneo o directamente en los espacios llenos de líquido del cerebro. La mayoría de los MiniPromoters no fueron selectivos: algunos iluminaron muchas células no dopaminérgicas, otros funcionaron apenas. Dos destacaron. Uno, llamado Ple384, se construyó a partir de regiones reguladoras del gen de la tirosina hidroximasa, la enzima clave usada por todas las neuronas productoras de catecolaminas. El otro, Ple388, procedía de PITX3, un gen crítico para un subconjunto de neuronas dopaminérgicas del mesencéfalo. Tanto Ple384 como Ple388 produjeron señales brillantes y fuertemente confinadas en la sustancia negra compacta y el área tegmental ventral —los centros mesencefálicos de las neuronas de dopamina— con más del 90 % de las células marcadas presentando también la molécula característica de la dopamina.
De ratones a monos sin perforar profundamente el cerebro
Cualquier terapia génica dirigida a enfermedades humanas debe finalmente funcionar en primates, cuyos cerebros son más grandes y complejos. Inyectar directamente en la sustancia negra es técnicamente exigente y puede dañar esta estructura pequeña y profunda. En su lugar, los investigadores probaron si los mismos MiniPromoters podían administrarse en el líquido cefalorraquídeo de macacos rhesus mediante una única inyección en un ventrículo lateral. Usando una variante de cápside AAV conocida por difundirse ampliamente desde los espacios líquidos, encontraron que tanto Ple384 como Ple388 impulsaron una expresión robusta en las neuronas dopaminérgicas del mesencéfalo en la sustancia negra y el área tegmental ventral, mientras que en gran medida respetaron otras regiones ricas en dopamina como el hipotálamo y el locus coeruleus. La mayoría de las células marcadas en la región objetivo eran neuronas dopaminérgicas, lo que confirma que los interruptores mantuvieron su selectividad entre especies.
Dos herramientas con distintas fortalezas
Aunque ambos MiniPromoters alcanzaron sus objetivos, lo hicieron con patrones diferentes. Ple384, basado en el gen más amplio de la tirosina hidroximasa, iluminó más neuronas en general y cubrió tanto las capas ventral como dorsal de la sustancia negra, así como una porción mayor del área tegmental ventral. Ple388, que refleja el gen PITX3 más restringido, etiquetó principalmente un subconjunto de neuronas del estrato ventral y produjo una fluorescencia más débil. La expresión fuera de objetivo se observó principalmente cerca de los sitios de inyección y en algunos órganos periféricos tras la administración por torrente sanguíneo, pero los controles cuidadosos mostraron que los vectores virales podían alcanzar muchas regiones del cerebro; fueron los MiniPromoters los que limitaron la expresión mayormente a las neuronas dopaminérgicas del mesencéfalo. Esta fuerza ajustable —uno más potente y amplio, otro más selectivo y moderado— permite a los investigadores elegir el interruptor que mejor se adapte a sus necesidades, desde una modulación suave hasta una intervención a gran escala.
Qué significa esto para terapias futuras
Para un público no especializado, el mensaje clave es que los autores han creado dos interruptores genéticos compactos que actúan como interruptores de luz precisos y programables para las neuronas de dopamina en ratones y monos. Ple384 ofrece acceso fuerte y extendido a estas células, mientras que Ple388 se centra en un subconjunto más estrecho y particularmente vulnerable. Debido a que los interruptores son lo bastante pequeños como para caber cómodamente dentro de los vectores virales de uso común, dejan espacio para los genes terapéuticos y pueden ayudar a reducir efectos secundarios al evitar regiones cerebrales no deseadas. A medida que la terapia génica para la enfermedad de Parkinson y afecciones relacionadas avance, tales elementos de control dirigidos serán ingredientes esenciales para tratamientos potentes pero precisos.
Cita: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
Palabras clave: neuronas de dopamina, terapia génica, enfermedad de Parkinson, vectores AAV, promotores específicos de célula