Clear Sky Science · es
Efectos terapéuticos del IGF-2 en NMOSD al inhibir la apoptosis de astrocitos mediante la modulación de la vía de señalización IGF-1R/PI3K/AKT
Protegiendo el cerebro en una enfermedad autoinmune poco conocida
El trastorno del espectro de la neuromielitis óptica, o NMOSD, es una enfermedad autoinmune rara pero devastadora que ataca los nervios ópticos y la médula espinal, dejando a menudo a los pacientes con ceguera, parálisis o problemas cognitivos graves. Los fármacos actuales se centran principalmente en calmar el sistema inmunitario, son costosos y no protegen directamente las células cerebrales del daño. Este estudio explora si una molécula natural relacionada con el crecimiento en la sangre, llamada IGF‑2, podría ayudar a proteger las células del cerebro del daño en NMOSD y ofrecer una nueva vía para tratar la enfermedad.
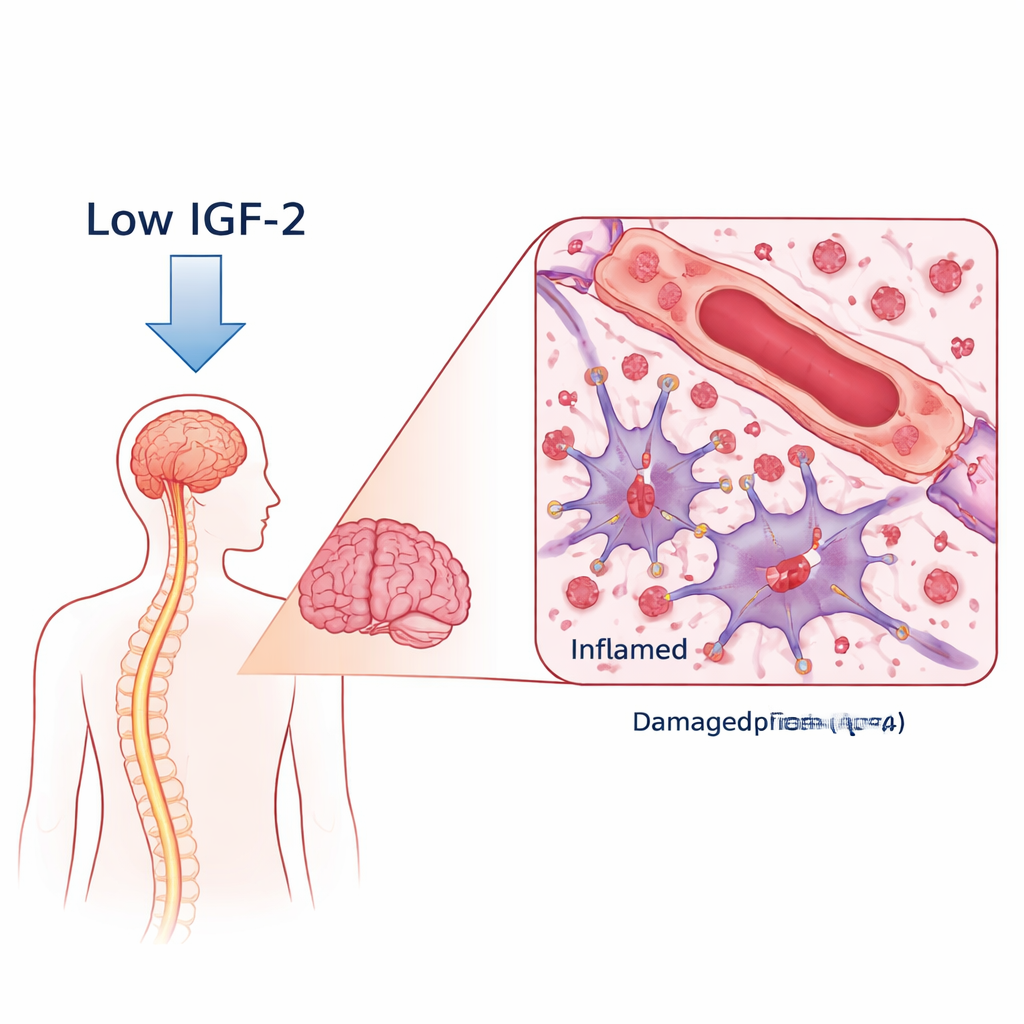
Un anticuerpo dañino y un protector ausente
En la NMOSD, el cuerpo produce anticuerpos contra una proteína canal de agua llamada AQP4, que se encuentra en células de apoyo con forma estrellada en el cerebro llamadas astrocitos. Cuando estos anticuerpos se unen, desencadenan ataques inmunitarios que dañan los astrocitos, desprenden la mielina (el recubrimiento aislante de los nervios) y pueden perjudicar a las neuronas. Los investigadores compararon la sangre de mujeres con NMOSD positivas para anticuerpos contra AQP4 con la de voluntarias sanas. Mediante un análisis proteico amplio, encontraron que los niveles de IGF‑2 eran notablemente más bajos en pacientes con NMOSD, mientras que dos proteínas fijadoras de IGF que pueden atrapar al IGF‑2 estaban elevadas. De forma importante, las pacientes con menor IGF‑2 tendían a presentar mayor discapacidad y peores puntuaciones en pruebas de pensamiento y memoria, vinculando esta molécula con la severidad de la enfermedad y la salud cognitiva.
El tratamiento estándar ayuda a recuperar el IGF-2
Muchas pacientes con NMOSD reciben rituximab, un fármaco que elimina las células B productoras de anticuerpos. El equipo midió las proteínas en sangre antes y después del tratamiento con rituximab. Tras la terapia, los niveles de IGF‑2 aumentaron y las proteínas fijadoras cayeron, acercándose al patrón observado en personas sanas. Esto sugiere que dominar el sistema inmunitario puede permitir al organismo restaurar algunos de sus factores protectores. Aunque rituximab no está diseñado para actuar sobre el IGF‑2, el cambio en esta molécula indica que puede formar parte de la respuesta de recuperación del cuerpo, y que el seguimiento del IGF‑2 podría ayudar a monitorizar la evolución de las pacientes a lo largo del tiempo.
Probando el IGF-2 en una versión murina de la enfermedad
Para comprobar si el IGF‑2 puede hacer más que solo señalar la gravedad de la enfermedad, los científicos recurrieron a un modelo en ratón. Inyectaron anticuerpos humanos contra AQP4 y complemento humano en los cerebros de ratones, lo que reprodujo características clave de la NMOSD: pérdida de AQP4 en astrocitos, inflamación, daño en la mielina y debilidad en las extremidades. Otro grupo de ratones recibió primero un virus inocuo que hacía que sus células cerebrales produjeran IGF‑2 en exceso. Estos ratones con niveles aumentados de IGF‑2 perdieron menos peso, presentaron problemas de movimiento más leves y mostraron menor pérdida de mielina e inflamación en el tejido cerebral y de la médula espinal. El tratamiento estándar con rituximab también fue beneficioso, pero la sobreexpresión de IGF‑2 pareció proteger el tejido cerebral de forma más directa, lo que sugiere un papel neuroprotector en lugar de solo inmunosupresor.
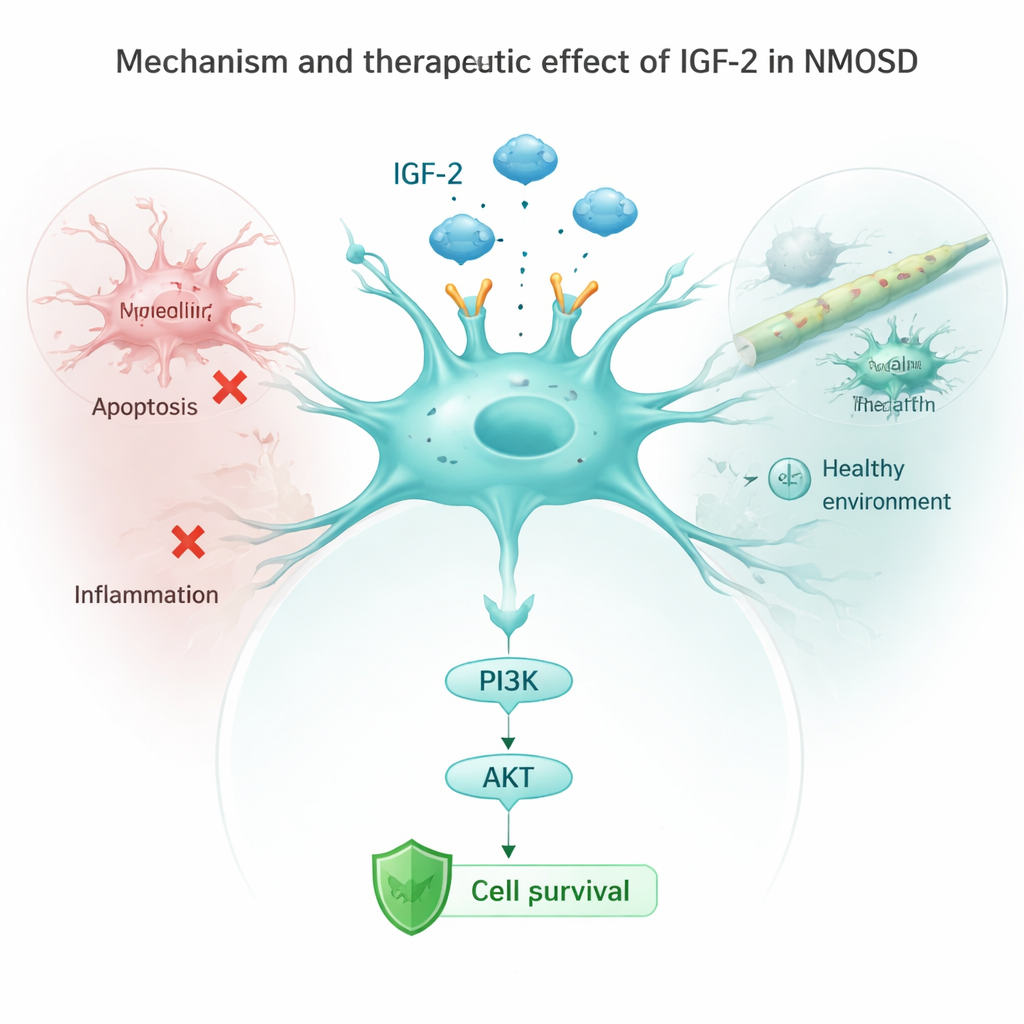
Cómo el IGF-2 atenúa la muerte celular y la inflamación
El equipo examinó luego astrocitos en placas de laboratorio expuestos a anticuerpos de NMOSD. Normalmente, estos anticuerpos reducían los niveles de un receptor clave llamado IGF‑1R y atenuaban una vía de seguridad aguas abajo conocida como PI3K/AKT, mientras activaban proteínas de “autodestrucción” y señales inflamatorias. Cuando los investigadores forzaron a los astrocitos a producir más IGF‑2, esta vía protectora se reactivó, disminuyeron los marcadores de muerte celular y las células liberaron menos moléculas inflamatorias como IL‑1β, IL‑6 y TNF‑α. Bloquear el receptor IGF‑1R borró en parte estos beneficios, mostrando que el IGF‑2 actúa principalmente activando la cadena IGF‑1R/PI3K/AKT dentro de los astrocitos. En ratones vivos, aumentar el IGF‑2 también redujo la activación de la microglía, las centinelas inmunitarias del cerebro, y disminuyó las señales inflamatorias en la sangre.
Qué podría significar esto para los pacientes
En conjunto, estos hallazgos sugieren que el bajo IGF‑2 es tanto un signo de alerta como una oportunidad desaprovechada en la NMOSD. Las pacientes con menos IGF‑2 tienden a estar más discapacitadas y a presentar peor funcionamiento cognitivo, mientras que restaurar o aumentar el IGF‑2 en modelos experimentales ayuda a que los astrocitos sobrevivan, reduce la inflamación cerebral y atenúa el daño neuronal. Aunque este trabajo está en fases iniciales y se basa en un número reducido de pacientes y en estudios en animales, apunta al IGF‑2 como un objetivo prometedor para futuras terapias que no solo mitiguen el ataque inmunitario, sino que también protejan directamente a las células cerebrales vulnerables.
Cita: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Palabras clave: neuromielitis óptica, astrocitos, IGF-2, neuroinflamación, neuroprotección