Clear Sky Science · es
Integración de toxicología de redes, aprendizaje automático y simulaciones de dinámica molecular para revelar los mecanismos duales de la tanshinona IIA en el cáncer de mama triple negativo y la cardiotoxicidad inducida por doxorrubicina
Por qué esta investigación importa para los pacientes
La doxorrubicina es un fármaco fundamental en el tratamiento del cáncer de mama, pero tiene una pega grave: puede dañar el corazón, a veces años después de terminar el tratamiento. Al mismo tiempo, el cáncer de mama triple negativo —una forma difícil de tratar que carece de los blancos hormonales y de factores de crecimiento habituales— sigue necesitando mejores terapias. Este estudio explora si la tanshinona IIA, un compuesto extraído de la hierba tradicional china Salvia miltiorrhiza, podría tanto proteger el corazón frente a la toxicidad de la doxorrubicina como ayudar a atacar tumores mamarios agresivos, lo que potencialmente haría la quimioterapia más segura y eficaz.
Un compuesto, dos grandes problemas
La doxorrubicina ha salvado innumerables vidas, pero sus beneficios se ven limitados por una cardiotoxicidad dependiente de la dosis: por encima de una determinada dosis vitalicia, el riesgo de insuficiencia cardíaca aumenta de forma pronunciada. Los clínicos a menudo afrontan un trade‑off doloroso entre controlar el cáncer y proteger el corazón. Trabajos previos en laboratorio sugerían que la tanshinona IIA puede aumentar las defensas antioxidantes en las células cardíacas y matar directamente células cancerosas, pero las razones moleculares subyacentes seguían poco claras. Los autores se propusieron mapear, de manera sistemática, cómo este único compuesto podría atenuar el daño cardíaco mientras también actúa contra el cáncer de mama triple negativo, construyendo un puente entre la medicina tradicional y la oncología de precisión moderna. 
Minería de grandes datos biológicos para la protección cardíaca
Para entender la protección cardíaca, el equipo recopiló primero miles de genes vinculados a la cardiotoxicidad de varias grandes bases de datos y los combinó con los objetivos proteicos conocidos de la doxorrubicina y de la tanshinona IIA. Surgieron trece dianas «superpuestas»: proteínas asociadas con el daño cardíaco, que interactuaban con la doxorrubicina y que además podrían ser moduladas por la tanshinona IIA. Usando mapas de interacción proteína–proteína, los investigadores redujeron esto a seis protagonistas centrales, incluyendo CCND1 (un regulador del ciclo celular), APAF1 (un iniciador de la muerte celular programada), AR (receptor de andrógenos), TERT (clave para el mantenimiento de los extremos cromosómicos), MMP2 (una enzima de remodelado tisular) y NQO1 (una enzima antioxidante). Docking computacional y simulaciones de dinámica molecular sugirieron que tanto la doxorrubicina como la tanshinona IIA pueden unirse fuertemente a estas proteínas, pero los complejos proteína–tanshinona IIA suelen ser más estables y energéticamente favorables, lo que implica que el compuesto herbal podría redirigir o suavizar las señales dañinas de la doxorrubicina en el corazón.
Descubriendo cómo actúa sobre los tumores agresivos
En la vertiente del cáncer, los investigadores se centraron en conjuntos de datos de expresión génica del cáncer de mama triple negativo. Compararon muestras tumorales con tejido mamario normal para encontrar cientos de genes que estaban anormalmente activados o silenciados. Luego emplearon una técnica llamada análisis de redes de coexpresión génica ponderada para identificar grupos de genes más estrechamente vinculados al fenotipo triple negativo. Al intersectar estos genes cancerosos con las dianas previstas de la tanshinona IIA, destilaron una lista reducida de candidatos y aplicaron tres métodos independientes de aprendizaje automático para ver qué genes distinguían mejor tumor de tejido normal y tenían más probabilidad de ser clínicamente relevantes. La evidencia convergente destacó una diana sobresaliente: EZH2, un gen que ayuda a empaquetar el ADN y que suele estar sobreactivado en cánceres agresivos.
Conectando la biología tumoral y el sistema inmune
Para entender por qué EZH2 importa en pacientes reales, el equipo examinó grandes bases de datos de cáncer. Encontraron que EZH2 está marcadamente más activo en tumores mamarios invasivos que en tejido mamario normal. Aunque su expresión no se correlacionó de manera uniforme con la supervivencia global en todos los casos de cáncer de mama, sí se asoció fuertemente con rasgos del microambiente inmune tumoral. Niveles más altos de EZH2 se correlacionaron con una mayor infiltración de varios tipos de células inmunes —como células B y T— y con una expresión elevada de moléculas que tanto estimulan como suprimen respuestas inmunitarias, incluidos puntos de control inmunitario bien conocidos como CTLA‑4 y LAG‑3. Estos patrones sugieren que EZH2 se sitúa en una encrucijada entre el crecimiento tumoral y el control inmune, y que un fármaco como la tanshinona IIA, al influir sobre EZH2, podría ayudar a remodelar cómo el sistema inmune reconoce y ataca el cáncer de mama triple negativo. 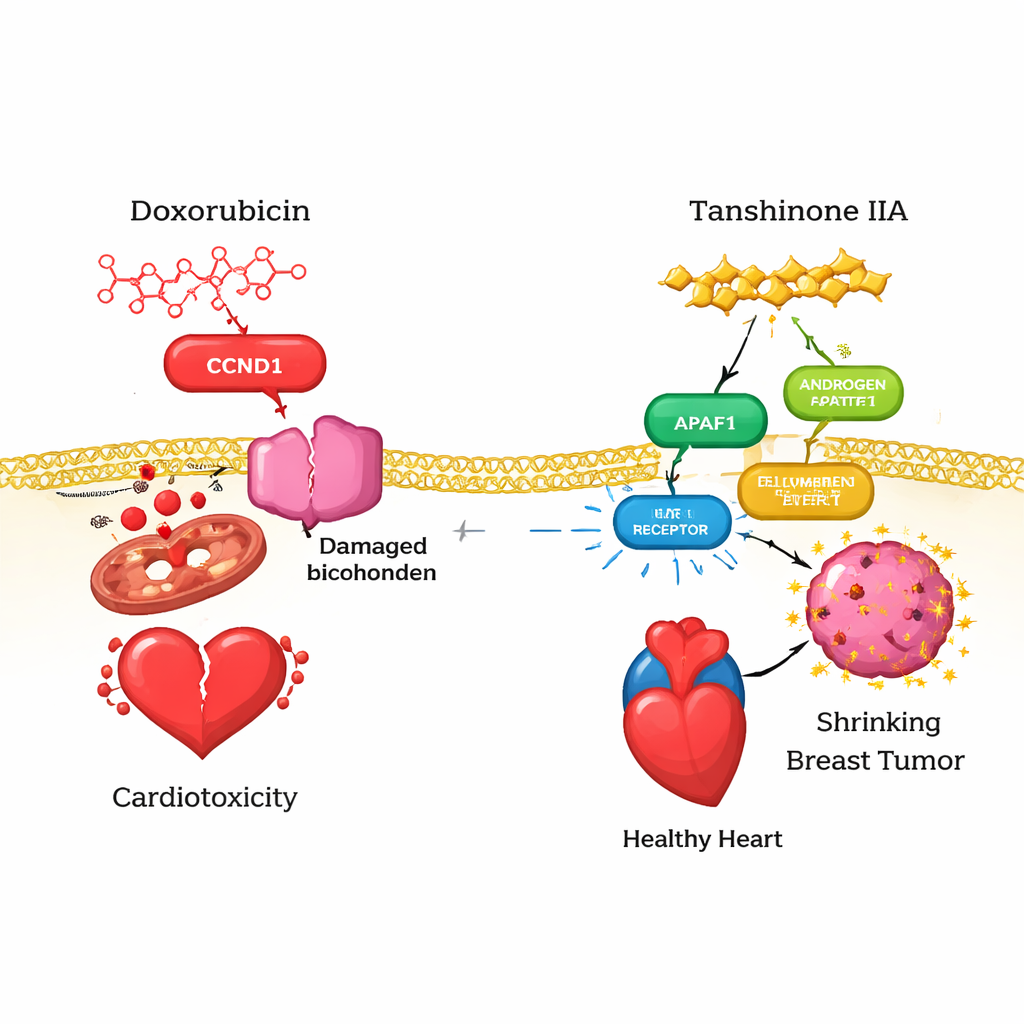
Qué podría significar esto para tratamientos futuros
En términos sencillos, este trabajo propone que la tanshinona IIA podría desempeñar un papel dual en el cuidado del cáncer de mama: actuar como una especie de «escudo químico» que reduce el daño cardíaco relacionado con la doxorrubicina al estabilizar proteínas clave protectoras del corazón, y a la vez servir como un arma dirigida contra el cáncer de mama triple negativo mediante su acción sobre EZH2 y las vías inmunitarias relacionadas. Los hallazgos se basan en análisis computacionales y estadísticos más que en ensayos en animales o humanos, por lo que son un plan de trabajo inicial más que una terapia lista para usar. Aun así, ofrecen una hoja de ruta molecular detallada para diseñar tratamientos combinados que preserven el poder salvador de la doxorrubicina mientras reducen sus riesgos a largo plazo —y para traducir un componente herbal tradicional en un complemento oncológico moderno guiado por mecanismos.
Cita: Wu, B., Lan, Xh., Chen, Xq. et al. Integrating network toxicology, machine learning, and molecular dynamics simulations to reveal tanshinone iia’s dual mechanisms in TNBC and doxorubicin-induced cardiotoxicity. Sci Rep 16, 6861 (2026). https://doi.org/10.1038/s41598-026-37428-8
Palabras clave: tanshinona IIA, cardiotoxicidad por doxorrubicina, cáncer de mama triple negativo, EZH2, farmacología de redes