Clear Sky Science · es
Evaluación metabolómica revela agotamiento de aminoácidos y metabolitos energéticos en el músculo esquelético tras lesión renal aguda isquémica en ratones
Por qué los riñones dañados pueden agotar tu fuerza
Las personas con insuficiencia renal súbita a menudo notan algo que parece no tener relación con la orina o las pruebas de sangre: sus músculos se sienten débiles y la recuperación es lenta. Este estudio plantea una pregunta sencilla pero importante: cuando los riñones se lesionan de forma repentina, ¿qué sucede exactamente dentro de los combustibles y bloques constructores del músculo? Mediante una encuesta química detallada del músculo de ratones, los investigadores muestran que la lesión renal aguda desencadena una pérdida de nutrientes clave y moléculas energéticas a nivel corporal, dejando el músculo esquelético en un estado empobrecido y con escasa energía.
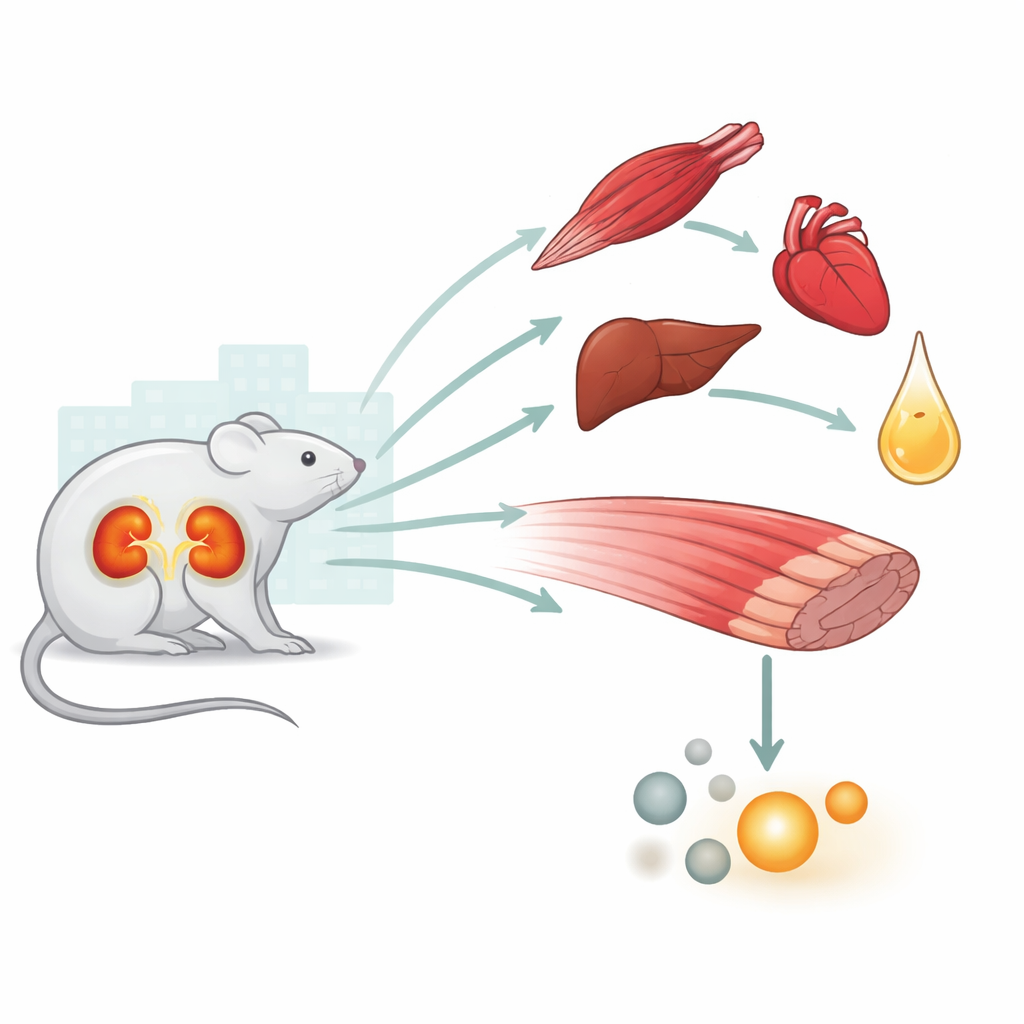
Una crisis de todo el organismo, no solo un problema renal
La lesión renal aguda (LRA) es frecuente en pacientes hospitalizados y críticos y se asocia fuertemente con mayor riesgo de muerte. Los médicos llevan tiempo observando que la LRA se comporta como un estado de estrés generalizado, que afecta al corazón, los pulmones, el hígado, el cerebro y los músculos. Trabajos anteriores de este grupo mostraron que tras la pérdida temporal del flujo sanguíneo a los riñones en ratones, el corazón, el hígado, los pulmones y los propios riñones presentaban signos químicos de baja energía y estrés oxidativo. Partiendo de eso, el estudio actual se centra en el músculo esquelético, un gran reservorio de carbohidratos y aminoácidos que el cuerpo puede utilizar durante estrés severo.
Cómo se hizo el estudio en ratones
Los investigadores indujeron LRA por isquemia en ratones jóvenes adultos macho mediante la compresión breve del suministro sanguíneo a ambos riñones, seguido de la restauración del flujo. Compararon estos animales con ratones sometidos a cirugía simulada (sham) y con controles no operados. A las 24 y 72 horas, recogieron un músculo clave de la pierna (el gastrocnemio) y emplearon un enfoque metabolómico no dirigido—un escaneo químico ultrasensible—para medir 175 moléculas pequeñas, incluidas aminoácidos, antioxidantes y compuestos relacionados con la energía. Se usaron métodos estadísticos y de reconocimiento de patrones para determinar qué moléculas cambiaron más y cómo difería la química muscular entre los grupos.
Combustible muscular y antioxidantes disminuyen
Los cambios más llamativos aparecieron a las 24 horas tras la lesión renal. Aproximadamente dos quintas partes de todos los metabolitos detectados se alteraron, y el patrón global fue claro: muchos compuestos clave en el músculo estaban disminuidos en comparación con la cirugía simulada. Aminoácidos esenciales y no esenciales como alanina, valina, lisina, metionina y tirosina descendieron, al igual que varias moléculas del ciclo de la urea (arginina, citrulina, ornitina, argininosuccinato) que ayudan a manejar los desechos de nitrógeno y apoyan la producción de creatina. El principal antioxidante celular, el glutatión, y sus bloques constructores (incluyendo metionina y un dipéptido cisteína‑glicina) también se redujeron, lo que apunta a un aumento del estrés oxidativo. Las moléculas relacionadas con la energía, incluida la creatina y los intermedios de vías energéticas centrales, también tendieron a disminuir, lo que sugiere que el músculo estaba sacrificando sus propias reservas para apoyar al resto del organismo.
Conectando el músculo con otros órganos
Para ver el panorama general, el equipo comparó los datos musculares con perfiles metabolómicos previamente recogidos del riñón, el hígado, el corazón y el plasma sanguíneo en el mismo punto temporal de 24 horas. En todos estos tejidos se repitieron ciertos temas: agotamiento generalizado de glutatión y sus precursores, descenso de la alanina y alteración consistente de la química relacionada con la arginina y el ciclo de la urea. Al mismo tiempo, algunos productos de degradación, como la alantoína (un marcador de estrés oxidativo), aumentaron en múltiples órganos y en la sangre. La creatina y su forma de alta energía, la fosfocreatina, estaban relativamente aumentadas en hígado, riñón y sangre, aun cuando la arginina y los aminoácidos caían en músculo y plasma, lo que sugiere que el músculo esquelético podría estar exportando sustratos para que otros órganos—y en especial los riñones lesionados—puedan seguir generando energía bajo presión.
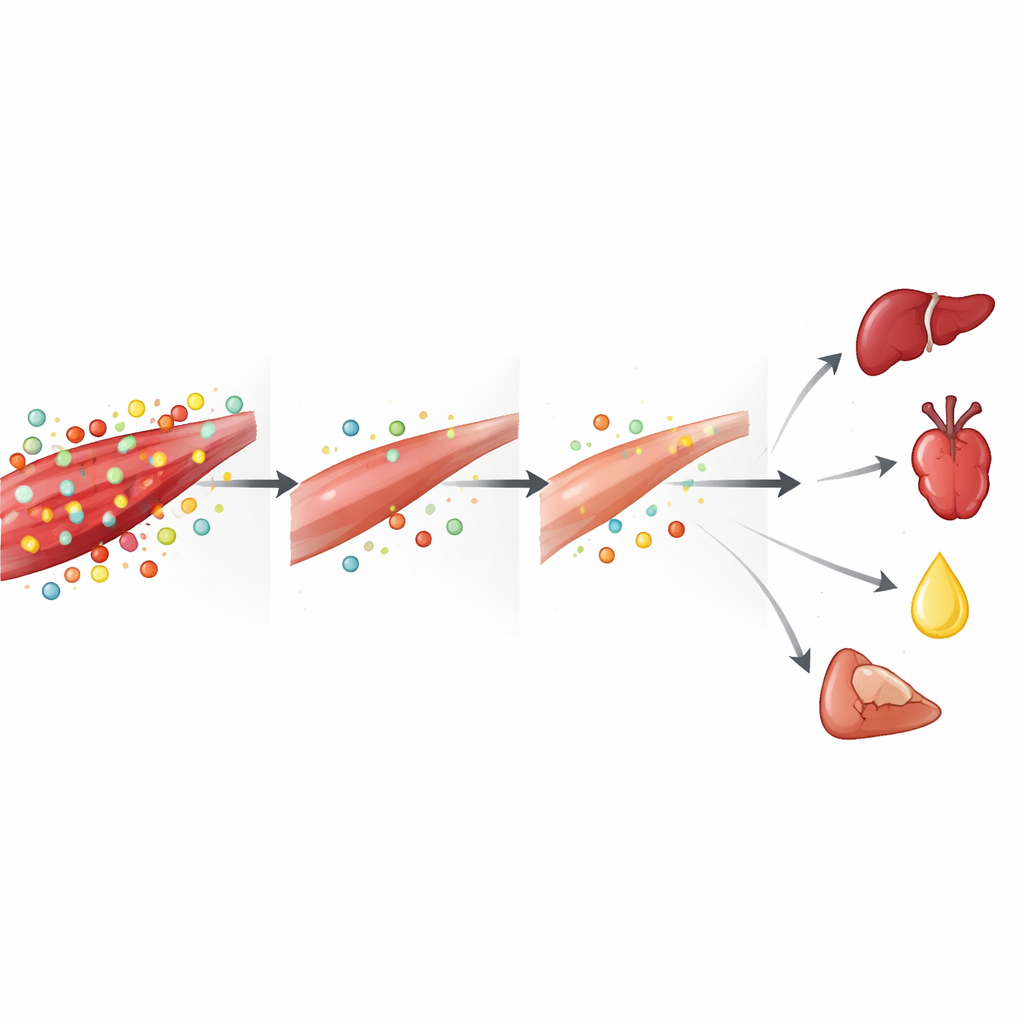
Qué significa esto para los pacientes y terapias futuras
En términos cotidianos, el estudio describe la LRA como un evento metabólico de “retirada de efectivo” para el cuerpo: el músculo esquelético descompone sus reservas de proteína y antioxidantes para ayudar a alimentar y proteger órganos vitales, dejando a los propios músculos con escasez de combustible y defensa. Esto ayuda a explicar por qué las personas con lesión renal grave son propensas a la pérdida muscular, la debilidad y una pobre recuperación funcional. También plantea la posibilidad de que un soporte nutricional cuidadosamente dirigido—particularmente aminoácidos y compuestos que refuercen los sistemas de glutatión y creatina‑fosfocreatina—podría algún día ayudar a proteger tanto a los riñones como a los músculos durante una enfermedad aguda. Aunque estos hallazgos provienen de ratones y se basan en instantáneas químicas en lugar de trazados directos de flujos, ofrecen un mapa detallado de cómo la química muscular se ve perturbada por la lesión renal y apuntan a nuevas estrategias para preservar la fuerza y mejorar los resultados cuando los riñones fallan de forma súbita.
Cita: Li, A.S., Baker, P.R., Park, S. et al. Metabolomic assessment reveals depletion of amino acids and energy metabolites in skeletal muscle after ischemic acute kidney injury in mice. Sci Rep 16, 8823 (2026). https://doi.org/10.1038/s41598-026-37424-y
Palabras clave: lesión renal aguda, metabolismo del músculo esquelético, agotamiento de aminoácidos, estrés oxidativo, metabolómica