Clear Sky Science · es
Análisis de la función cardíaca sistólica en ratones con eliminación de PERM1 usando grandes cohortes de animales
Por qué importan a la salud humana los diminutos corazones de ratón
La insuficiencia cardiaca suele describirse como una bomba cansada, pero lo que realmente debilita un corazón es sorprendentemente complejo. En este estudio, los científicos usaron un grupo inusualmente grande de ratones para plantear una pregunta concreta: ¿apagar un único gen llamado PERM1, conocido por ayudar a las células cardiacas a generar energía, también cambia la fuerza con que el corazón se contrae? Al escanear cuidadosamente los corazones de más de 170 ratones, muestran que este gen remodela sutilmente el corazón y reduce su potencia de bombeo, mientras que los animales en gran medida siguen pareciendo sanos desde el exterior. Sus hallazgos ayudan a zanjar un debate en el campo y ofrecen una hoja de ruta para diseñar mejores experimentos cardíacos en el futuro.
Un gen que enlaza el uso de combustible con la contracción cardíaca
PERM1 se identificó por primera vez como un interruptor que aumenta la producción de energía en las células musculares, incluido el corazón. Trabajos previos mostraron que los niveles de PERM1 disminuyen en corazones en insuficiencia tanto en ratones como en humanos, lo que planteó la posibilidad de que niveles bajos de PERM1 puedan contribuir realmente a latidos más débiles. Pero los estudios con ratones sin PERM1 —animales diseñados genéticamente para carecer del gen— habían dado respuestas contradictorias sobre si sus corazones bombeaban menos eficazmente. Dado que PERM1 se contempla como posible diana para nuevas terapias de insuficiencia cardiaca, los autores se propusieron probar su impacto en la función cardíaca con suficientes animales y estadísticas rigurosas para obtener una respuesta clara de sí o no.
Una mirada de números grandes a corazones pequeños
El equipo reunió datos de ecocardiogramas —la misma técnica de ultrasonido usada en clínicas de cardiología— de cada ratón sin PERM1 y de su compañero de camada sano utilizado en su laboratorio durante un período de 18 meses. Esta revisión retrospectiva produjo 84 animales normales (tipo salvaje) y 88 knockout, un tamaño de muestra mucho mayor del habitual en estudios cardíacos en ratón. A partir de las imágenes de ultrasonido midieron indicadores estándar de cómo funciona el ventrículo izquierdo, la principal cámara de bombeo. El número clave fue la fracción de eyección, el porcentaje de sangre expulsado en cada latido, junto con medidas relacionadas como cuánto disminuye el diámetro ventricular al contraerse, qué grosor tienen las paredes y la cantidad total de sangre bombeada por minuto.
Contracción más débil, cámara más grande, rendimiento similar
Los resultados muestran un patrón consistente. En promedio, la fracción de eyección cayó de alrededor del 65% en ratones normales a un 54% en los knockout de PERM1, una diferencia lo bastante grande como para tener relevancia clínica en pacientes humanos y respaldada por estadísticas muy sólidas. Otras medidas de contracción, como el acortamiento fraccional y el engrosamiento de la pared, también disminuyeron. Al mismo tiempo, los ventrículos izquierdos de los knockout eran visiblemente más grandes, especialmente al final de la contracción, lo que indica que quedó más sangre retenida en la cámara. A pesar de esta contracción más débil, la cantidad total de sangre bombeada por minuto solo cayó ligeramente —aproximadamente un 6%— porque las cámaras agrandadas podían contener más volumen inicialmente. En otras palabras, el corazón compensó en parte la mala contracción estirando su cámara principal.
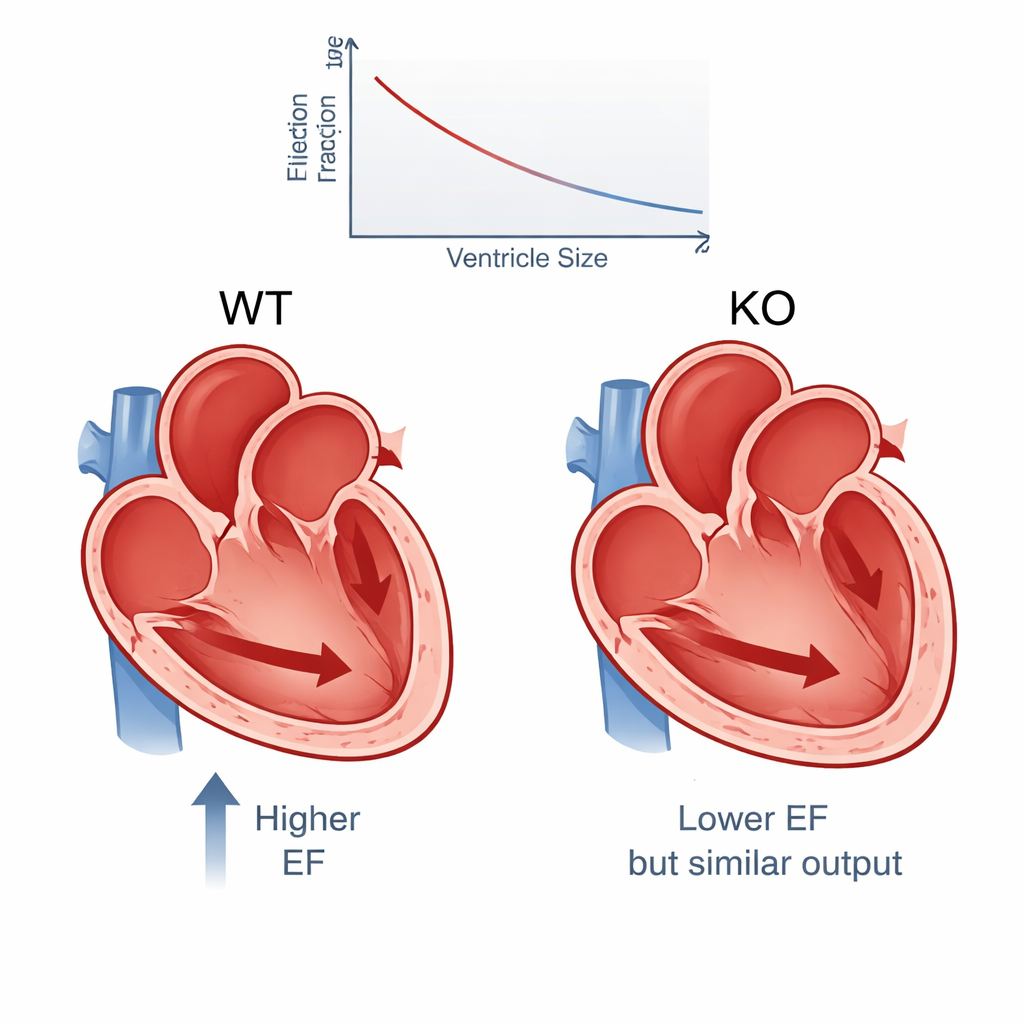
Diversidad oculta en corazones “idénticos”
Debido a que el estudio incluyó tantos animales, los investigadores pudieron mirar más allá de los promedios y estudiar cómo variaban los corazones individuales. Incluso entre ratones sanos genéticamente idénticos, observaron una dispersión sorprendentemente amplia en la fracción de eyección. La eliminación de PERM1 desplazó toda la distribución hacia abajo —más corazones con menor fuerza de bombeo— pero no amplió la propia dispersión. Cerca del 7% de los ratones knockout tenían fracciones de eyección por debajo del 40%, un nivel que en humanos calificaría como insuficiencia cardiaca con fracción de eyección reducida, sin embargo estos ratones todavía mantenían un gasto cardíaco casi normal. Los análisis estadísticos mostraron que el sexo, la edad y el peso corporal explicaban solo una pequeña porción de la variabilidad; la mayoría de las diferencias probablemente provengan de factores biológicos más difíciles de medir, como influencias ambientales sutiles o cambios epigenéticos.
Qué significa esto para la investigación cardíaca futura
Para ayudar a otros científicos a diseñar mejores experimentos, los autores usaron su gran conjunto de datos para calcular cuántos animales se necesitan normalmente para detectar cambios significativos en cada parámetro cardíaco. Encontraron que los tamaños de grupo modestos que suelen emplearse en el campo pueden fácilmente pasar por alto efectos reales pero moderados, sobre todo para medidas sutiles como el volumen sistólico o el gasto cardíaco. En conjunto, el estudio aporta argumentos sólidos de que la pérdida de PERM1 provoca una remodelación específica del corazón —cámaras más grandes, contracción más débil— en lugar de un fallo absoluto, y que esta remodelación se compensa en parte mediante cambios estructurales que ayudan a preservar el flujo sanguíneo. Para el público no especializado, la conclusión es que un único gen regulador de la energía puede empujar al corazón hacia un nuevo modo de funcionamiento, uno que parece sano desde fuera pero que alberga cambios más discretos en la estructura de la bomba y en la fuerza con que trabaja.
Cita: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Palabras clave: insuficiencia cardiaca, contractilidad cardíaca, energética mitocondrial, modelos murinos, ecocardiografía