Clear Sky Science · es
Identificación y caracterización de biomarcadores relacionados con fibroblastos y subpoblaciones proinflamatorias en la periodontitis mediante análisis integrado transcriptómico y de una sola célula
Por qué tus encías importan más allá de la sonrisa
Encías que sangran y dientes flojos pueden parecer problemas menores, pero la enfermedad crónica de las encías—conocida como periodontitis—puede dañar el hueso mandibular, provocar pérdida dental y está relacionada con afecciones como enfermedades cardíacas y diabetes. Este estudio examina de cerca a un grupo de células en las encías que suele pasarse por alto, llamadas fibroblastos, para entender cómo contribuyen a promover o frenar la inflamación. Al combinar grandes conjuntos de datos genómicos con análisis unicelular, los investigadores descubren nuevas señales de alarma y tipos celulares que podrían mejorar cómo los dentistas diagnostican y tratan la enfermedad periodontal.
Actores ocultos en las encías doloridas
Los fibroblastos son las células trabajadoras que construyen y mantienen el tejido conectivo que mantiene los dientes en su lugar. Durante años se les consideró principalmente como un “andamiaje” estructural. Esta investigación muestra que son mucho más: los fibroblastos pueden actuar como pequeños centros de control de la inflamación. Cuando las bacterias alteran el equilibrio normal de la microbiota oral, los fibroblastos responden liberando mensajeros químicos que atraen células inmunitarias y que pueden ayudar a reparar el tejido o intensificar el daño. Los autores se centraron en identificar señales génicas relacionadas con fibroblastos que difieren entre encías sanas y periodontitis, y en detectar subgrupos de fibroblastos que se vuelven especialmente inflamatorios en tejido enfermo.
Escaneando el tejido gingival célula por célula
Para lograrlo, el equipo analizó varios grandes conjuntos de datos de expresión génica de pacientes con encías sanas y con periodontitis, junto con un conjunto de datos moderno de secuenciación unicelular que perfila miles de células individuales. Primero mapearon los principales tipos celulares del tejido gingival—como células inmunitarias, células vasculares y fibroblastos—y confirmaron que la cantidad y la actividad de fibroblastos era mayor en encías enfermas. Luego buscaron genes que estuvieran alterados en la periodontitis y que estuvieran específicamente vinculados a los fibroblastos. Usando un método estadístico que reduce las características a las más informativas, identificaron seis genes clave relacionados con fibroblastos cuyo patrón combinado de actividad distinguía con fiabilidad la periodontitis de la salud en múltiples grupos de pacientes.
Patrones de riesgo y “personalidades” inmunitarias de la enfermedad gingival
Con estos seis genes, los investigadores construyeron un modelo diagnóstico que funcionó bien para separar muestras enfermas de sanas, y lo tradujeron en un gráfico de puntuación sencillo—llamado nomograma—que, en principio, podría estimar el riesgo individual. Al agrupar a los pacientes según la intensidad de expresión de estos genes fibroblásticos surgieron tres formas distintas de periodontitis. Una forma mostró un paisaje inmunitario altamente inflamatorio, repleto de linfocitos T agresivos y macrófagos en “modo ataque”. Una segunda forma estuvo dominada por células que amortiguan las respuestas inmunitarias, sugiriendo un entorno más suprimido. Una tercera forma quedó en un punto intermedio, con una mezcla más equilibrada o en reposo de células inmunitarias. Estos patrones sugieren que no toda la enfermedad periodontal es la misma y que los fibroblastos contribuyen a moldear estas diferentes “personalidades” de la inflamación.
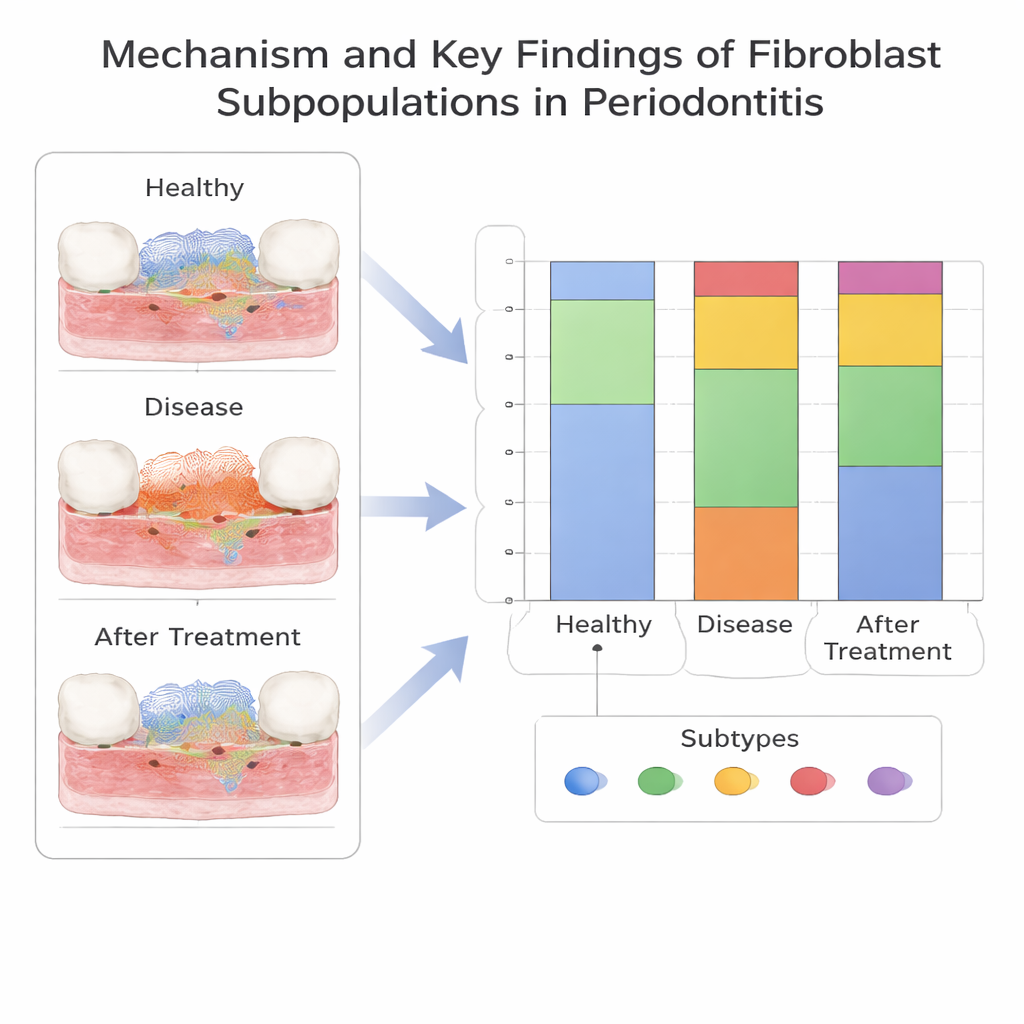
Un nuevo subtipo de fibroblasto proinflamatorio
Profundizando a nivel unicelular, el equipo dividió los fibroblastos en cinco subtipos según su actividad génica. Un subtipo, marcado por un gen llamado CXCL13, destacó porque era mucho más común en la periodontitis que en las encías sanas. Este grupo de fibroblastos CXCL13-positivos apareció temprano a lo largo de una trayectoria de desarrollo y se asoció con señales que atraen células inmunitarias y remodelan la matriz tisular—características coherentes con un fuerte papel proinflamatorio. En contraste, otro subtipo de fibroblasto se enriqueció en tejido sano y podría ayudar a mantener la estabilidad del entorno gingival. Los autores confirmaron en muestras de pacientes que ciertos genes relacionados con fibroblastos, especialmente SELL, y los propios fibroblastos CXCL13-positivos, eran efectivamente más altos en encías enfermas, reforzando los hallazgos computacionales.
Qué significa esto para el cuidado futuro de las encías
En términos sencillos, el estudio revela que algunos fibroblastos en tus encías actúan como aceleradores de la inflamación, mientras que otros pueden comportarse más como frenos o equipos de reparación. Al identificar marcadores génicos precisos y un subtipo proinflamatorio distinto de fibroblastos, el trabajo abre la puerta a pruebas más exactas que detecten la periodontitis antes y con mayor fiabilidad. También sugiere que tratamientos futuros podrían dirigirse a estas vías específicas impulsadas por fibroblastos—suprimir subconjuntos dañinos como los fibroblastos CXCL13-positivos o potenciar los protectores—para controlar la inflamación gingival de forma más eficaz y, posiblemente, reducir su impacto en la salud general.
Cita: Huang, M., Lin, Y., Wu, Z. et al. Identification and characterization of fibroblast-related biomarkers and pro-inflammatory subpopulations in periodontitis by integrated transcriptomic and single-cell analysis. Sci Rep 16, 6223 (2026). https://doi.org/10.1038/s41598-026-37385-2
Palabras clave: periodontitis, fibroblastos, inflamación gingival, secuenciación de ARN unicelular, biomarcadores