Clear Sky Science · es
Modelos generalizados de vasos sanguíneos para oncología basada en nanopartículas magnéticas: propiedades geométricas y microfluídicas
Guiando pequeños imanes a través del cuerpo
Imagínese poder atraer fármacos contra el cáncer directamente hacia un tumor usando un imán, preservando el resto del organismo de efectos secundarios intensos. Este estudio explora cómo viajan partículas magnéticas diminutas a través de redes que imitan vasos sanguíneos y plantea una pregunta aparentemente sencilla: en condiciones de flujo realistas, ¿pueden los imanes realmente dirigir estas partículas hacia donde los médicos quieren que vayan?
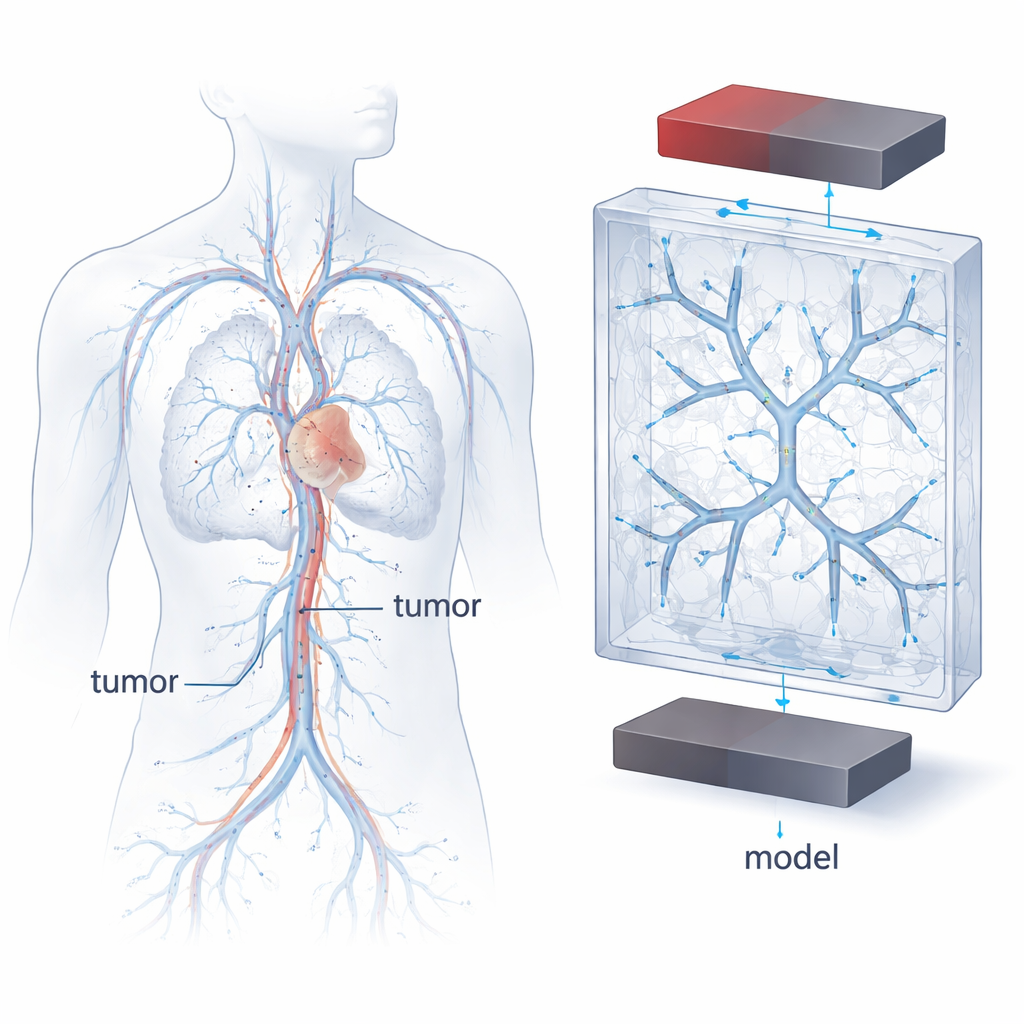
Por qué importan la geometría del vaso y el flujo
Las terapias magnéticas contra el cáncer se basan en nanopartículas de óxido de hierro superparamagnéticas (SPIONs) que pueden ser atraídas por un campo magnético mientras transportan fármacos por el torrente sanguíneo. Pero los vasos sanguíneos no son tubos rectos y sencillos: se ramifican, se estrechan, curvan y dividen, y la sangre acelera o se ralentiza en respuesta. Estos cambios de forma y velocidad afectan cómo se mueven las partículas, dónde se concentran y si contactan las paredes del vaso el tiempo suficiente para adherirse. Los vasos sanguíneos reales de los pacientes son extremadamente variables, lo que dificulta comparar experimentos o predecir el comportamiento de una nueva terapia. Por ello, los autores se propusieron construir una “vasculatura modelo” altamente controlada y repetible que aun así capture las características esenciales de los vasos que alimentan los tumores.
Construyendo redes vasculares tumorales idealizadas
Para diseñar estos vasos modelo, el equipo se basó en reglas clásicas que describen cómo se ramifican las arterias reales. Una de esas reglas, la ley de Murray, relaciona los diámetros de los vasos progenitores y sus ramas de forma eficiente en términos energéticos. Usando medidas clínicas de tumores de mama y estas leyes de escala, los investigadores generaron matemáticamente árboles ramificados que imitan cómo los vasos que alimentan tumores se estrechan hasta llegar a la red capilar. Luego emplearon impresión 3D de alta resolución para incrustar redes de canales huecos con dos, tres o cuatro niveles de ramificación dentro de bloques de plástico transparente. Los canales seguían un patrón de ramificación simétrico y se extendían en tres dimensiones, ofreciendo un paisaje simplificado pero inspirado fisiológicamente para estudiar el movimiento de las partículas.
Observando partículas magnéticas en acción
A través de estas redes impresas, el equipo bombeó agua como sustituto de la sangre, inyectó después un fluido que contenía SPIONs aguas arriba y aplicó un campo magnético estático alrededor del modelo. Imágenes de alta velocidad proporcionaron un registro casi cinematográfico de cómo las nubes oscuras de partículas cruzaban distintas ramas, mientras que el análisis por computadora convirtió los cambios de brillo en señales temporales que reflejaban la presencia local de partículas. Al variar la velocidad de flujo de fondo, la concentración de partículas, la complejidad de las ramificaciones y la presencia o ausencia del imán, los investigadores pudieron desentrañar cómo cada factor moldeaba la distribución de partículas, el tiempo de residencia y la deposición eventual en las paredes de los canales.
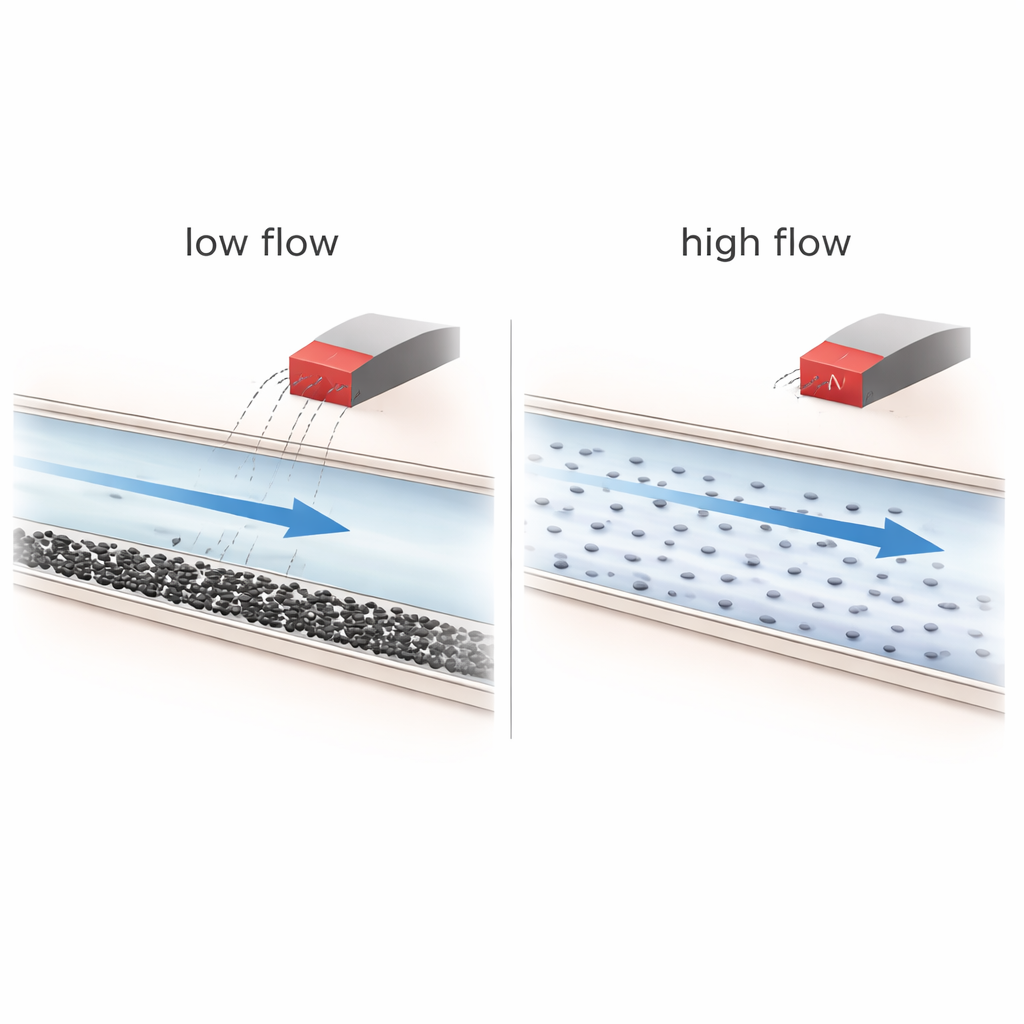
Cuando los imanes ayudan—y cuando no
Los experimentos revelan que las condiciones de flujo dominan la historia. A mayores velocidades de flujo, el fluido se mezcla bien y las nanopartículas viajan rápidamente; en estas condiciones, el campo magnético tiene casi ninguna influencia y las partículas simplemente siguen las líneas de corriente a través de la red. Sin embargo, a bajas velocidades de flujo, la gravedad y los efectos de concentración hacen que las partículas se asienten hacia el fondo de los canales, formando capas estratificadas y a veces agregados sueltos. En esta situación ya desigual, el imán puede empujar más partículas hacia ciertas ramas y prolongar ligeramente su tiempo de residencia, particularmente en redes más complejas y altamente ramificadas. No obstante, los cálculos muestran que la fuerza magnética sobre una sola partícula de 40 nanómetros es muchos órdenes de magnitud más débil que la fuerza viscosa del líquido en movimiento, lo que hace físicamente poco realista el «direccionamiento de una sola partícula» en las condiciones probadas.
Qué significa esto para futuras terapias contra el cáncer
Para no especialistas, la conclusión principal es que los imanes por sí solos no pueden extraer de forma fiable nanopartículas libremente suspendidas de un torrente sanguíneo de rápido movimiento. En cambio, los efectos magnéticos apreciables surgen solo cuando las partículas ya se han ralentizado, asentado o aglomerado, situaciones que efectivamente amplifican su respuesta magnética. Los modelos vasculares generalizados impresos en 3D presentados aquí ofrecen una forma estandarizada de explorar tales efectos a través de diferentes geometrías de red y regímenes de flujo. Para la dirección magnética de fármacos en el futuro, este trabajo sugiere que las estrategias exitosas probablemente necesitarán explotar comportamientos colectivos —como la agregación controlada o sistemas portadores— en lugar de confiar en dirigir nanopartículas aisladas a través de vasos grandes y de rápida perfusión.
Cita: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Palabras clave: dirección magnética de fármacos, nanopartículas, vasculatura tumoral, modelos microfluídicos, administración de fármacos