Clear Sky Science · es
Dirigir el eje Akt–EphA2 y la adhesión célula–célula aumenta la sensibilidad a la anoikis en células cancerosas
Por qué importan las células cancerosas que flotan libres
Cuando las células cancerosas se desprenden de un tumor y viajan por el torrente sanguíneo, normalmente deberían morir porque pierden su agarre con el tejido circundante. Este programa de seguridad incorporado, llamado muerte celular inducida por desprendimiento, ayuda a evitar que tejidos crezcan donde no deben. Sin embargo, las células cancerosas metastásicas a menudo aprenden a ignorar esta señal y permanecen vivas mientras flotan, lo que facilita que formen nuevos tumores. Este estudio plantea una pregunta aparentemente sencilla: si restauramos un «sentido del tacto» mecánico clave en células de cáncer de mama agresivas, ¿podemos forzar a estas células errantes a morir, y si no, qué trucos de respaldo usan para sobrevivir?
Reavivar un sentido del tacto perdido
Las células evalúan constantemente la rigidez de su entorno, tirando de las estructuras que las anclan. En tejido sano, perder contacto o aterrizar sobre una superficie muy blanda tiende a desencadenar la autodestrucción. La proteína Tropomiosina 2.1 (Tpm2.1) es una parte importante de esta maquinaria interna de tensión y a menudo falta o está reducida en células cancerosas. Los investigadores usaron una línea celular de cáncer de mama metastásico ampliamente estudiada y la modificaron para producir más Tpm2.1, restaurando gran parte de esta detección de rigidez. Cuando estas células modificadas se forzaron a crecer en platos especiales que impiden la adhesión, sí experimentaron más muerte celular, crecieron más despacio y se movieron menos que las células cancerosas no modificadas. Aun así, incluso tras varios días en suspensión, aproximadamente el 70 % de las células que expresaban Tpm2.1 seguían vivas, lo que sugiere que revivir su sentido del tacto por sí solo no resuelve completamente el problema.
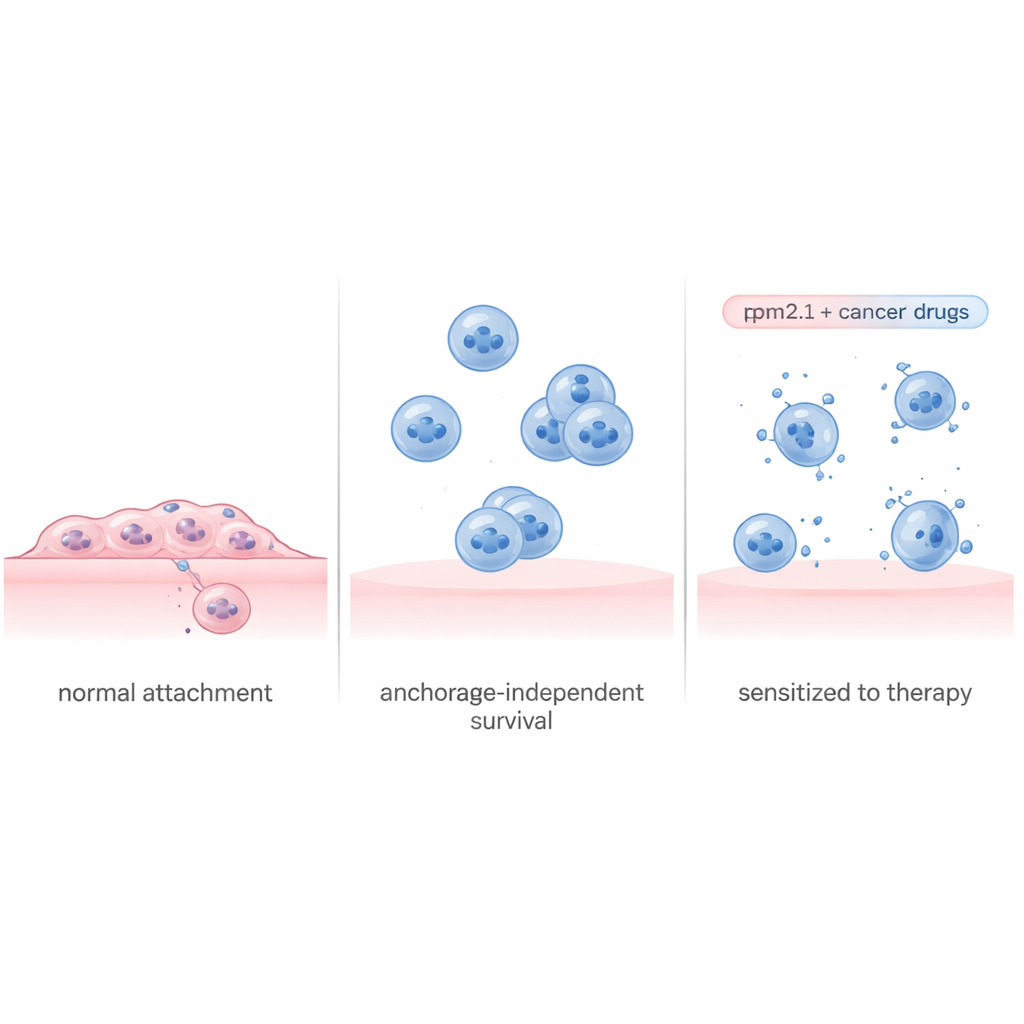
Leer el manual de supervivencia de las células cancerosas
Para entender por qué algunas células morían mientras otras vivían, el equipo separó las células flotantes que expresaban Tpm2.1 en dos grupos: las que mostraban signos tempranos de muerte celular y las que parecían sanas. Luego midieron qué genes estaban activados o desactivados en cada grupo durante cuatro días. Las células moribundas mostraron un apagado general de programas relacionados con la división celular, la reparación del ADN y la adhesión, junto con señales de estrés que parecían un camino sin retorno hacia la autodestrucción. En contraste, las células que sobrevivieron activaron un plan de supervivencia coordinado. Poco después del desprendimiento, encendieron vías inflamatorias y relacionadas con el sistema inmune y, más tarde, aumentaron importantes circuitos de crecimiento y supervivencia, incluido un conocido eje centrado en la proteína Akt. Al mismo tiempo, reforzaron con fuerza genes que ayudan a las células a adherirse entre sí, lo que les permite formar cúmulos protectores incluso sin agarrarse a la matriz circundante.
Fuerza en los números: cómo los cúmulos celulares resisten la muerte
Dado que los datos genéticos apuntaban a un aumento de la adhesión célula–célula, los investigadores probaron si la simple aglomeración podía ayudar a las células a sobrevivir en suspensión. Cuando las células que expresaban Tpm2.1 se cultivaron a alta densidad, donde la formación de cúmulos era fácil, murieron muchas menos células que cuando se mantuvieron dispersas. Una molécula de adhesión, ICAM1, destacó por estar especialmente elevada en las células que sobrevivieron y ya se sabe que ayuda a formar cúmulos de células tumorales circulantes y a que se alojen en tejidos distantes. Bloquear ICAM1 con un inhibidor de pequeña molécula hizo que más células que expresaban Tpm2.1 murieran en suspensión, mientras que tuvo poco efecto en cultivos adheridos estándar. Estos hallazgos respaldan la idea de que, una vez que su mecánica interna se restaura parcialmente, las células cancerosas aún pueden escapar de la muerte aferrándose literalmente unas a otras en lugar de al entorno.
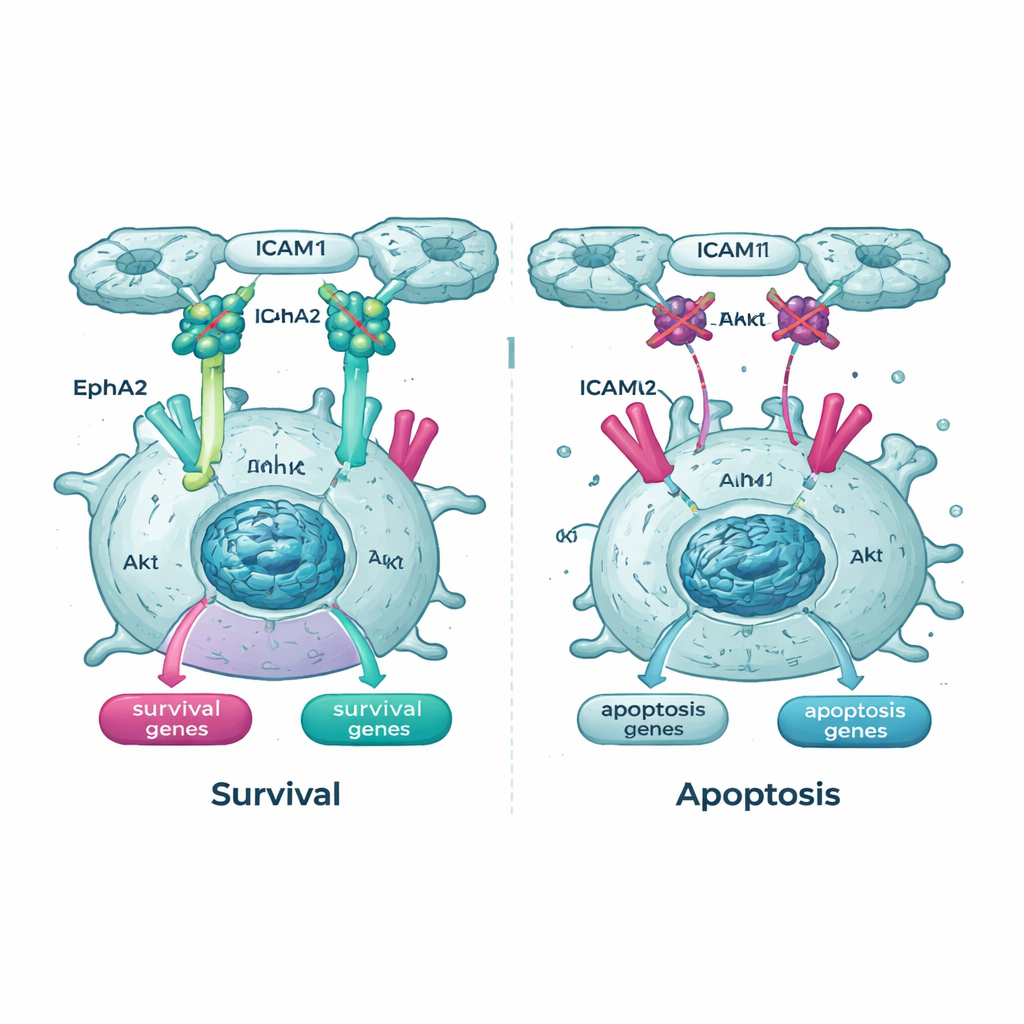
Cortar líneas vitales clave dentro de la célula
Los muestreos genéticos también destacaron la vía Akt y uno de sus socios, un receptor llamado EphA2, como líneas vitales importantes para las células cancerosas en suspensión. En las células que expresaban Tpm2.1, la forma activa fosforilada de Akt era más baja en suspensión que en las células control, y los niveles y la actividad de EphA2 también se redujeron. Cuando el equipo trató las células con fármacos que bloquean Akt o EphA2, tanto las células cancerosas normales como las que expresaban Tpm2.1 se volvieron mucho más propensas a morir en suspensión. Es notable que las células con la detección de rigidez restaurada fueron especialmente sensibles a estos fármacos con el tiempo, lo que implica que una vez que sus comprobaciones mecánicas de seguridad se reactivan parcialmente, dependen más de las señales de supervivencia que quedan.
Convertir un estado preparado en una debilidad letal
Para un público no especializado, el mensaje clave es que arreglar un interruptor de seguridad roto en las células cancerosas—su capacidad para sentir y responder a la pérdida de contacto—es necesario pero no suficiente para que se autodestruyan. Las células que sobreviven lo hacen agrupándose y redirigiendo su cableado interno a través de vías alternativas de crecimiento y supervivencia. Este trabajo muestra que restaurar la detección de rigidez con Tpm2.1 coloca a las células de cáncer de mama metastásico en un estado «preparado» en el que están más cerca de la muerte, pero aún no comprometidas. Al bloquear entonces la vía Akt–EphA2 y alterar la adhesión célula–célula mediante ICAM1, los investigadores pueden empujar a estas células preparadas hasta el límite y aumentar en gran medida la muerte inducida por desprendimiento. En términos prácticos, el estudio esboza una estrategia para futuras terapias combinadas destinadas a eliminar las células tumorales flotantes antes de que puedan sembrar nuevas metástasis.
Cita: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Palabras clave: metástasis del cáncer de mama, adhesión celular, anoikis, señalización Akt, detección de rigidez