Clear Sky Science · es
Impacto de la microbiota Oligo‑MM12 definida en la colonización intestinal y la diseminación de Listeria monocytogenes
Por qué importan los microbios en tu intestino
Muchas personas conocen a Listeria monocytogenes como un germen transmitido por los alimentos que puede causar enfermedades graves en alimentos listos para consumir y en individuos vulnerables. Lo que es menos obvio es que la capacidad de esta bacteria para establecerse en el cuerpo depende no solo de nuestro sistema inmunitario, sino también de la bulliciosa comunidad de microbios que ya habitan en nuestros intestinos. Este estudio utiliza modelos murinos diseñados y un "colon artificial" en miniatura para plantear una pregunta simple pero importante: ¿cómo influye la complejidad del microbioma intestinal en la capacidad de Listeria para colonizar el intestino y diseminarse por el organismo?
Historia de dos barrios microbianos
Para abordar esta cuestión, los investigadores compararon dos tipos de ratones. Un grupo, denominado ratones SPF, portaba una mezcla rica y natural de bacterias intestinales similar a la que se encuentra en muchos animales de laboratorio. El otro grupo, ratones Oligo‑MM12, albergaba una comunidad mucho más sencilla compuesta por solo 12 cepas bacterianas bien caracterizadas. Dado que se conoce a cada miembro de esta comunidad y se mantiene estable entre generaciones, los ratones Oligo‑MM12 son una herramienta potente para desentrañar qué microbios ayudan a bloquear a los invasores y cuáles pueden dejar huecos en nuestras defensas. Al comparar estos ratones, el equipo pudo evaluar cómo un ecosistema intestinal denso y diverso difiere de uno depurado y minimalista a la hora de afrontar un desafío infeccioso.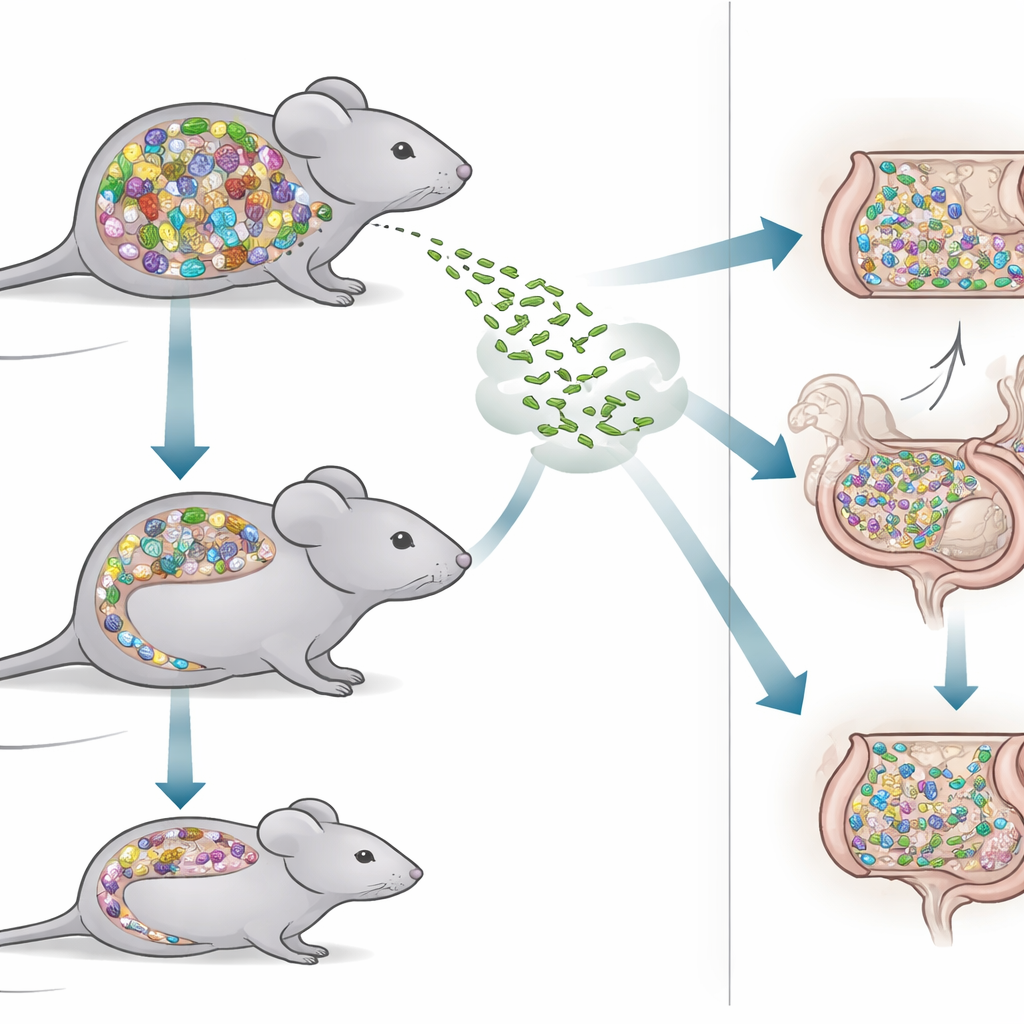
Siguiendo a Listeria por el intestino y más allá
Los científicos infectaron por vía oral ambos tipos de ratones con la misma dosis de Listeria y monitorizaron cuántas bacterias aparecían en las heces y en órganos internos durante tres días. Curiosamente, la comunidad más simple Oligo‑MM12 pareció inicialmente más eficaz en contener a Listeria: al primer día tras la infección, estos ratones expulsaron menos células de Listeria en las heces que los ratones SPF. Sin embargo, esa ventaja temprana se desvaneció. Para el tercer día, los ratones Oligo‑MM12 estaban eliminando más Listeria, mientras que los ratones SPF habían reducido progresivamente los niveles. A pesar de estas diferencias claras en el intestino, las cantidades de Listeria en órganos internos como el hígado, el bazo y los ganglios linfáticos fueron similares entre ambos modelos murinos, lo que sugiere que, una vez que Listeria alcanza tejidos profundos, la complejidad del microbioma desempeña un papel menor.
Simular el colon en una caja controlada
Para separar los efectos de los tejidos y la inmunidad del huésped del comportamiento de los propios microbios, el equipo también realizó un experimento ex vivo usando un dispositivo llamado biorreactor micro‑Matrix. Prepararon suspensiones fecales de cada tipo de ratón, las añadieron a un medio nutritivo en pocillos sellados y libres de oxígeno, e introdujeron Listeria en algunas de estas culturas en miniatura mientras dejaban otras como controles. Durante cinco días midieron los recuentos de Listeria y secuenciaron ADN bacteriano para seguir cómo evolucionaban las comunidades. En este colon artificial, Listeria creció a niveles similares tanto si se enfrentaba a la microbiota compleja SPF como a la comunidad más simple Oligo‑MM12, y su presencia provocó solo cambios modestos en la composición global de la comunidad. Este contraste con los animales vivos subraya hasta qué punto el sistema inmunitario, el revestimiento intestinal y los flujos de bilis y moco configuran la infección en el intestino real.
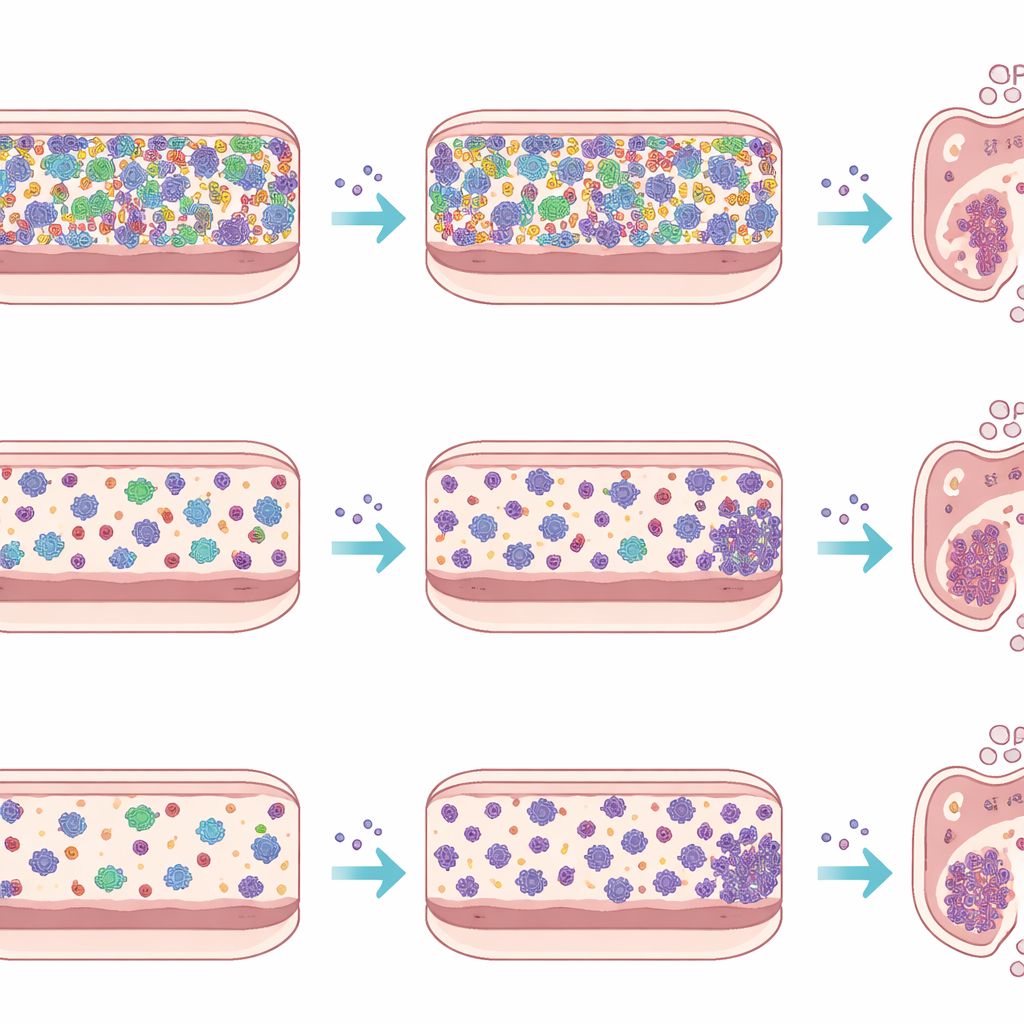
Ganadores, perdedores y espectadores microbianos clave
Al observar qué grupos bacterianos aumentaron o disminuyeron durante la infección, el estudio identifica candidatos que pueden influir en el éxito de Listeria. En los ratones Oligo‑MM12, los niveles de Akkermansia, una bacteria asociada al moco a menudo vinculada a la salud intestinal, bajaron el segundo día para recuperarse con fuerza el tercer día. En los ratones SPF, varios géneros conocidos por producir metabolitos beneficiosos o por apoyar la integridad de la barrera, como Blautia y Bacteroides, decrecieron durante la infección, mientras que ciertas bacterias de tipo Prevotella mostraron subidas y bajadas complejas que podrían reflejar el objetivo directo de compuestos antimicrobianos producidos por la propia Listeria. Ex vivo, estos patrones fueron en gran medida atenuados, lo que refuerza la idea de que muchos de los cambios observados surgen de interacciones a tres bandas entre patógeno, microbios residentes y el entorno del huésped, más que de una simple competencia microbio–microbio.
Qué significa esto para proteger a las personas
Para el público general, el mensaje central es que no todos los microbiomas que parecen saludables protegen contra la infección de la misma manera, y que "más diversidad" no siempre es mejor en todo momento. La comunidad simplificada Oligo‑MM12 proporcionó una fuerte resistencia temprana a Listeria en el intestino, pero con el tiempo el microbioma más intrincado de los ratones SPF hizo un mejor trabajo eliminando al invasor. El trabajo muestra que modelos de microbiota cuidadosamente diseñados y de baja complejidad, combinados con sistemas ex vivo controlables, pueden revelar qué grupos bacterianos y qué factores ambientales son cruciales para bloquear patógenos transmitidos por los alimentos. En última instancia, estos conocimientos podrían orientar probióticos dirigidos o terapias basadas en el microbioma que refuercen a los aliados microbianos adecuados en el momento oportuno para prevenir infecciones graves por Listeria en pacientes en riesgo.
Cita: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Palabras clave: Infección por Listeria, microbioma intestinal, resistencia a la colonización, modelo murino, probióticos