Clear Sky Science · es
Análisis integrado de reguladores globales y genes de eflujo asociados con la reversión de la resistencia antimicrobiana en Klebsiella pneumoniae multirresistente
Por qué estos gérmenes hospitalarios son tan difíciles de eliminar
En hospitales de todo el mundo, ciertas cepas de la bacteria Klebsiella pneumoniae se han vuelto notoriamente difíciles de tratar. Resistentes a múltiples antibióticos que antes funcionaban de forma fiable, convierten infecciones rutinarias en emergencias que amenazan la vida. Este estudio examina el motor microbiano para entender un truco importante que usan estas bacterias: bombas microscópicas que expulsan los antibióticos fuera de la célula, y los interruptores genéticos que parecen aumentar o disminuir la actividad de esas bombas.
Súperbacterias y sus salidas moleculares de escape
Klebsiella pneumoniae multirresistente se encuentra ya en muchos hospitales, incluido el centro médico iraquí donde se llevó a cabo esta investigación. Estas bacterias pueden sobrevivir a varias familias principales de antibióticos a la vez, como las fluoroquinolonas, los aminoglucósidos y las cefalosporinas de tercera generación. Una forma de lograrlo es instalando potentes “bombas de eflujo” en su envoltura celular. Entre las más importantes está un sistema llamado AcrAB‑TolC, que atraviesa las membranas bacterianas y funciona como una pequeña bomba de achique, captando moléculas de antibiótico dentro de la célula y expulsándolas antes de que los fármacos causen daño serio. Cuando estas bombas están muy activas, la concentración de antibiótico en el interior de la bacteria nunca alcanza niveles letales.
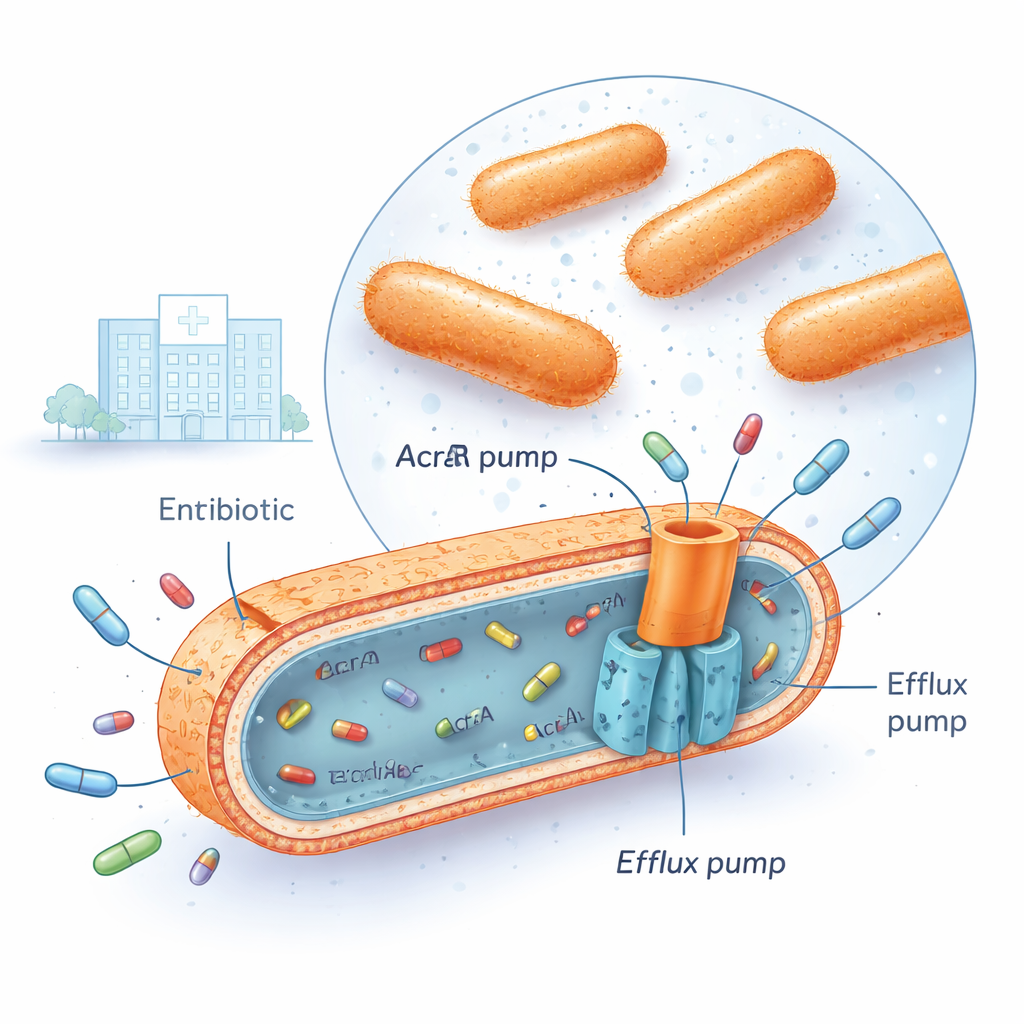
Interruptores génicos que acompañan la sobreactivación de las bombas
Los investigadores recogieron 30 aislados clínicos multirresistentes de Klebsiella pneumoniae y los compararon con 10 aislados susceptibles a antibióticos y una cepa de referencia estándar. Utilizando una técnica llamada PCR cuantitativa en tiempo real, midieron cuánto estaban activados ciertos genes. Se centraron en tres “reguladores globales”: genes denominados marA, soxS y rob, junto con las tres partes de la bomba AcrAB‑TolC (acrA, acrB y tolC). En las cepas resistentes, dos reguladores, marA y soxS, normalmente se mostraron elevados entre cuatro y cinco veces respecto a las bacterias susceptibles, mientras que acrB, un componente central de la bomba, aumentó casi ocho veces. El análisis estadístico mostró que cuando los niveles de marA y soxS eran altos, los de acrB también solían serlo, y esas cepas tendían a soportar dosis mucho mayores de fluoroquinolonas como la ciprofloxacina. Un tercer regulador, rob, cambió poco y no se correlacionó con la actividad de la bomba, lo que sugiere que desempeña un papel menor en las condiciones probadas.
Apagar las bombas para debilitar la resistencia
Comprobar que los genes de bombas y reguladores están activos a la vez es sugestivo pero no suficiente para demostrar que realmente impulsan la resistencia. Para probar si las bombas eran funcionalmente importantes, el equipo recurrió a una herramienta química llamada PAβN. Este compuesto no se usa como fármaco en pacientes, pero en el laboratorio puede taponar bombas similares a AcrAB‑TolC e impedir que expulsen antibióticos. Los científicos eligieron diez aislados resistentes que mostraban niveles especialmente altos del gen acrB y midieron cuánta ciprofloxacina se necesitaba para detener su crecimiento, con y sin PAβN. En ocho de esas diez cepas, bloquear la bomba redujo la dosis necesaria de ciprofloxacina al menos cuatro veces, y a veces hasta dieciséis veces. Esta reducción muestra que, en muchas de estas superbacterias, las bombas de eflujo activas son de hecho una razón principal por la que toleran dosis altas de antibióticos.
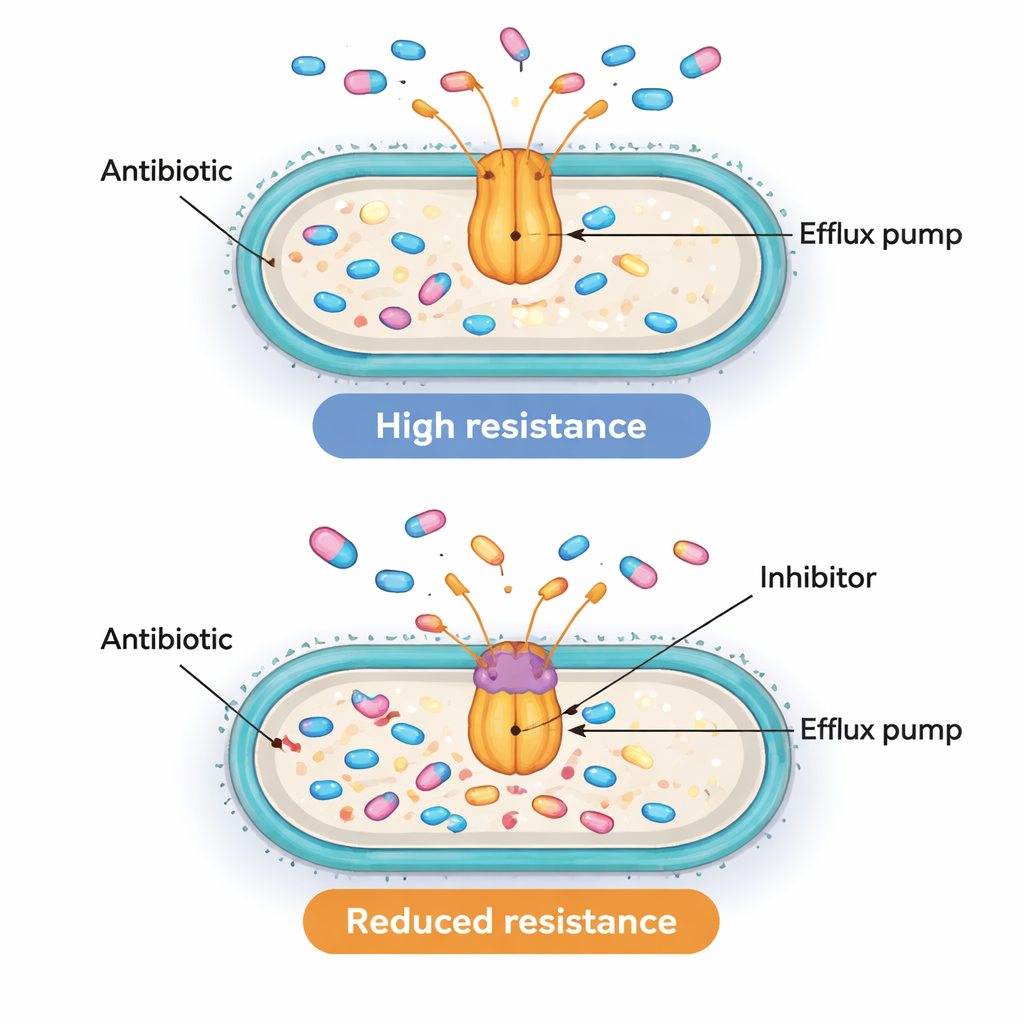
Un rompecabezas de resistencia complejo con objetivos prometedores
No todas las cepas se comportaron igual. Algunas bacterias con expresión elevada de genes de la bomba solo recuperaron parcialmente la sensibilidad cuando las bombas fueron bloqueadas, lo que implica que otras vías de resistencia —como cambios en el blanco del antibiótico dentro de la célula, producción de enzimas que inactivan el fármaco, o bombas alternativas— también contribuyen. La gentamicina, un antibiótico aminoglucósido, por ejemplo, permaneció en gran medida sin verse afectada por los patrones observados en marA/soxS y AcrAB‑TolC, subrayando que la multirresistencia suele construirse a partir de varias defensas superpuestas en lugar de un único mecanismo.
Qué significa esto para tratamientos futuros
Para el público general, el mensaje clave es que algunas bacterias hospitalarias pueden sobrevivir a los antibióticos no solo bloqueando o degradando los fármacos, sino expulsándolos activamente. Este estudio asocia una mayor actividad de dos “interruptores” genéticos, MarA y SoxS, con bombas de eflujo más activas y una mayor resistencia a una clase de antibióticos de uso común. Cuando las bombas se taponan experimentalmente, muchas de estas bacterias recuperan al menos parcialmente la sensibilidad. Aunque el trabajo aún no demuestra exactamente cómo estos reguladores controlan las bombas, destaca tanto a los reguladores como a las bombas como objetivos atractivos. A largo plazo, combinar antibióticos convencionales con bloqueadores seguros de bombas —o con fármacos que reduzcan la actividad de estos reguladores globales— podría ayudar a restaurar la utilidad de tratamientos existentes frente a infecciones multirresistentes por lo demás intimidantes.
Cita: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Palabras clave: resistencia a los antibióticos, bombas de eflujo, Klebsiella pneumoniae, fluoroquinolonas, reversión de la resistencia