Clear Sky Science · es
La disminución de la enzima desubiquitinante USP10 se correlaciona con la apoptosis neuronal en la mielopatía asociada a HTLV-1
Por qué importa a las personas que viven con enfermedades virales del sistema nervioso
Algunos virus no solo provocan infecciones de corta duración; pueden dañar silenciosamente el sistema nervioso durante muchos años. El virus linfotrópico T humano tipo 1 (HTLV-1) es uno de esos virus y puede causar un trastorno crónico de la médula espinal llamado mielopatía asociada a HTLV-1 (HAM). Las personas con HAM pierden gradualmente fuerza y control en las piernas, además de presentar problemas vesicales y sensitivos. Este estudio plantea una pregunta simple pero crucial: ¿por qué mueren las neuronas de la médula espinal en esta afección, y podría una sola molécula protectora ayudar a explicar quiénes evolucionan mejor o peor?
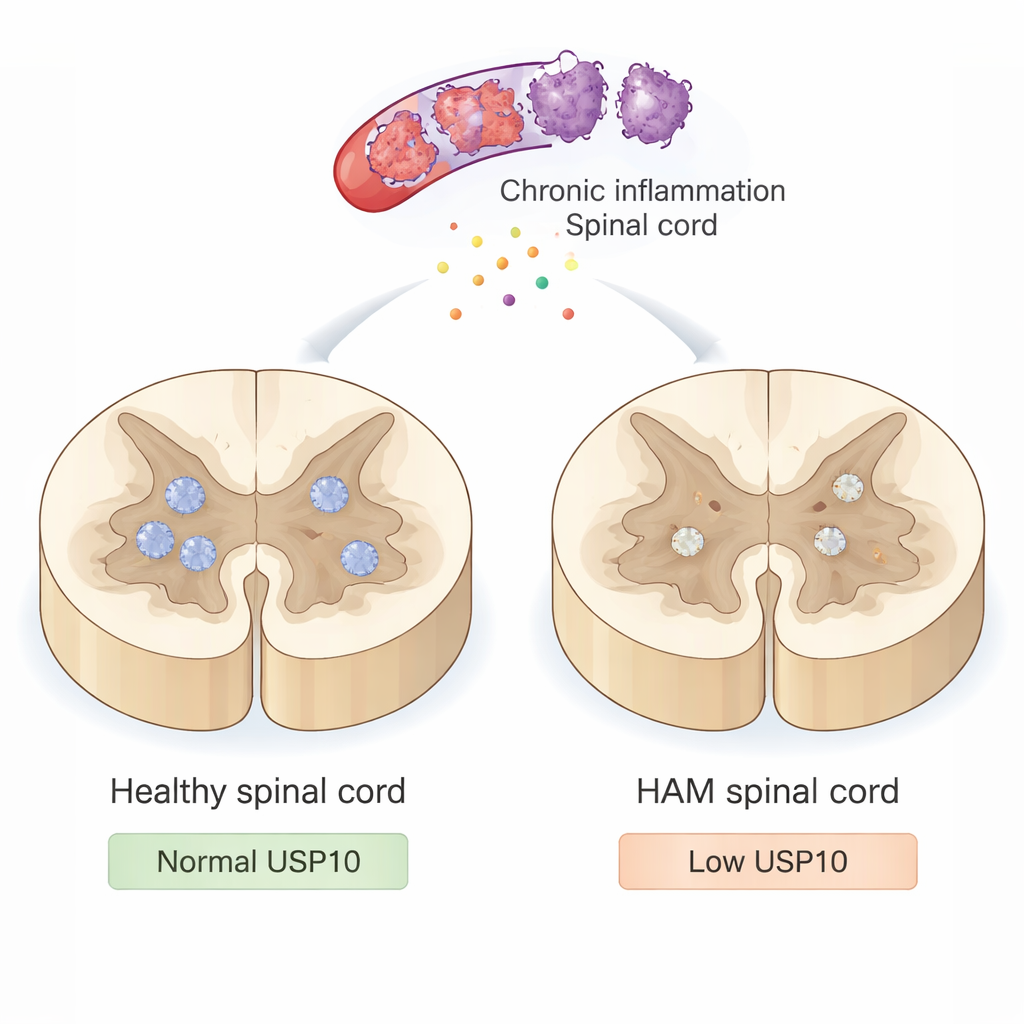
Un ataque lento a la médula espinal
La HAM no se debe a que el virus infecte directamente las neuronas. En cambio, HTLV-1 infecta células inmunitarias que invaden la médula espinal y desencadenan una inflamación prolongada. Estas células inmunitarias hiperactivas liberan sustancias tóxicas y señales inflamatorias que, aunque destinadas a controlar la infección, también lesionan a las neuronas cercanas y su mielina aislante. Con el tiempo, este asedio latente provoca piernas rígidas y débiles y dificultad para caminar. Aun así, los médicos no comprenden del todo por qué algunas neuronas sucumben a este entorno inflamatorio mientras otras sobreviven durante décadas.
Una enzima celular de “limpieza” bajo sospecha
Los investigadores se centraron en una proteína llamada USP10, una enzima que ayuda a gestionar el sistema de control de calidad de proteínas de la célula y que se sabe que limita el estrés celular y la muerte programada (apoptosis). USP10 está activa en muchos tejidos, incluido el cerebro y la médula espinal, y trabajos previos en Parkinson, accidente cerebrovascular y otras afecciones sugieren que ayuda a las neuronas a resistir el daño oxidativo e inflamatorio. Usando muestras de médula espinal de ocho personas que murieron con HAM y de dos controles neurológicos sanos, el equipo empleó técnicas de tinción para ver dónde estaba presente USP10 y cuán intensamente se expresaba en las neuronas.
Menos USP10, más neuronas en muerte
En médulas espinales sanas, USP10 se veía fuertemente en muchas neuronas. Sin embargo, en la mayoría de los casos de HAM, la tinción de USP10 en las neuronas estaba claramente reducida, y en un paciente casi ausente. Los científicos buscaron entonces signos de apoptosis mediante dos métodos: una prueba TUNEL que detecta ADN fragmentado y tinción para caspasa-3 activa, una proteína involucrada tempranamente en la muerte celular. En los controles, prácticamente ninguna neurona mostró estas señales de muerte. En contraste, en los pacientes con HAM, una gran fracción de neuronas fue positiva en TUNEL y muchas mostraron caspasa-3 activa. Importante: las muestras con menor expresión de USP10 tendían a tener más neuronas apoptóticas y menos neuronas sobrevivientes marcadas por NeuN, un marcador neuronal estándar. Un paciente notable con HAM que aún caminaba con solo un bastón tras 22 años tenía una fuerte expresión de USP10 y un número de neuronas relativamente preservado, lo que sugiere que niveles mayores de USP10 podrían ayudar a proteger frente a una discapacidad severa.
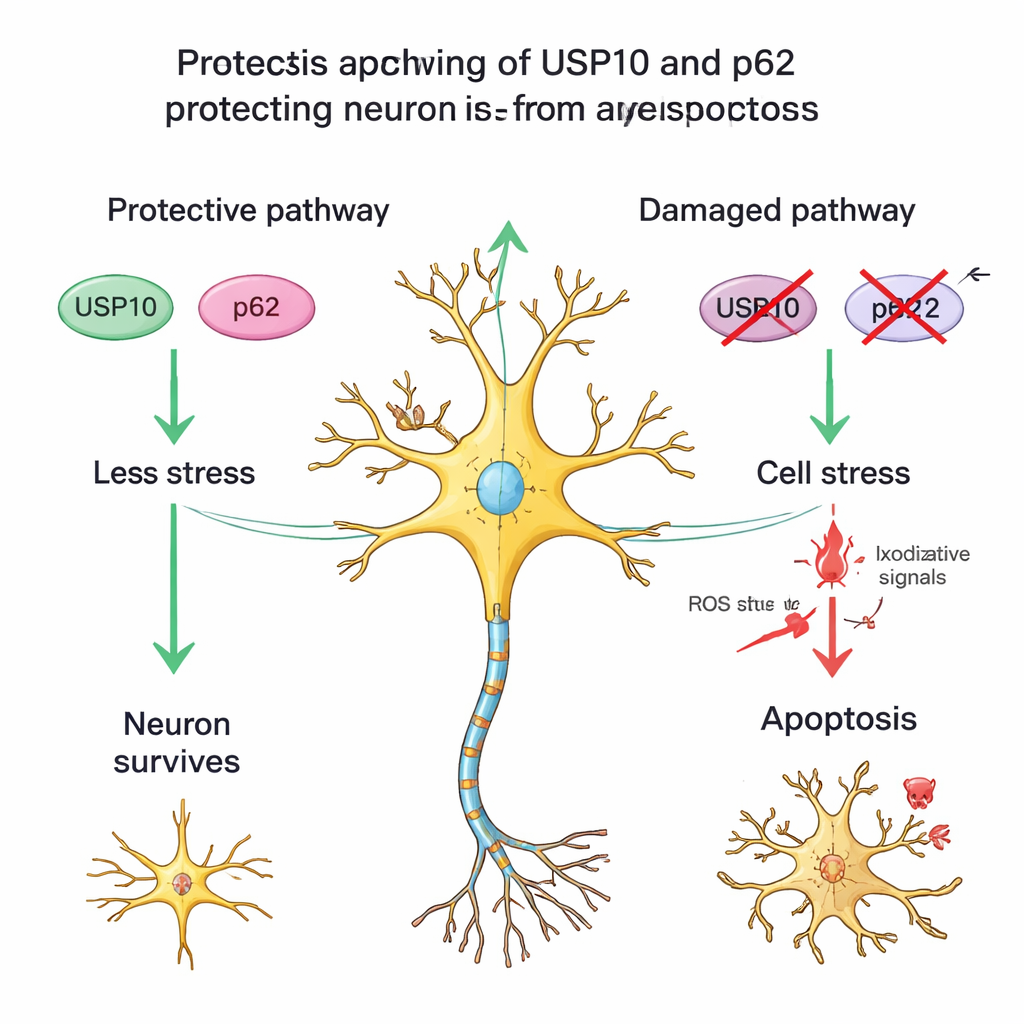
Una proteína compañera y células estresadas pero supervivientes
El equipo también examinó otra proteína, p62, que actúa junto con USP10 en el manejo de proteínas dañadas y en la regulación de vías de estrés y supervivencia. En médulas espinales sanas, la tinción de p62 fue moderada; entre los pacientes con HAM, aquellos con baja USP10 a menudo también presentaban tinción de p62 más débil y menos neuronas sobrevivientes. Este patrón respalda la idea de una asociación USP10–p62 que ayuda a las neuronas a soportar la inflamación crónica. Además, los investigadores observaron muchas neuronas en el tejido de HAM que conservaban la morfología típica de las células nerviosas pero habían perdido la tinción de NeuN, un signo visto en otras lesiones cerebrales cuando las neuronas están bajo estrés grave pero no completamente muertas. Esto sugiere que en HAM, algunas neuronas no solo se pierden por completo, sino que otras permanecen en un estado dañado y vulnerable, posiblemente porque las defensas vinculadas a USP10 están debilitadas.
Qué podría significar esto para el diagnóstico y el tratamiento futuros
Este estudio no demuestra que la pérdida de USP10 cause directamente la muerte neuronal, porque se basa en un número pequeño de muestras de autopsia y no puede seguir los cambios en el tiempo. Aun así, los vínculos consistentes entre baja USP10, reducción de p62, más señales de apoptosis y menos neuronas sobrevivientes apuntan a una vía común que podría unir la inflamación crónica con la lenta degeneración neuronal en la HAM. Para los pacientes, esto plantea una posibilidad alentadora: medir o potenciar las vías relacionadas con USP10 en la médula espinal —o potencialmente en muestras más accesibles como el líquido cefalorraquídeo— podría algún día ayudar a identificar a quienes tienen mayor riesgo de progresión rápida, orientar el seguimiento o inspirar nuevos tratamientos diseñados para reforzar los sistemas de protección frente al estrés de la propia célula en enfermedades neuroinflamatorias inducidas por virus.
Cita: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Palabras clave: Mielopatía asociada a HTLV-1, neuroinflamación, apoptosis neuronal, USP10, degeneración de la médula espinal