Clear Sky Science · es
Actividad antibacteriana y citotoxicidad de cementos a base de silicato tricálcico con diferentes aditivos antibacterianos
Por qué importa para tu próximo empaste
Cuando tienes una cavidad profunda, los dentistas intentan hoy conservar la mayor cantidad posible de tejido dental natural en lugar de eliminarlo todo mediante el taladro. Eso a menudo significa que se deja una fina capa de dentina ablandada con bacterias bajo el empaste. Este estudio plantea una pregunta simple pero crucial: ¿podemos mejorar un cemento de restauración dental muy usado para que elimine silenciosamente los gérmenes residuales sin dañar las células vivas dentro del diente?
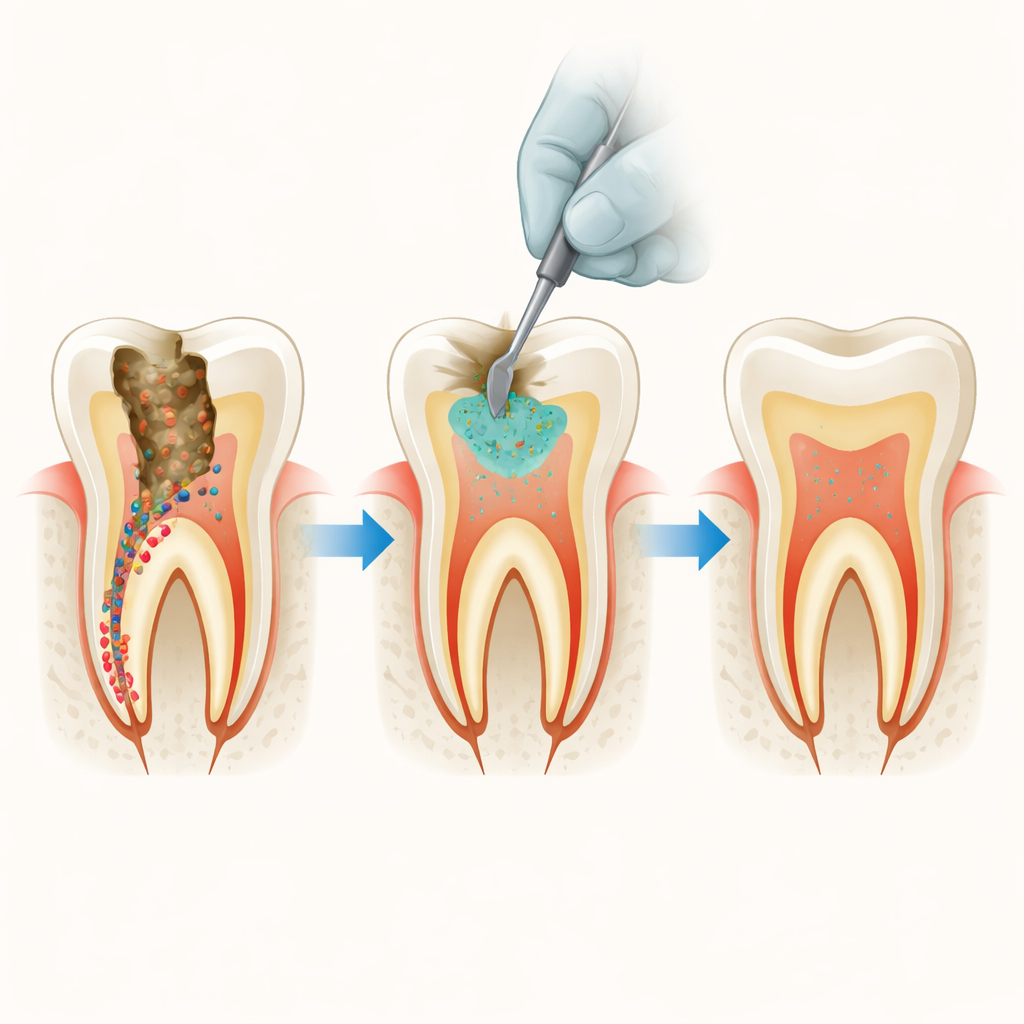
Caries profundas y gérmenes ocultos
Las técnicas modernas de "perforación mínima" buscan evitar exponer el núcleo blando del diente, la pulpa, dejando dentina que todavía puede remineralizarse. La desventaja es que algunas bacterias que causan caries, como Streptococcus mutans y especies de Lactobacillus, pueden permanecer en esa capa. Con el tiempo, estas bacterias pueden provocar una nueva desmineralización bajo un empaste que parece sano. Los cementos a base de silicato tricálcico son populares para sellar cavidades profundas porque favorecen la re‑formación de minerales y crean una barrera hermética, pero por sí solos no son muy eficaces para detener bacterias.
Convertir un cemento común en un luchador contra gérmenes
Los investigadores tomaron este cemento conocido y mezclaron cinco diferentes aditivos antibacterianos en diversas concentraciones. Dos eran compuestos orgánicos presentes con frecuencia en desinfectantes (cloruro de benzalconio y cetrimida), y tres eran sustancias inorgánicas usadas en productos o materiales dentales (dióxido de titanio, óxido de zinc y fluoruro estanoso). Presionaron estas mezclas en pequeños discos y los colocaron sobre placas recubiertas con cinco tipos de bacterias relacionadas con la caries y las infecciones orales. Midiendo las zonas claras alrededor de cada disco donde las bacterias no crecían, pudieron evaluar cuán eficaz era cada formulación para frenar a los gérmenes.
Encontrar el punto óptimo entre matar gérmenes y respetar las células
Dado que un material que mata bacterias pero también envenena las células dentales sería inútil en la boca, el equipo también evaluó cómo afectaban los aditivos más prometedores a células vivas. Expusieron de forma indirecta dos tipos de células humanas—fibroblastos, que son células de soporte comunes, y células madre de la pulpa dental, que contribuyen a reparar el tejido dental—al cemento. Una prueba de cambio de color midió cuántas células permanecían activas, y colorantes fluorescentes especiales mostraron células vivas (verde) y muertas (rojo) bajo el microscopio. Este montaje imitó la situación real en una cavidad profunda, donde el cemento está separado de la pulpa por una delgada capa de dentina y libera sustancias que difunden hacia las células.
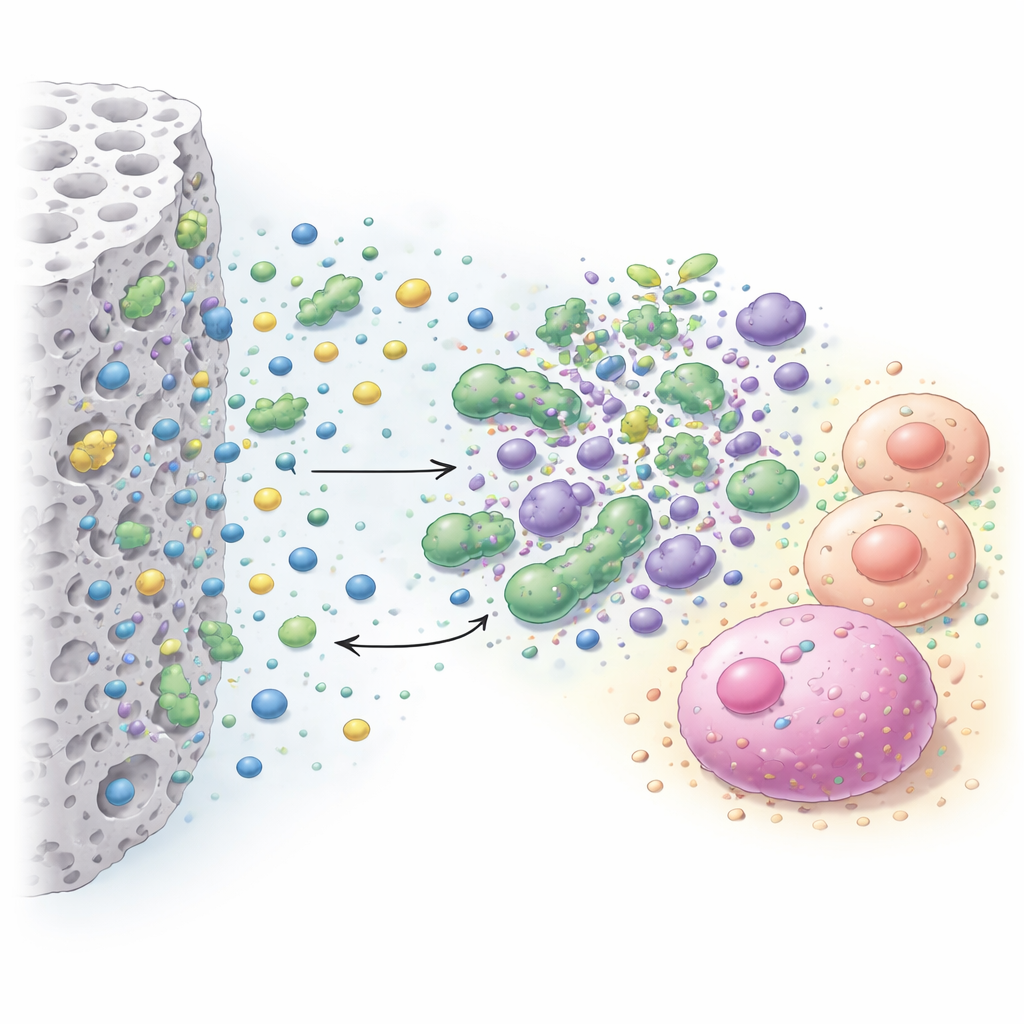
Qué funcionó mejor y qué fue demasiado agresivo
Los resultados mostraron que el tipo y la cantidad de aditivo importaban mucho. El cloruro de benzalconio ofreció el efecto antibacteriano más fuerte y amplio, produciendo grandes zonas libres de gérmenes frente a todas las especies probadas, especialmente las cepas de Lactobacillus que se encuentran a menudo en caries profundas. La cetrimida también ayudó, pero generalmente requirió concentraciones mayores para igualar el rendimiento del benzalconio. Los tres agentes inorgánicos solo mejoraron el efecto antibacteriano del cemento en las dosis más altas probadas y, aun así, principalmente frente a ciertas bacterias como S. mutans y Actinomyces. En cuanto a la seguridad, el cemento base por sí solo fue benigno con ambos tipos celulares e incluso pareció favorecer la salud de los fibroblastos. Añadir cloruro de benzalconio siguió siendo inocuo para los fibroblastos hasta aproximadamente 1%, se volvió ligeramente dañino entre 2 % y 4 %, y claramente más perjudicial al 7%. Las células madre pulpares fueron en general más sensibles: tanto el cloruro de benzalconio como la cetrimida redujeron su supervivencia, con la cetrimida volviéndose moderadamente tóxica a partir del 2%.
Qué podría significar esto para la atención dental futura
En conjunto, el estudio señala una formulación especialmente prometedora: un cemento a base de silicato tricálcico que contenga 1% de cloruro de benzalconio. A ese nivel, el material suprimió con fuerza las bacterias dañinas manteniendo los fibroblastos completamente vivos y las células madre de la pulpa dental mayoritariamente viables. En términos prácticos, sugiere que los empastes profundos del futuro podrían fabricarse con un cemento que combata discretamente los gérmenes residuales bajo la superficie sin ser demasiado agresivo con el tejido vivo del interior del diente. Hace falta más trabajo—especialmente en condiciones bucales reales y complejas—pero esta fórmula equilibrada podría ayudar a los dentistas a proteger mejor los dientes tratados con técnicas mínimamente invasivas.
Cita: Banon, R., Martens, L., De Coster, P. et al. Antibacterial activity and cytotoxicity of tricalcium silicate-based cements with different antibacterial additives. Sci Rep 16, 8349 (2026). https://doi.org/10.1038/s41598-026-37269-5
Palabras clave: caries dentales profundas, cemento dental antibacteriano, silicato tricálcico, cloruro de benzalconio, biocompatibilidad de células pulpares