Clear Sky Science · es
Imágenes de biomoléculas intercelulares usando indicadores de proteína fluorescente con anclajes lipídico-PEG
Observar cómo las células se comunican en tiempo real
Nuestros cerebros y cuerpos dependen de una conversación química continua entre células. Iones y neurotransmisores transportan mensajes a través de pequeñísimos espacios, pero estas señales rápidas y efímeras son difíciles de ver sin perturbarlas. Este estudio presenta una forma sencilla de “pintar” células vivas con sensores luminosos que se adhieren a su superficie externa, lo que permite a los científicos observar estos mensajes —especialmente iones de potasio y el neurotransmisor glutamato— en vivo y con detalle. 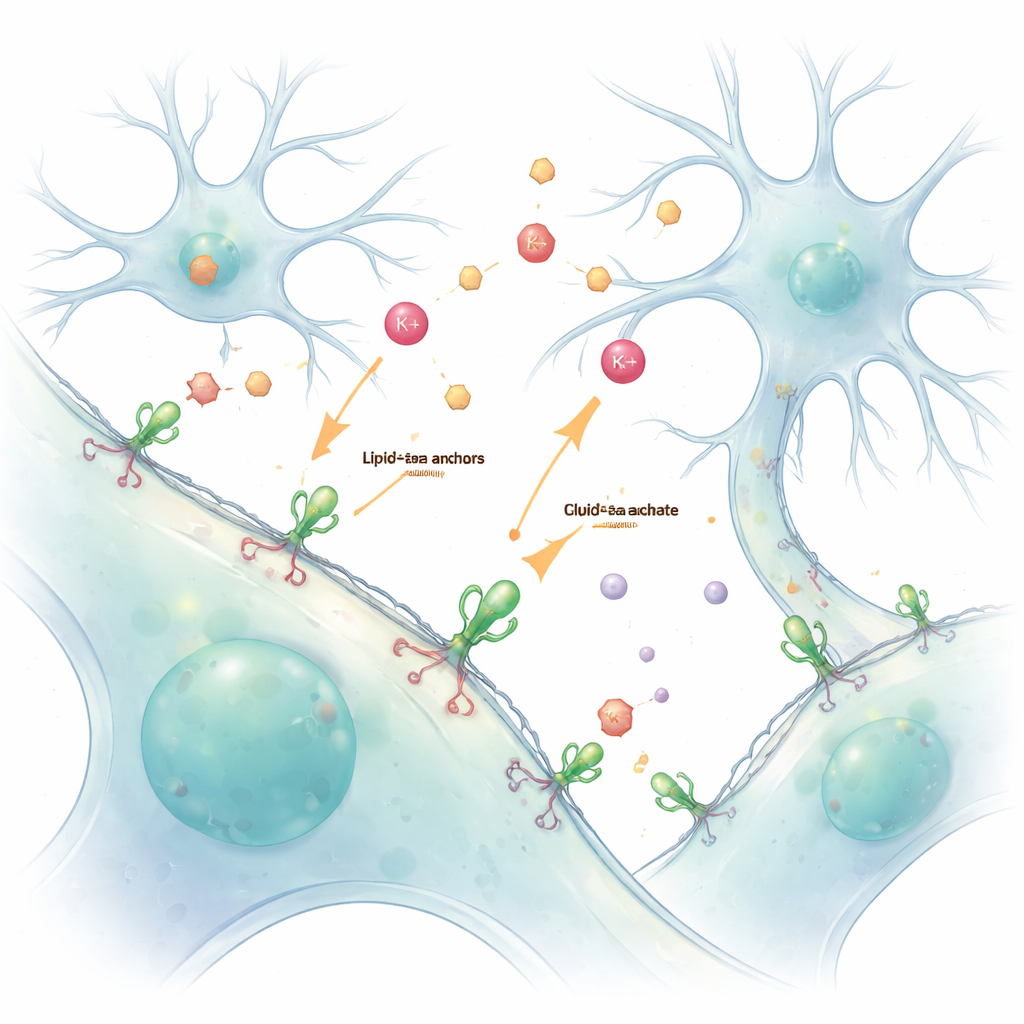
Una nueva forma de etiquetar la superficie celular
Tradicionalmente, los investigadores diseñan células para que produzcan sensores proteicos fluorescentes a partir de su propio ADN. Aunque potente, este enfoque genético con frecuencia sitúa mal los sensores dentro de la célula, dificultando separar lo que ocurre dentro de lo que ocurre fuera. Los autores resolvieron esto usando un manejador químico llamado anclaje lipídico–PEG. Un extremo de esta molécula se incrusta en la membrana externa, mientras que el otro extremo se une químicamente a un sensor de proteína fluorescente. Cuando estos sensores preparados se añaden simplemente a células vivas, recubren de forma espontánea la superficie externa, formando una capa luminosa y estable que informa sobre lo que ocurre en el fluido circundante.
Convertir el potasio y el glutamato en luz
El equipo adaptó dos indicadores fluorescentes existentes: GINKO2, que responde a iones de potasio, y R-iGluSnFR1, que responde al glutamato. Purificaron estas proteínas de bacterias y luego les añadieron los anclajes lipídico–PEG. En células humanas en cultivo, el sensor de potasio anclado formó un contorno suave a lo largo de la superficie celular y se volvió más brillante siempre que aumentó el potasio extracelular, para luego atenuarse cuando los niveles bajaron. Es importante que sus propiedades emisoras de luz y su sensibilidad coincidieron estrechamente con las del sensor original no modificado en experimentos de tubo de ensayo, mostrando que el anclaje no afectó su rendimiento. Lo mismo ocurrió con el sensor de glutamato, que siguió respondiendo tras el anclaje y destacó claramente el glutamato en el espacio justo fuera de las células.
Escuchar a las neuronas en cultivos y cortes
Los investigadores pasaron luego a células nerviosas del hipocampo de ratón, una región cerebral importante para el aprendizaje y la memoria. Recubrieron estas neuronas con el sensor de glutamato anclado lipídico–PEG y cargaron el interior de las mismas células con un tinte de calcio separado que informa sobre la actividad eléctrica. Usando microscopía de reflexión interna total, pudieron observar destellos rojos del glutamato en la superficie celular mientras las señales verdes dentro de las células informaban de la actividad eléctrica. Esta vista bicolor mostró que los sensores anclados podían rastrear la liberación espontánea de neurotransmisores sin necesidad de modificar genéticamente las neuronas.
Mapear ondas químicas a través del tejido cerebral
A continuación, el equipo probó el método en cortes cerebrales agudos, que preservan el cableado natural del hipocampo. Aplicaron el sensor de potasio anclado a los cortes y estimularon eléctricamente las fibras nerviosas. El sensor anclado produjo aumentos de fluorescencia claros y repetibles después de cada estímulo, mientras que los sensores no anclados se difundieron rápidamente y dieron señales débiles e inestables. Bañando los cortes en soluciones con niveles de potasio conocidos y corrigiendo por el leve brillo propio del tejido, los autores construyeron una curva de calibración y estimaron las concentraciones reales de potasio extracelular. Los niveles de base fueron aproximadamente 2,5 milimolar y aumentaron hasta unos 3,4 milimolar con una estimulación moderada, en línea con medidas clásicas por electrodos. Los sensores anclados para potasio y glutamato revelaron cómo estas señales se propagan de forma diferente: los cambios de glutamato se mantuvieron cerca de las sinapsis activas, mientras que los aumentos de potasio se extendieron cientos de micrómetros, sugiriendo efectos más amplios sobre la excitabilidad de la red. 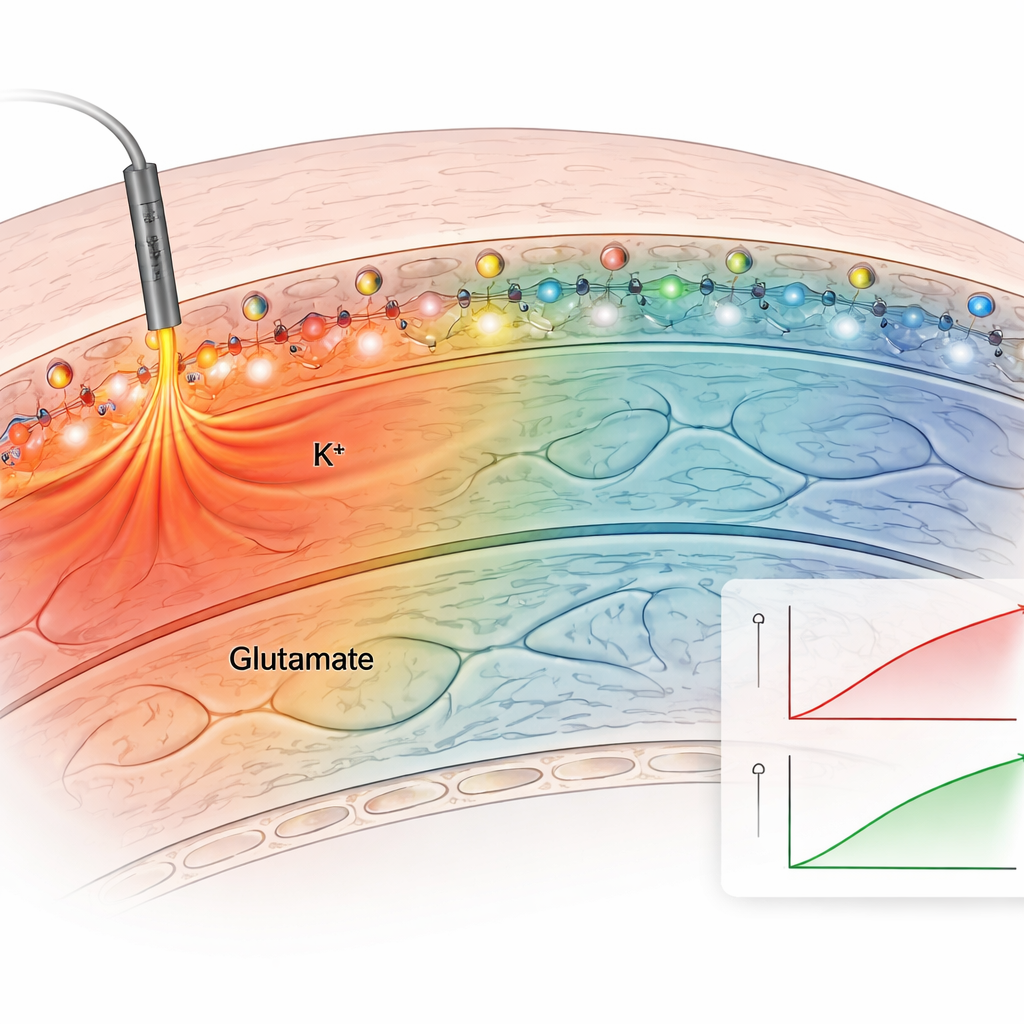
Sondear cómo el cerebro elimina y genera señales
Debido a que los sensores están fijados en la superficie celular, los autores pudieron desentrañar qué procesos moldean estas ondas extracelulares. Bloquear los transportadores de glutamato, que normalmente recogen el glutamato, hizo que el sensor de glutamato anclado mostrara señales más grandes y de mayor duración, confirmando que la captación local limita la propagación del glutamato. Bloquear los receptores de glutamato tipo AMPA redujo tanto las respuestas eléctricas como las señales de potasio, lo que indica que la mayor parte del aumento de potasio proviene de neuronas postsinápticas activadas por la entrada sináptica. Bloquear los canales de sodio con tetrodotoxina casi abolió los cambios de potasio, vinculándolos directamente con los potenciales de acción. En conjunto, estos experimentos ilustran cómo los sensores anclados pueden convertir química compleja y distribuida en películas y mapas intuitivos.
Por qué esto importa para la investigación cerebral futura
Para los no especialistas, el mensaje clave es que este trabajo ofrece una forma rápida y no genética de recubrir células y tejidos vivos con reporteros moleculares altamente sensibles. En lugar de reconfigurar cada tipo celular, los científicos pueden añadir proteínas sensor pre-fabricadas desde el exterior y visualizar de inmediato cómo cambian iones y neurotransmisores en tiempo real en la superficie celular. Este enfoque mejora el control, la reproducibilidad y la precisión espacial al tiempo que evita los retos de la entrega génica, especialmente en preparaciones delicadas como los cortes cerebrales agudos. A medida que se desarrollen más indicadores fluorescentes para diferentes sustancias, la misma estrategia de anclaje lipídico–PEG podría convertirse en un conjunto de herramientas de uso general para observar el lenguaje químico de las células en todo el organismo.
Cita: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Palabras clave: señalización extracelular, biosensores fluorescentes, imagen de glutamato, dinámica del potasio, neuronas del hipocampo