Clear Sky Science · es
Convolución dinámica de grafos con poda exhaustiva y clasificación con GNN para la detección precisa de metástasis en ganglios linfáticos
Por qué importan los cambios diminutos en los ganglios linfáticos
Cuando el cáncer de mama se disemina, su primera parada suele ser los ganglios linfáticos, pequeños filtros situados a lo largo del sistema de drenaje del cuerpo. Detectar si las células cancerosas han llegado a estos ganglios es una de las pistas más importantes que usan los médicos para elegir cirugía, quimioterapia y radioterapia. Sin embargo, incluso los patólogos expertos pueden pasar por alto grupos muy pequeños de células tumorales en imágenes digitales de microscopio, especialmente cuando se parecen mucho al tejido sano. Este estudio presenta un nuevo marco de inteligencia artificial que trata el tejido como una red de regiones conectadas, permitiendo encontrar señales sutiles de diseminación con notable precisión.
Convertir imágenes de tejido en redes
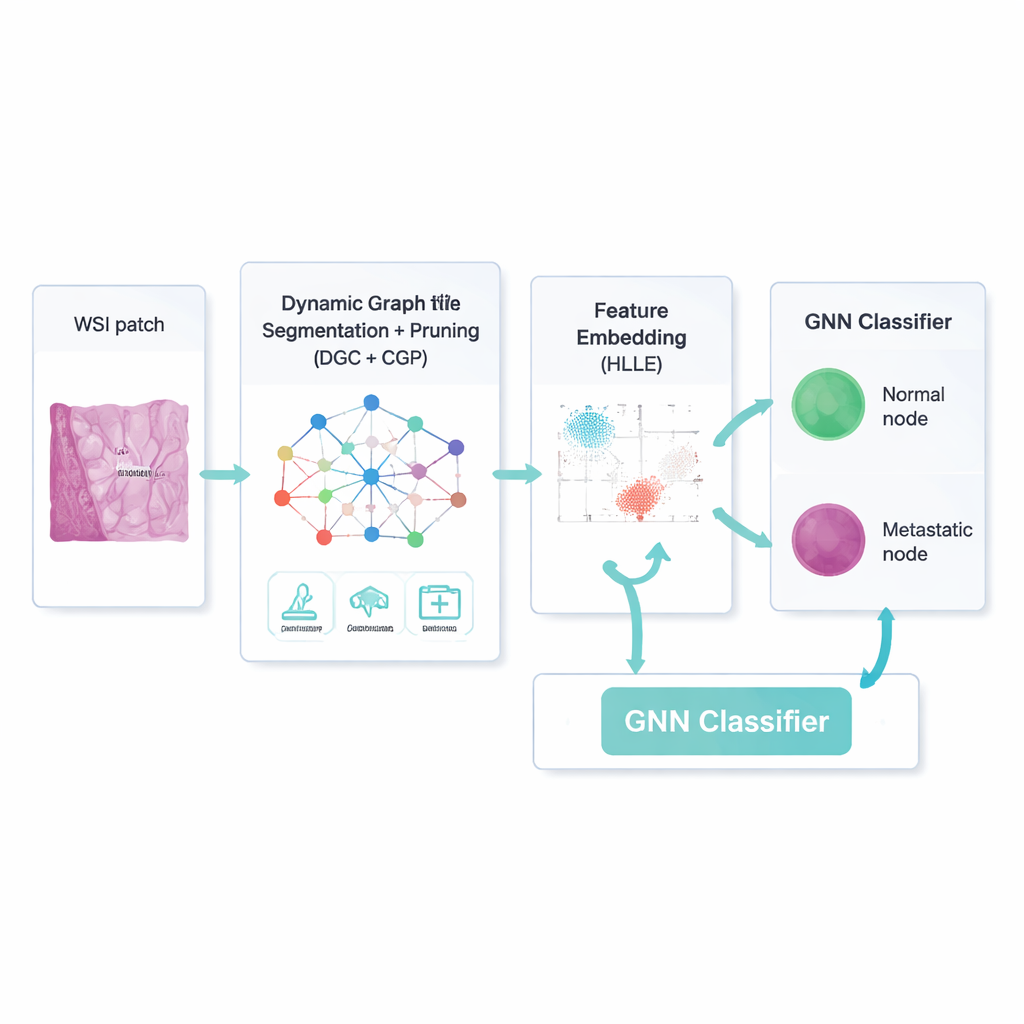
Los investigadores trabajan con enormes diapositivas digitales de tejido teñido, llamadas imágenes de diapositiva completa, procedentes de biopsias de ganglios linfáticos por cáncer de mama. Estas imágenes contienen millones de píxeles y una mezcla desconcertante de tipos celulares, colores y texturas. Para domar esa complejidad, el equipo primero limpia las imágenes: normaliza brillo y color, reduce el ruido y genera copias aumentadas rotando y volteando parches, de modo que el ordenador aprenda a lidiar con la variación natural. Cada parche de imagen se divide luego en regiones pequeñas y relativamente uniformes ("superpíxeles"), que se convierten en los puntos—o nodos—de un grafo, mientras que las relaciones entre regiones vecinas forman las líneas de conexión—o aristas. Esta visión en red preserva las formas y disposiciones irregulares del tejido real mejor que los métodos tradicionales basados en cuadrículas.
Una forma más inteligente de centrarse en lo importante
Construir una red no basta; muchas conexiones y características de imagen son irrelevantes o incluso engañosas. Por eso el marco utiliza un autoencoder convolucional de grafos dinámico—un tipo de red neuronal que aprende tanto cómo es cada región como cómo se influyen entre sí las regiones. Un mecanismo adicional de "atención" enseña al modelo a ponderar algunos canales de imagen más que otros, por ejemplo enfatizando bordes en el límite de un tumor. Al mismo tiempo, una estrategia llamada Poda Gradual Exhaustiva del Grafo recorta de forma sostenida las piezas poco útiles: conexiones débiles entre regiones, características numéricas menos informativas y pesos del modelo de bajo impacto. Esta poda ocurre durante el entrenamiento, no después, de modo que el sistema aprende a hacer más con menos, terminando tanto más rápido como más fácil de interpretar.
Comprimir patrones sin perder su forma
Una vez que el modelo ha separado las regiones probablemente ganglionares del tejido de fondo, aún tiene que describir cada región de manera que sea compacta pero significativa. Para ello, los autores usan una técnica llamada Embedding Lineal Local basado en el Hessiano. En términos sencillos, comprime muchas características numéricas en un conjunto más pequeño mientras intenta preservar la "forma" curva de cómo los ejemplos reales se disponen en el espacio de características—por ejemplo, cómo las metástasis diminutas difieren de las células inmunitarias normales a lo largo de patrones sutiles de textura o color. Estas descripciones comprimidas se convierten en la entrada a un clasificador basado en redes neuronales en grafos, que de nuevo opera sobre la red de regiones y sus conexiones limpiadas, decidiendo para cada nodo si es metastásico o no.
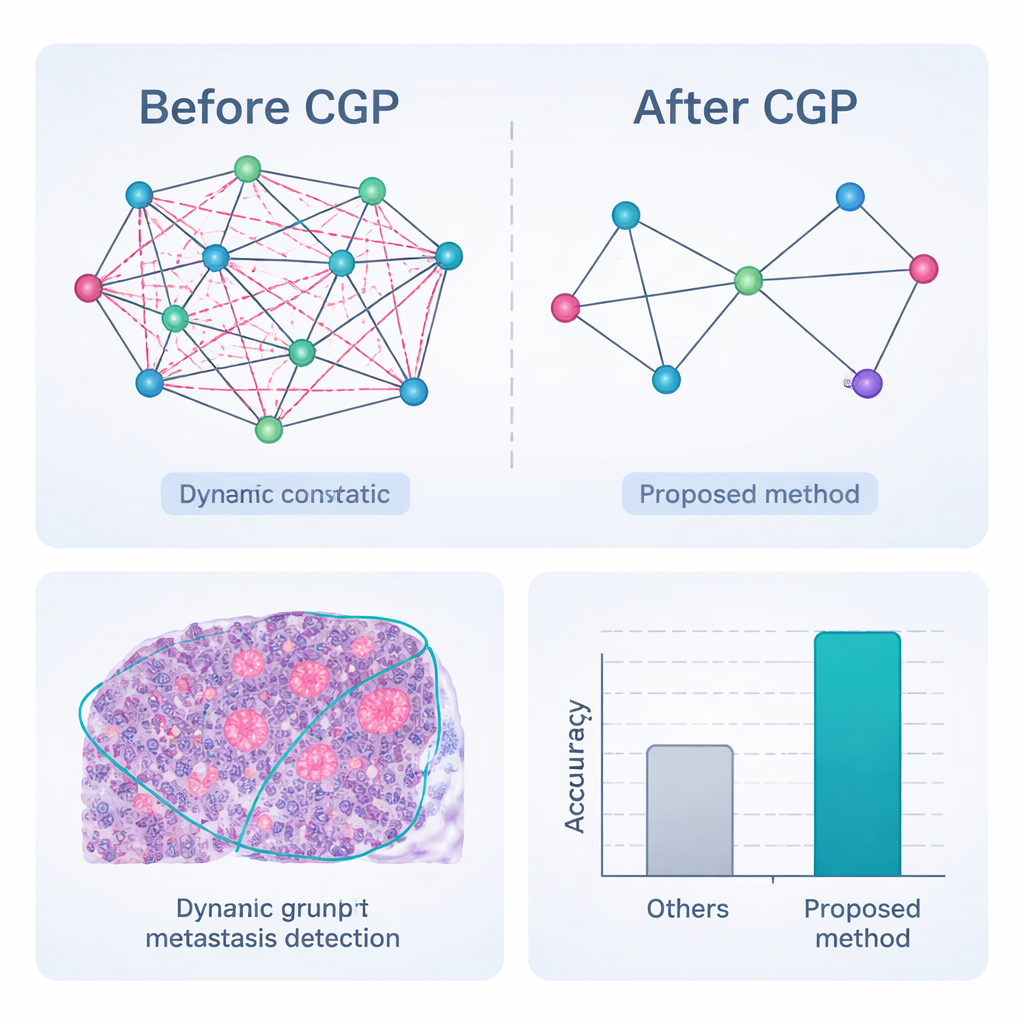
Poner el marco a prueba
La canalización completa—preprocesado, segmentación dinámica de grafos con poda, incrustación de características y clasificación basada en grafos—se evaluó en CAMELYON17, una colección pública de 1.000 diapositivas de ganglios linfáticos anotadas por expertos de pacientes con cáncer de mama. En comparación con una gama de competidores fuertes de aprendizaje profundo, incluidos populares redes convolucionales y modelos híbridos tipo transformer, el nuevo método alcanzó las puntuaciones más altas en casi todas las medidas. Clasificó correctamente los ganglios como cancerosos o no en el 98,65% de los casos y mostró mejor concordancia con los contornos de tumor trazados por expertos, especialmente para metástasis muy pequeñas o tenues. De forma crucial, debido a que el grafo se poda agresivamente, el sistema logra estos resultados con muchas menos operaciones y menor uso de memoria, lo que lo hace más adecuado para el uso en tiempo real en laboratorios de patología concurridos.
Qué supone esto para pacientes y clínicos
En términos cotidianos, este trabajo muestra cómo pensar el tejido como una red inteligentemente recortada de regiones conectadas puede ayudar a que los ordenadores actúen como segundos lectores extremadamente cuidadosos de las diapositivas de ganglios linfáticos. Al centrar la atención y la potencia computacional en las estructuras más informativas mientras descarta el ruido, el marco es mejor para detectar diminutas semillas de cáncer que de otro modo podrían pasarse por alto, y lo hace con suficiente eficiencia como para ser práctico. Aunque se necesita validación clínica adicional, tales herramientas podrían apoyar a los patólogos en la toma de decisiones más rápidas y consistentes sobre si el cáncer se ha diseminado—información que moldea directamente los planes de tratamiento y, en última instancia, los resultados para los pacientes.
Cita: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Palabras clave: metástasis en ganglios linfáticos, patología digital, redes neuronales en grafos, segmentación de imágenes médicas, cáncer de mama