Clear Sky Science · es
Caracterización estructural de la unión de metales en la tirosilproteína sulfotransferasa humana 2, TPST2
Por qué los iones metálicos diminutos importan para la señalización celular
Dentro de nuestras células, innumerables máquinas moleculares ajustan en silencio cómo crecen los tejidos, cómo actúan las hormonas y cómo se comunican las células inmunitarias. Una de esas máquinas, una enzima llamada TPST2, añade una pequeña etiqueta de sulfato a ciertas proteínas mientras pasan por el centro de envío de la célula, el aparato de Golgi. Este estudio revela cómo iones metálicos sencillos como el sodio y el manganeso ayudan a TPST2 a funcionar con más eficacia al reforzar sutilmente partes de su estructura—una idea que puede conectar el equilibrio mineral en las células con el cáncer y enfermedades relacionadas con hormonas. 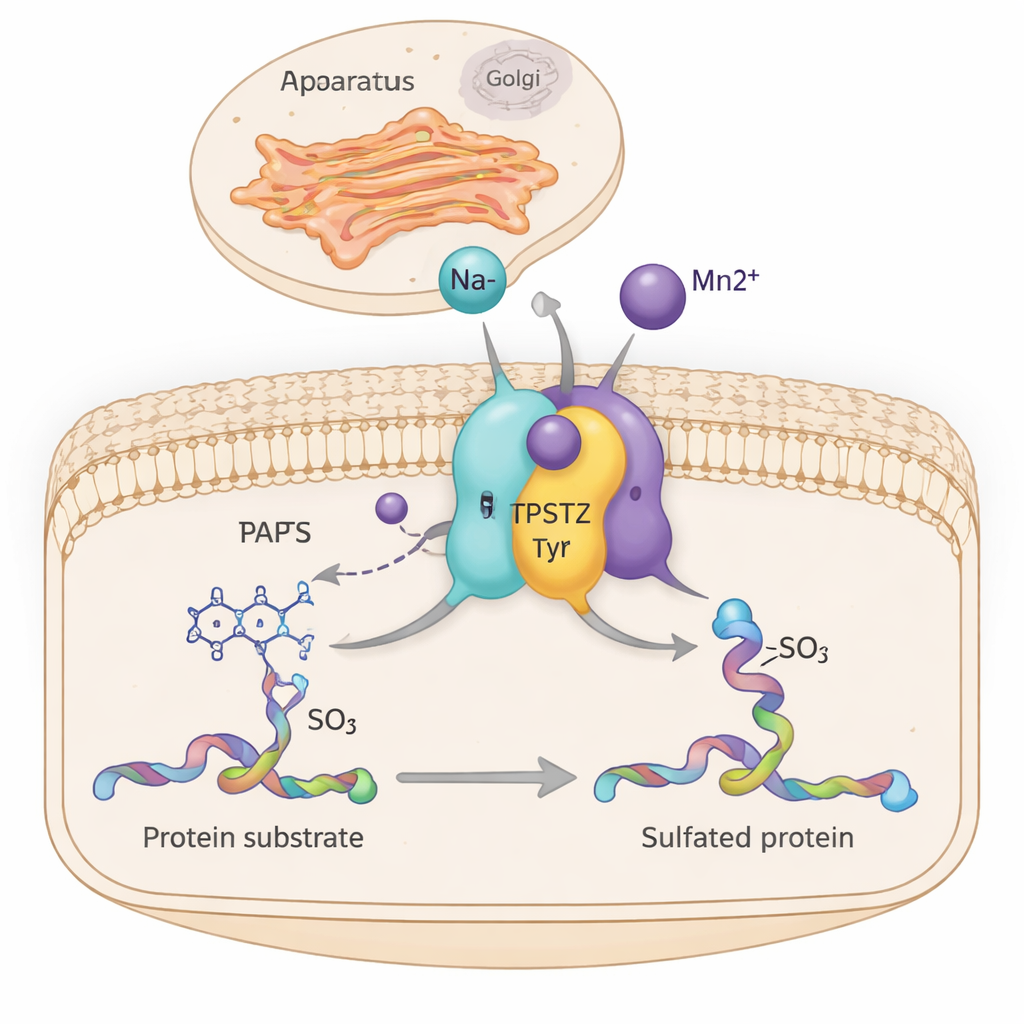
Una proteína que adorna a otras proteínas
TPST2 pertenece a una familia de enzimas que realizan la “sulfonación de tirosina”, una modificación química añadida a residuos de tirosina específicos en las proteínas. Estas proteínas sulfonadas desempeñan papeles clave fuera de las células, influyendo en la coagulación sanguínea, el movimiento de los leucocitos, la unión hormona–receptor e incluso en la entrada de virus en las células. En humanos hay dos enzimas sulfotransferasas principales, TPST1 y TPST2, que se sitúan en la membrana del Golgi y modifican las proteínas mientras se preparan para la exportación. Estudios en ratón muestran que la pérdida de TPST2 interrumpe la producción de hormonas tiroideas, frena el crecimiento y causa infertilidad masculina, subrayando su importancia para la fisiología normal.
Vínculos con el cáncer y eludir la respuesta inmune
Investigaciones recientes han vinculado directamente a TPST2 con la enfermedad. En el melanoma, TPST2 modifica un componente del receptor de interferón de una manera que debilita la señalización inmunitaria, y bloquear TPST2 potencia el efecto de las terapias con inhibidores de puntos de control inmunitario que se dirigen a PD-1. En el cáncer de páncreas, una vía dependiente de TPST2 ayuda a estabilizar una proteína (integrina β4) que promueve el crecimiento y la diseminación del tumor. Inhibir TPST2 en estos modelos ralentiza la división e invasión de las células cancerosas. Dado que TPST2 actúa sobre proteínas en la superficie celular, reconfigura efectivamente cómo las células detectan y responden a su entorno, lo que la convierte en un objetivo atractivo para nuevas terapias.
Encontrar los "interruptores" metálicos
Los bioquímicos sabían desde hace tiempo que TPST2 se vuelve mucho más activa cuando están presentes metales divalentes como el manganeso (Mn²⁺), pero faltaba la razón estructural. En este estudio, los autores produjeron el núcleo catalítico de la TPST2 humana y lo cristalizaron junto con un subproducto de la reacción y con sodio (Na⁺) o manganeso. Empleando cristalografía de rayos X de alta resolución, descubrieron dos pequeños bolsillos de unión a metales dentro de la enzima, cada uno con una ordenada disposición de seis átomos alrededor (octaédrica). Al ajustar la longitud de onda de los rayos X a las firmas únicas de distintos metales, confirmaron que Mn²⁺ ocupa selectivamente estos sitios, mientras que metales como zinc y cobre se unen débilmente en otras ubicaciones o no se unen en absoluto.
Rigidez en piezas móviles clave en lugar de remodelar toda la proteína
De forma sorprendente, TPST2 con sodio y TPST2 con manganeso parecían casi idénticas en conjunto; no hubo una apertura o cierre dramático de la proteína. En cambio, los metales afectaron principalmente a dos regiones flexibles cerca de la entrada del sitio activo: una hélice denominada α3 y un bucle cercano conocido como el bucle α12–α13. En estados sin metal o con unión débil, estos segmentos se mueven y están parcialmente desordenados. Cuando se une Na⁺, se vuelven más ordenados; Mn²⁺ los ajusta aún más, como muestran la reducción del movimiento térmico en los datos de rayos X y los análisis computacionales de flexibilidad. Esta rigidez adicional eleva modestamente la temperatura de fusión de la enzima y se piensa que reduce el coste "entrópico" de organizar el sitio activo—facilitando y acelerando que TPST2 coloque los sustratos en la posición correcta para la sulfonación. 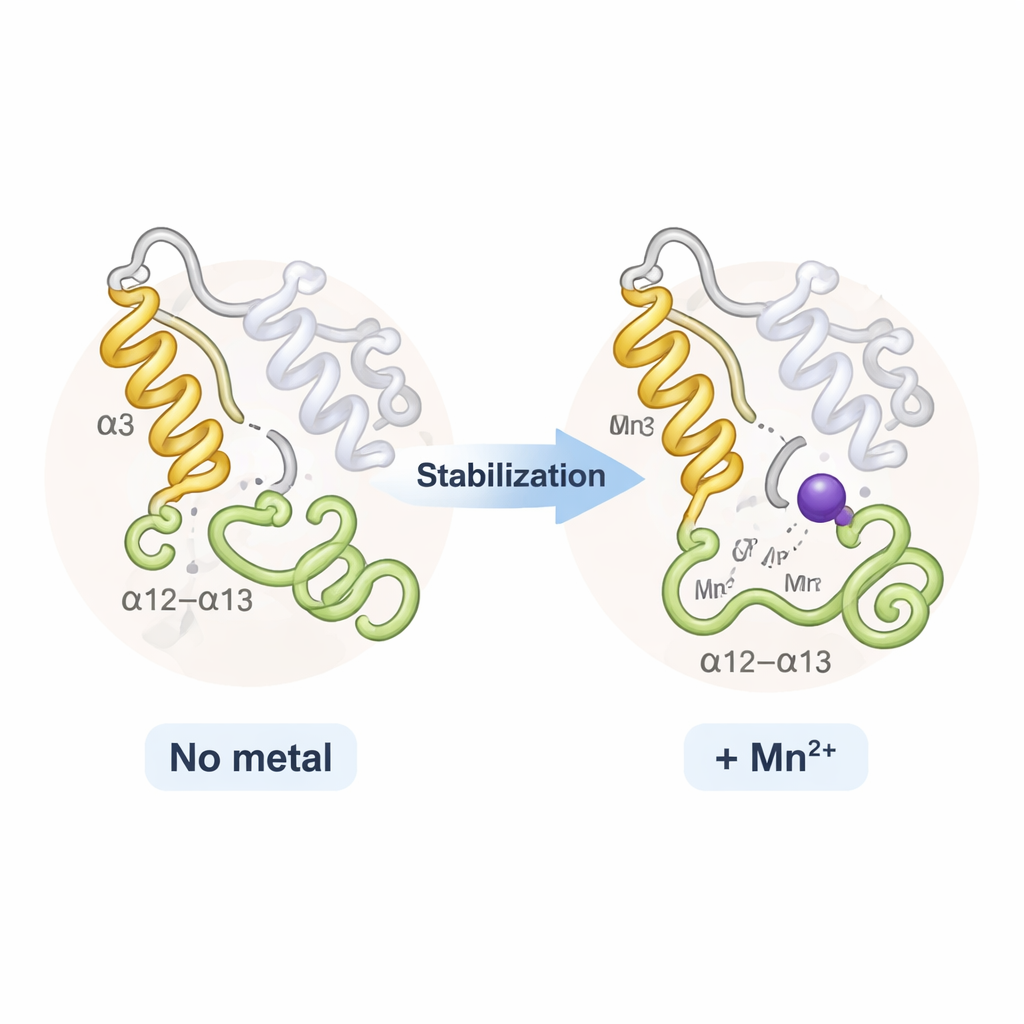
De los minerales celulares al control de la señalización
Los autores proponen un modelo de “activación por ordenación”. En ausencia de metal unido, TPST2 es flexible alrededor de la entrada del sitio activo y funciona de manera poco eficiente. El sodio, abundante en las células, puede unirse a los mismos sitios y crear un estado parcialmente ordenado y moderadamente activo. El manganeso, presente en cantidades micromolares cuidadosamente controladas dentro del Golgi, se une con más fuerza y bloquea las regiones clave en un estado óptimamente arreglado, maximizando la eficiencia catalítica. Esto sugiere que cambios sutiles en los niveles de manganeso del Golgi podrían ajustar la intensidad con la que TPST2 modifica sus dianas. Dado que TPST2 influye en la producción hormonal y en la señalización del cáncer, el trabajo destaca un posible vínculo entre el equilibrio de iones metálicos, las "decoraciones" proteicas y la enfermedad—y ofrece un marco estructural para diseñar fármacos que modulen la actividad de TPST2 imitando o alterando la unión de metales.
Cita: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Palabras clave: sulfonación de tirosina, TPST2, manganeso, aparato de Golgi, modificación de proteínas