Clear Sky Science · es
Enfriamiento ultrarrápido mejorado por presión en superficies sólidas dobles mejora la recuperación post-descongelación en hepatocitos y cortes precisos de hígado
Por qué importa congelar tejido hepático
Mantener células y tejidos vivos fuera del cuerpo es una de las labores silenciosas de la medicina moderna. Las células hepáticas congeladas permiten a los investigadores probar nuevos fármacos, modelar enfermedades y, quizá algún día, reparar órganos en fallo. Pero congelar material vivo es complicado: si los cristales de hielo se forman dentro o entre las células, desgarran estructuras delicadas. Este estudio explora una nueva forma de congelar rápidamente células hepáticas y finos cortes de hígado, y bajo condiciones tan controladas, que los cristales dañinos apenas tienen tiempo de formarse.
El problema del hielo y los protectores químicos
La criopreservación convencional se basa en dos herramientas imperfectas: el frío y los químicos. Al enfriarse, el agua tiende a formar hielo, que puede perforar membranas y alterar tejidos. Para evitarlo, los científicos añaden agentes crioprotectores, como el dimetilsulfóxido (DMSO), que ayudan a que el agua pase a un estado vítreo en lugar de cristalino. Sin embargo, a las altas concentraciones normalmente usadas, estos agentes pueden ser tóxicos para las células o provocar hinchazón y contracción dañinas a medida que entran y salen del tejido. El objetivo de los autores fue reducir la cantidad de DMSO necesaria sin permitir la formación de hielo dañino, haciendo el almacenamiento de células y tejidos hepáticos más seguro y práctico.
Una nueva forma de presionar y enfriar al mismo tiempo
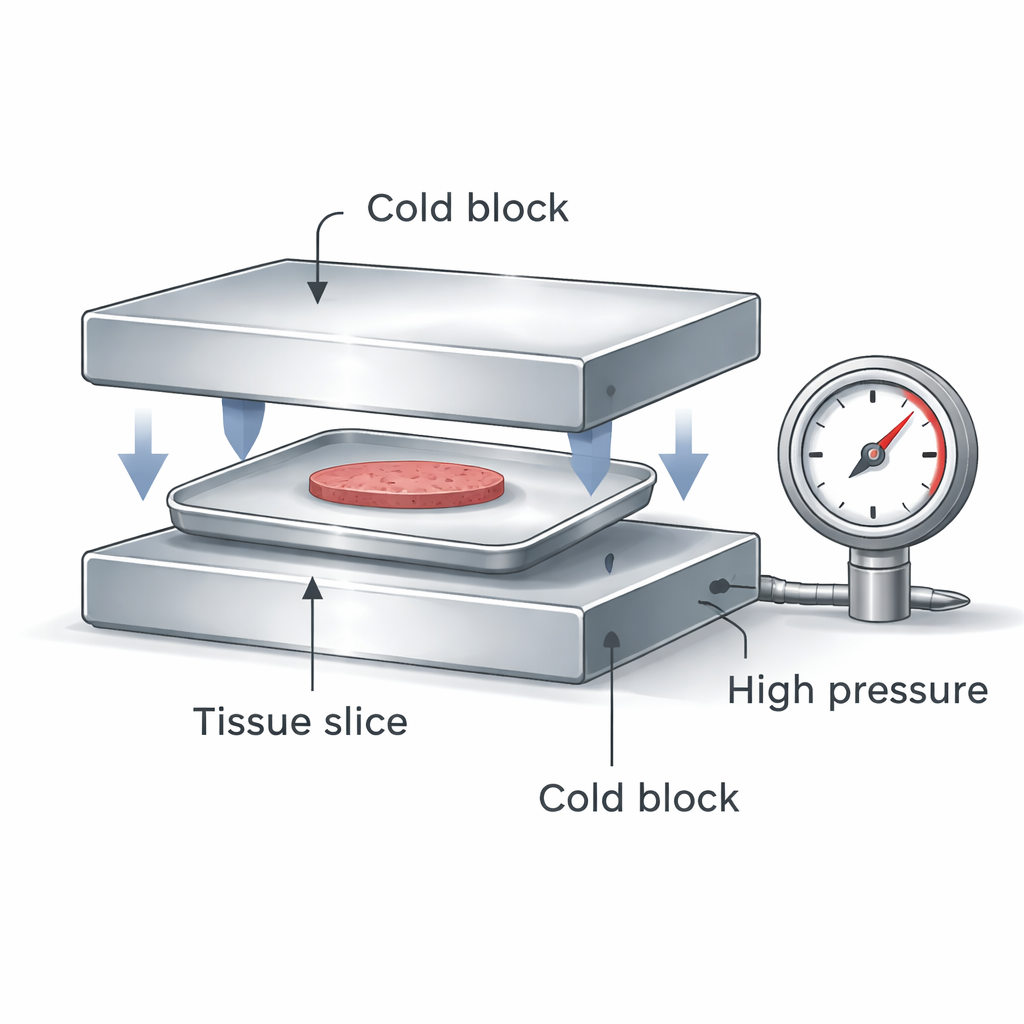
El equipo diseñó un dispositivo compacto que sandwicha un contenedor plano de aluminio sellado, que contiene células hepáticas o cortes precisos de hígado, entre dos bloques metálicos extremadamente fríos. Cuando los bloques se comprimen, realizan dos funciones importantes a la vez: generan alta presión dentro del contenedor sellado y extraen calor de la muestra tanto por la parte superior como por la inferior. La alta presión modifica el comportamiento del agua para que el hielo se forme a temperaturas más bajas y la solución vitrifique con mayor facilidad. El contacto doble proporciona una velocidad de enfriamiento mucho más rápida y uniforme que sumergir un vial de plástico en nitrógeno líquido, y el contenedor sellado mantiene la muestra aislada de la contaminación.
Encontrar el punto óptimo entre seguridad y supervivencia
Para comprobar si este enfoque era lo suficientemente suave para material vivo, los investigadores primero verificaron que el propio contenedor de aluminio no dañara las células HepG2 derivadas del hígado durante los breves tiempos de manipulación utilizados. La supervivencia celular se mantuvo esencialmente sin cambios. A continuación expusieron estas células a distintos niveles de DMSO antes de congelarlas y confirmaron un compromiso ya conocido: más DMSO suprime mejor el hielo pero resulta claramente tóxico al 30%, mientras que el 20% sigue siendo en gran medida tolerable. Para los cortes de hígado de ratón, probaron cuánta presión podía soportar el tejido en ausencia de congelación. Pulsos breves de hasta 150 megapascales tuvieron poco efecto sobre la viabilidad, pero 200 megapascales provocaron aproximadamente una caída del 30%, lo que marca un límite superior para una operación segura.
Cortes hepáticos mejor preservados tras la descongelación
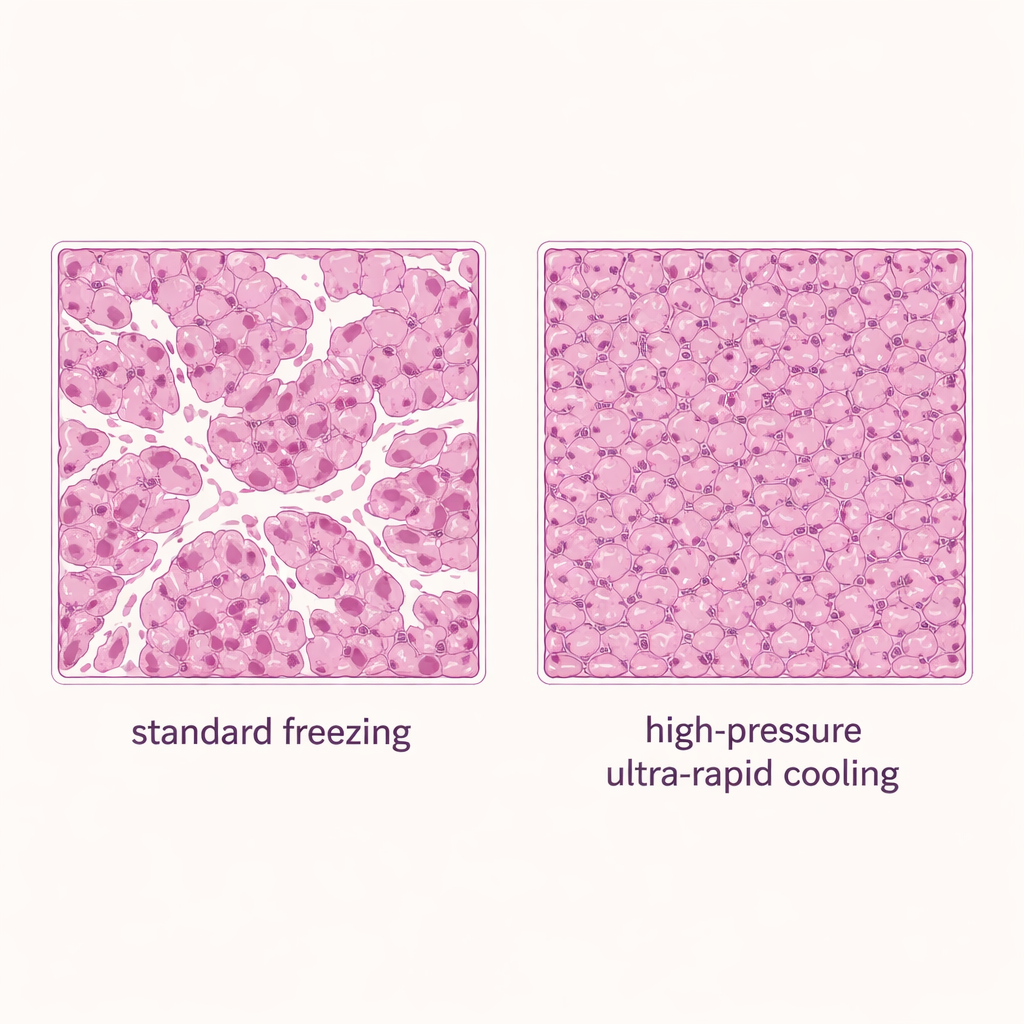
Con los rangos seguros establecidos, los autores compararon tres métodos de congelación para cortes de hígado: inmersión estándar del contenedor sellado en nitrógeno líquido (un enfoque por convección o basado en fluido), enfriamiento en superficie sólida sin presión añadida, y enfriamiento en superficie sólida con alta presión de 150 megapascales. Todos los grupos usaron 20% de DMSO. El método asistido por presión ofreció los mejores resultados: se conservó alrededor del 80% de la viabilidad original del tejido, superando tanto a la congelación estándar como al enfriamiento en superficie sólida por sí solo. La microscopía de cortes teñidos apoyó estos hallazgos. Las muestras congeladas por inmersión convencional mostraron muchos espacios blancos abiertos —firmas del daño por hielo—, mientras que el enfriamiento en superficie sólida mejorado por presión produjo tejido más denso e intacto con muchas menos lagunas.
Qué significa esto para el futuro del almacenamiento de tejidos
En conjunto, el estudio demuestra que apretar un corte de hígado sellado en aluminio entre dos bloques ultrafríos bajo alta presión controlada puede mejorar considerablemente la supervivencia del tejido tras la descongelación. Al combinar un enfriamiento más rápido y homogéneo con la alteración del comportamiento del agua por la presión, el método limita el crecimiento de hielo dañino mientras sigue usando una concentración moderada y clínicamente conocida de DMSO. Para un lector general, la conclusión es que una ingeniería más inteligente—cómo empaquetamos y enfriamos el tejido—puede ser tan importante como los químicos que añadimos. Este enfoque de doble cara y alta presión podría convertirse en un paso hacia un almacenamiento más seguro y fiable de tejido hepático y, eventualmente, de otros órganos para investigación y terapia.
Cita: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Palabras clave: criopreservación, tejido hepático, vitrificación, enfriamiento a alta presión, congelación sin hielo