Clear Sky Science · es
Análisis comparativo de modelos supervisados y ensamblados con exploración no supervisada para la predicción de la enfermedad de Alzheimer
Por qué importa la advertencia temprana
La enfermedad de Alzheimer va robando lentamente a las personas la memoria y la independencia, a menudo mucho antes de que se establezca un diagnóstico firme. Las familias, los médicos y los sistemas de salud salen beneficiados cuando se detectan señales de advertencia de forma temprana, porque es entonces cuando el tratamiento, la planificación y el apoyo pueden marcar la mayor diferencia. Este estudio plantea una pregunta práctica: ¿pueden programas informáticos cuidadosamente diseñados, entrenados con información clínica de uso rutinario y escaneos cerebrales, detectar la demencia con más fiabilidad que las herramientas estándar actuales—y al mismo tiempo revelar patrones ocultos en cómo se desarrolla la enfermedad?
Convertir los historiales de pacientes en señales útiles
Los investigadores recurrieron a una colección de datos conocida como OASIS-2, que sigue a 150 adultos mayores de entre 60 y 96 años durante varios años. Para cada visita, el conjunto de datos incluye información básica como edad, años de escolaridad y nivel socioeconómico, así como puntuaciones en pruebas cognitivas y mediciones derivadas de resonancias magnéticas cerebrales, como el volumen cerebral total. Antes de cualquier predicción, el equipo limpió los datos, eliminó identificadores y casos ambiguos, completó un pequeño número de valores faltantes y normalizó todas las mediciones numéricas en una escala común. También abordaron un problema clave del mundo real: en el conjunto de datos hay muchas más personas sanas que con demencia. Para evitar que los modelos simplemente adivinasen “sin demencia” la mayor parte del tiempo, los investigadores emplearon esquemas de ponderación que hacen que los errores sobre el grupo menor, el de personas con demencia, tengan mayor peso durante el entrenamiento.
Comparando herramientas clásicas con equipos de modelos
Con este conjunto de datos preparado, los autores compararon herramientas familiares de aprendizaje automático con “ensamblados” más avanzados, que combinan varios modelos en un predictor más sólido. El grupo clásico incluyó regresión logística, árboles de decisión, máquinas de vectores de soporte y bosques aleatorios. El grupo de ensamblados presentó AdaBoost, XGBoost y un modelo de voto mayoritario que integró tres clasificadores ajustados. Todos los modelos se entrenaron en una porción de los datos y se probaron en casos retenidos, evaluando el rendimiento mediante la exactitud, la capacidad para detectar correctamente a los individuos con demencia (recall) y el área bajo la curva ROC, un resumen de qué tan bien el modelo separa los casos sanos de los enfermos. 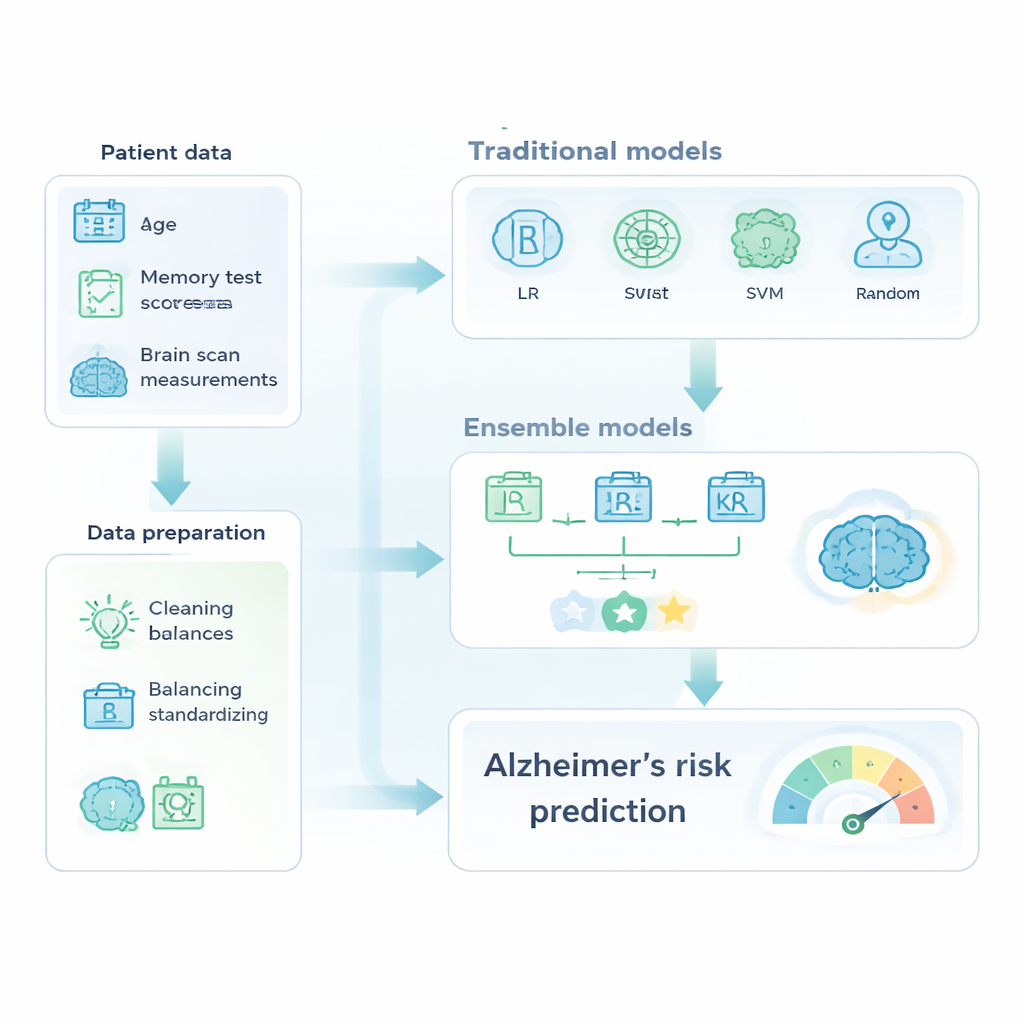
Cuando muchas mentes superan a una
Los resultados cara a cara fueron claros. Si bien los mejores métodos tradicionales funcionaron razonablemente bien, se estabilizaron alrededor de los niveles reportados en estudios previos, con precisiones en pruebas en el rango bajo a medio del 80 por ciento. En contraste, el ensamblado por voto mayoritario alcanzó aproximadamente un 95 por ciento de exactitud y una puntuación ROC igualmente alta, superando el hito comúnmente citado del 92 por ciento. AdaBoost y otros modelos ensamblados también lo hicieron mejor que cualquier modelo tradicional individual. Esta ventaja surge porque distintos algoritmos capturan diferentes aspectos de los datos; al permitirles “votar”, el ensamblado suaviza las peculiaridades y el sobreajuste individuales, conduciendo a predicciones más estables. El precio de esta ganancia es una menor transparencia: resulta más difícil ver, de un vistazo, por qué un ensamblado tomó una decisión concreta en comparación con una regresión simple o un árbol individual. 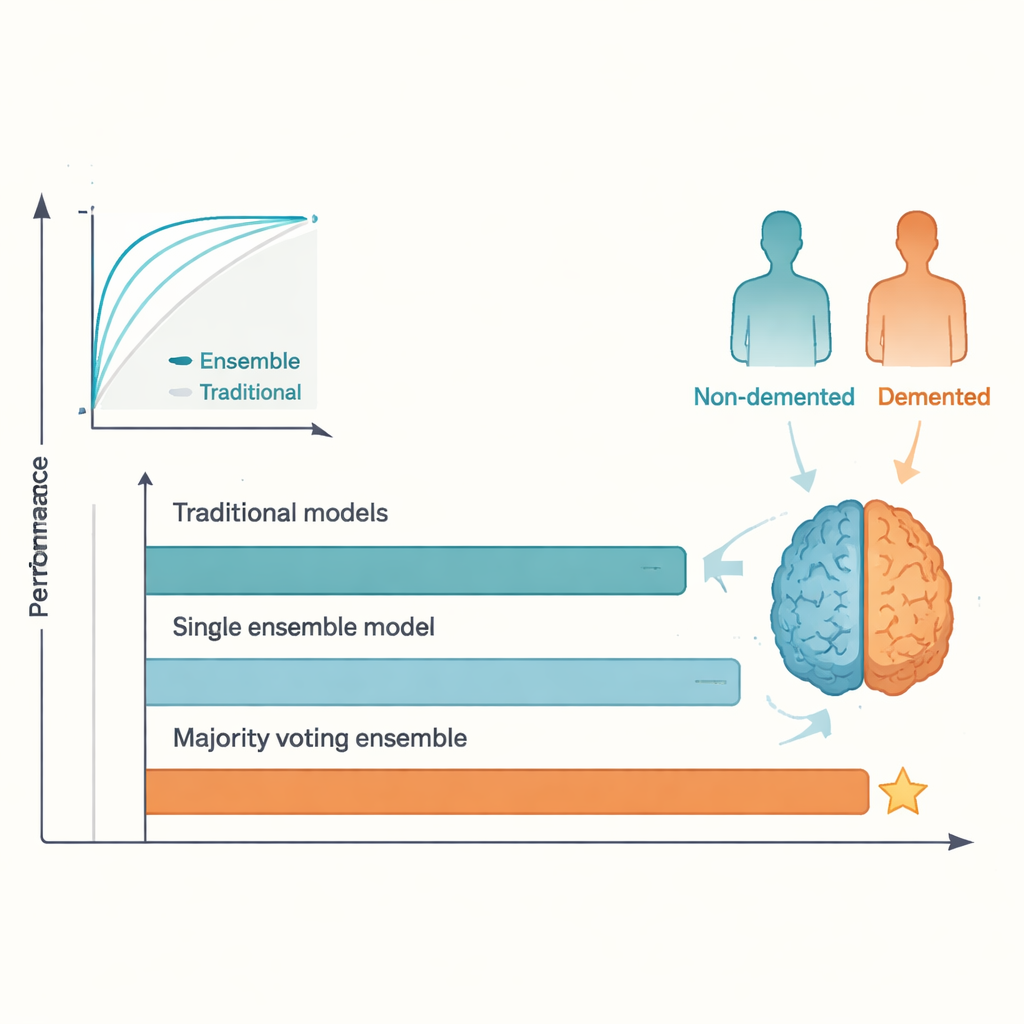
Buscando agrupamientos naturales en los datos
Más allá de preguntar quién tiene demencia, los investigadores también exploraron cómo se agrupan naturalmente los pacientes, independientemente de las etiquetas de diagnóstico. Para ello transformaron todas las variables continuas en categorías ordenadas—como rangos de edad o de volumen cerebral—y aplicaron una técnica llamada análisis de correspondencias múltiples para comprimir esta rica información en unas pocas dimensiones subyacentes. Luego emplearon k-means para particionar esos puntos en un pequeño número de grupos coherentes. Algunos clústeres estuvieron dominados por personas con volumen cerebral preservado y puntuaciones cognitivas normales, mientras que otros agruparon a individuos con bajo volumen cerebral, pobres resultados en las pruebas y calificaciones de demencia más severas. El hecho de que estos clústeres no supervisados concordaran bien con el estado clínico sugiere que los datos contienen una señal fuerte y consistente sobre el riesgo y la progresión de la enfermedad.
Qué significa esto para pacientes y clínicos
Para un lector no especializado, la conclusión es sencilla: cuando se diseñan con cuidado, los equipos de modelos de aprendizaje automático pueden detectar la demencia relacionada con Alzheimer en datos clínicos estructurados con mayor precisión que los métodos antiguos, y pueden hacerlo usando información que muchas clínicas ya recogen. Al mismo tiempo, las técnicas exploratorias muestran que las personas se agrupan en perfiles distintos de salud cerebral y función cognitiva, lo que apunta a diferentes trayectorias que la enfermedad podría seguir. Aunque el estudio está limitado por su tamaño de muestra modesto y por la complejidad de interpretar modelos ensamblados, demuestra que combinar predicción potente con un análisis exploratorio riguroso puede afinar la detección temprana y profundizar nuestra comprensión de cómo se desarrolla el Alzheimer.
Cita: Amr, Y., Gad, W., Leiva, V. et al. Comparative analysis of supervised and ensemble models with unsupervised exploration for alzheimer’s disease prediction. Sci Rep 16, 7322 (2026). https://doi.org/10.1038/s41598-026-37122-9
Palabras clave: Enfermedad de Alzheimer, predicción de demencia, aprendizaje automático, modelos ensamblados, imagen cerebral