Clear Sky Science · es
Identificación de RBX1 como regulador de la transcripción de LIPT1 y su papel en la muerte celular inducida por cobre en células de GBM
Por qué importan el cobre y los tumores cerebrales
El glioblastoma multiforme es una de las formas más mortales de cáncer cerebral; la mayoría de los pacientes sobreviven poco tiempo después del diagnóstico, a pesar de cirugía, radioterapia y quimioterapia agresivas. Este estudio explora un aliado inesperado contra estos tumores: el metal cobre. Los investigadores examinan una forma de muerte celular recientemente reconocida desencadenada por el cobre e identifican una vía molecular que podría ayudar a los médicos a aprovechar este proceso para debilitar los tumores y, potencialmente, potenciar el ataque del sistema inmunitario contra las células cancerosas.
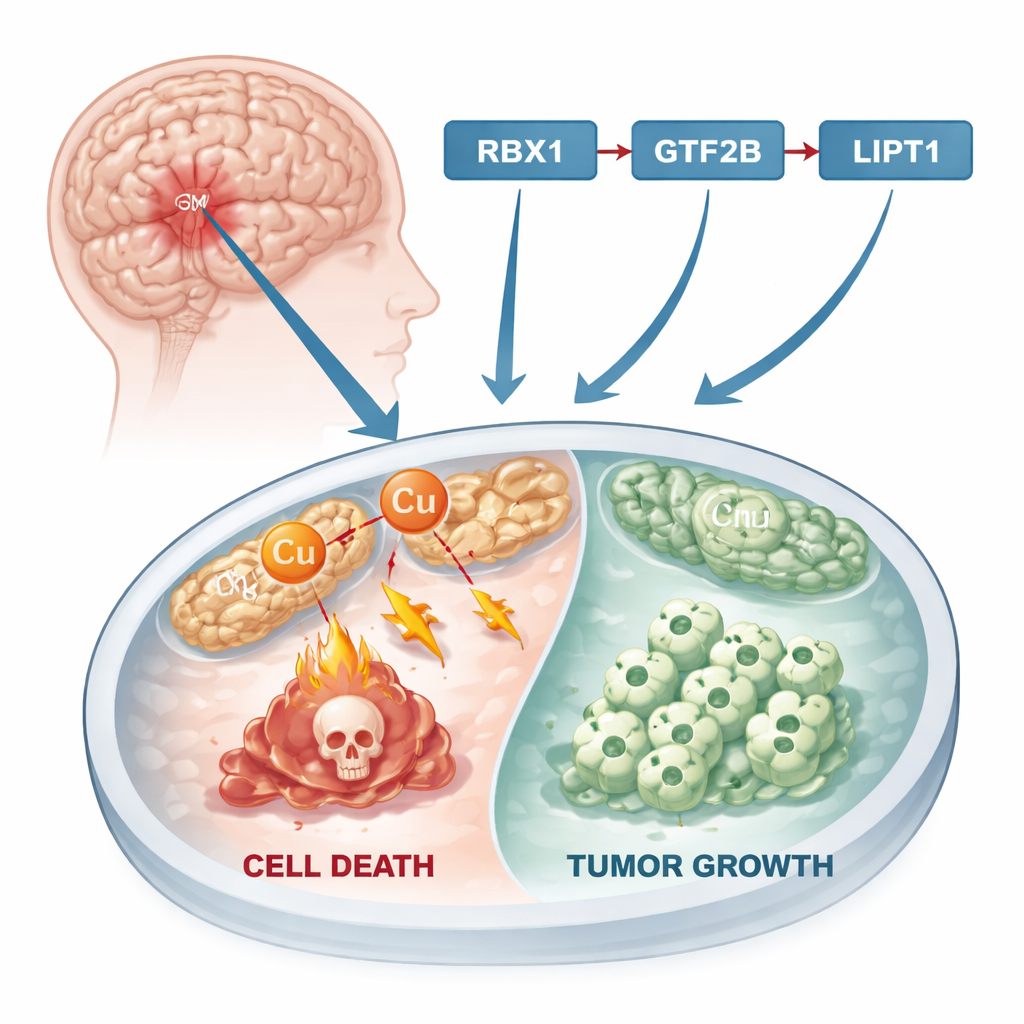
Una nueva vía de muerte celular
Durante décadas, la investigación del cáncer se ha centrado en formas conocidas de muerte celular como la apoptosis, en la que las células dañadas se apagan de forma ordenada. Recientemente, los científicos descubrieron una ruta diferente llamada muerte celular inducida por cobre, o “cuprotosis”. En este proceso, el exceso de cobre se acumula dentro de las centrales energéticas de la célula, las mitocondrias. Allí interfiere con proteínas clave, provocando la formación de agregados tóxicos que acaban matando la célula. Dado que muchos tumores presentan un metabolismo metálico alterado y niveles de cobre más altos que los tejidos normales, la cuprotosis ofrece un posible punto de presión: si los investigadores pueden empujar a las células tumorales hacia esta muerte impulsada por cobre, podrían frenar o detener el crecimiento del cáncer.
Poniendo el foco en un gen clave en glioblastoma
Los autores comenzaron encuestando un grupo de genes ya conocidos por su implicación en la cuprotosis y compararon su comportamiento en muestras de glioblastoma frente a tejido cerebral normal. Un gen en particular, llamado LIPT1, destacó. Presentaba mayor actividad en tejido de glioblastoma y en varias líneas celulares de glioblastoma que en células cerebrales normales. De forma importante, los pacientes cuyos tumores mostraban mayor actividad de LIPT1 tendían a permanecer más tiempo sin recurrencia tras el tratamiento. Niveles altos de LIPT1 también se asociaron con una mayor presencia de células T CD8, los principales agentes citotóxicos del sistema inmunitario contra el cáncer, lo que sugiere que este gen podría contribuir a que el microambiente tumoral sea más vulnerable al ataque inmunitario.
Qué ocurre cuando se atenúa el interruptor de la muerte por cobre
Para probar si LIPT1 afecta realmente a la muerte inducida por cobre, el equipo expuso células de glioblastoma a una combinación farmacológica que transporta cobre y que desencadena de forma fiable la cuprotosis. A continuación utilizaron herramientas genéticas para reducir los niveles de LIPT1. Cuando LIPT1 se suprimió, las células tumorales mostraron mayor resistencia a la muerte inducida por cobre, sobrevivieron mejor y exhibieron mayor capacidad de migración e invasión, comportamientos asociados a un cáncer más agresivo. En cultivos mixtos de células tumorales y células T CD8 humanas, la disminución de LIPT1 también redujo la liberación de moléculas de señalización inmunitaria y dificultó que las células T destruyeran las células cancerosas. En conjunto, estos experimentos indican que LIPT1 aumenta la sensibilidad a la muerte inducida por cobre y favorece la actividad inmunitaria antitumoral.
Rastreando la cadena de mando hasta RBX1
El siguiente reto fue entender por qué LIPT1 está elevado en glioblastoma. Combinando varias bases de datos grandes de genes y proteínas, los investigadores identificaron un factor de transcripción —una especie de interruptor maestro de la actividad génica— llamado GTF2B que se une cerca del gen LIPT1 y probablemente potencia su expresión. Luego investigaron qué controla a GTF2B. Emergiu como fuerte candidato una segunda proteína, RBX1. RBX1 forma parte del sistema celular de etiquetado y eliminación que marca a otras proteínas para su degradación. En células de glioblastoma, los niveles de RBX1 eran menores que en células cerebrales normales, mientras que GTF2B y LIPT1 eran más altos. Ensayos de laboratorio mostraron que RBX1 puede añadir pequeñas etiquetas de “destrúyeme” a GTF2B, conduciendo a su degradación; cuando RBX1 aumentó, los niveles de GTF2B y la actividad de LIPT1 disminuyeron, y bloquear la maquinaria de degradación celular revirtió este efecto.
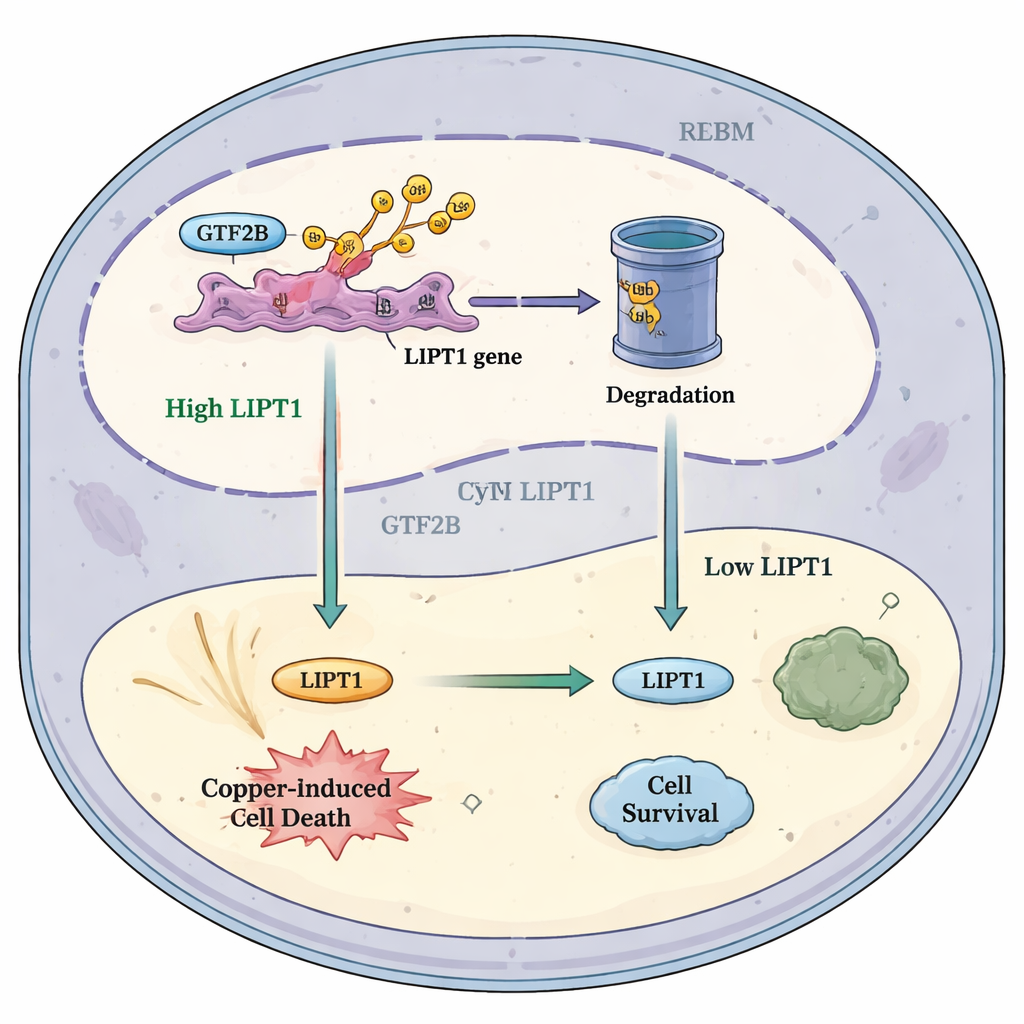
Cómo podría ayudar esta vía a futuros tratamientos
Integrando estos hallazgos, los autores proponen un modelo simple: en condiciones sanas, RBX1 mantiene a GTF2B bajo control, limitando cuánto activa el gen LIPT1. En el glioblastoma, la reducción de RBX1 implica que menos GTF2B se degrade. El exceso de GTF2B potencia LIPT1, aumentando la sensibilidad de las células tumorales a la muerte inducida por cobre y atrayendo a más células inmunitarias que combaten el cáncer. Este modelo sugiere que ajustar con cuidado la vía RBX1–GTF2B–LIPT1, posiblemente junto con fármacos dirigidos al cobre e inmunoterapias, podría inclinar la balanza dentro de los tumores cerebrales hacia la autodestrucción. Aunque queda mucho trabajo antes de que esta idea llegue a los pacientes, el estudio destaca una intersección prometedora entre la biología de los metales, la regulación génica y la inmunología del cáncer que podría abrir nuevas vías terapéuticas para uno de los cánceres más resistentes.
Cita: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Palabras clave: glioblastoma, muerte celular inducida por cobre, LIPT1, inmunología tumoral, vía RBX1