Clear Sky Science · es
MCT1 como regulador crítico de la señalización de la insulina, la homeostasis energética y la función de los podocitos
Por qué importan las elecciones de combustible de las células renales
Nuestros riñones filtran silenciosamente cientos de litros de sangre cada día, y gran parte de ese trabajo depende de unas células diminutas llamadas podocitos que envuelven los filtros renales. Estas células deben remodelarse constantemente para mantener las proteínas en la sangre y los desechos en la orina. Este estudio explora cómo obtienen energía los podocitos, qué ocurre cuando se bloquea una de sus principales “puertas de combustible” y por qué eso podría importar en afecciones comunes como la diabetes y la enfermedad renal. 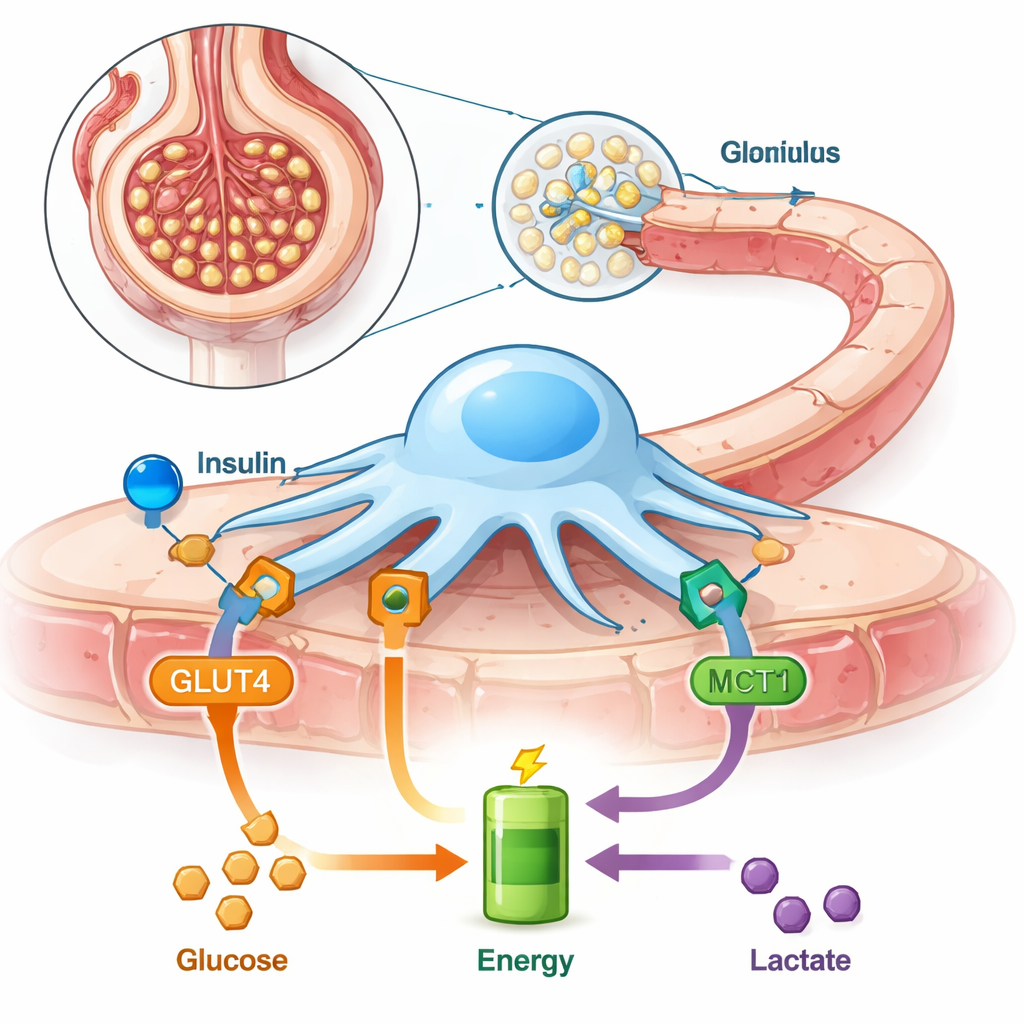
Células guardianas en el filtro
Los podocitos se sitúan en el lado externo de cada filtro renal, extendiendo delicadas prolongaciones en forma de pies que se entrelazan para formar una barrera final antes de que se produzca la orina. Debido a que están siempre ajustando su forma, consumen mucha energía. A diferencia de muchas otras células, los podocitos dependen en gran medida de la degradación de la glucosa sin oxígeno (una vía llamada glucólisis) y son especialmente sensibles a la insulina, que les indica captar más glucosa de la sangre a través de un transportador llamado GLUT4. Los autores habían mostrado previamente que los podocitos también pueden usar lactato como combustible, una pequeña molécula a menudo descartada como “residuo”, lo que sugiere que estas células son más flexibles de lo que se pensaba.
La puerta del lactato: MCT1
El lactato entra y sale de las células a través de proteínas transportadoras específicas. Una de las más importantes es el transportador de monocarboxilatos 1 (MCT1), que puede llevar lactato hacia el interior de las células para que se queme como energía. En este estudio, los investigadores emplearon podocitos de rata cultivados en placa y bloquearon MCT1 con un inhibidor químico. Después preguntaron cómo afectaba esto a la capacidad de la insulina para impulsar la captación de glucosa, cuánta energía podían generar las células, cómo quedaba su armazón interno y cuánto se volvía “permeable” el filtro a una gran proteína sanguínea llamada albúmina. También probaron filtros renales completos de ratas (glomérulos aislados) para ver cómo el lactato y el bloqueo de MCT1 cambiaban la fuga de proteínas en un sistema más intacto.
Cuando la puerta de combustible se cierra
Bloquear MCT1 produjo varios efectos llamativos. Primero, redujo la captación de glucosa por los podocitos, tanto en condiciones basales como tras la estimulación con insulina, y debilitó un interruptor clave en la vía de la insulina (una proteína llamada Akt) sin alterar el receptor de insulina en sí. Al mismo tiempo, el desplazamiento normal del transportador GLUT4 hacia la superficie celular quedó atenuado. Las mediciones del metabolismo celular mostraron que la producción total de energía disminuyó cuando se bloqueó MCT1, y las células cambiaron su balance alejándose de la glucólisis hacia una quema más dependiente del oxígeno en las mitocondrias. Incluso al añadir insulina o lactato, ese déficit energético no se corrigió por completo, lo que sugiere que MCT1 es central para cómo los podocitos equilibran sus fuentes de energía. 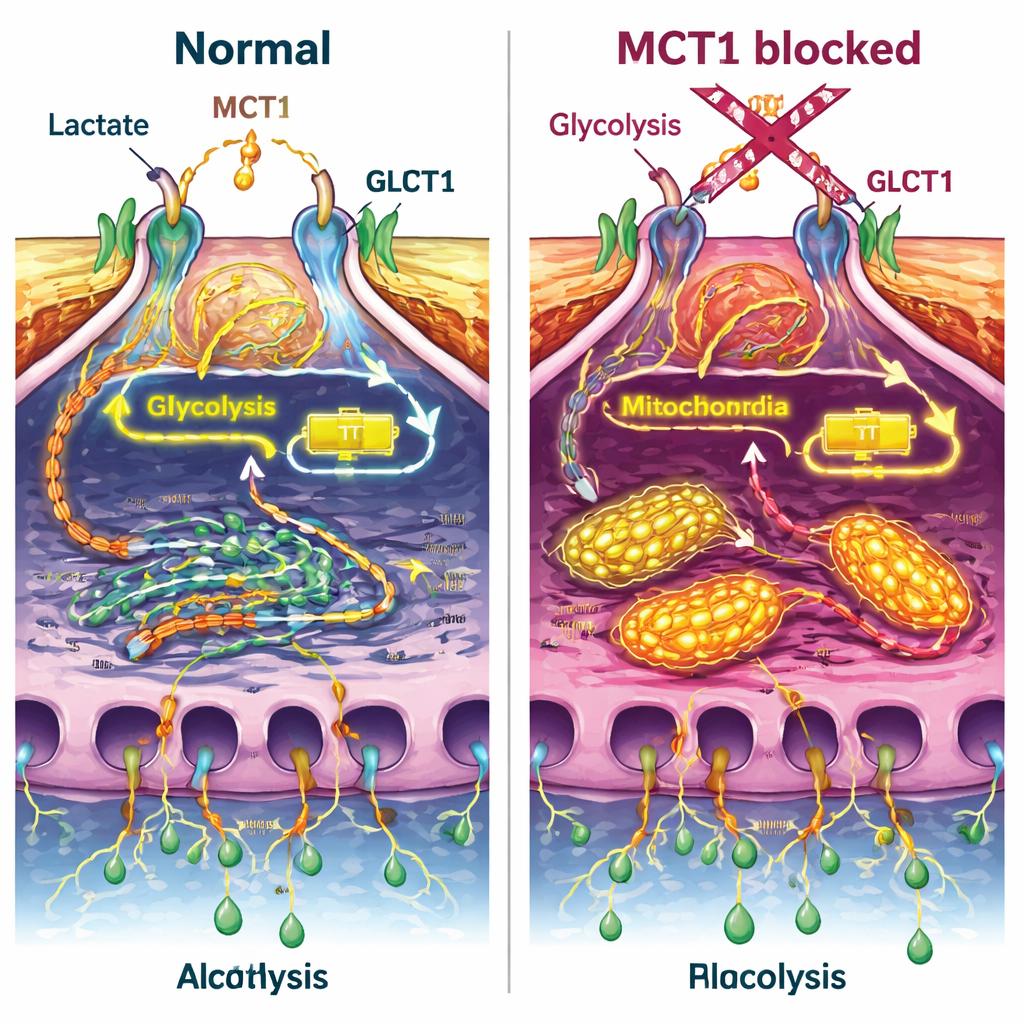
Filtros permeables y andamiajes estresados
Los cambios energéticos estuvieron estrechamente ligados al daño físico. Cuando se bloqueó MCT1, las capas de podocitos en cultivo dejaron pasar más albúmina, un efecto similar al de la insulina por sí sola. El propio lactato también aumentó la permeabilidad de la barrera, y combinar lactato o insulina con el bloqueo de MCT1 mantuvo la alta permeabilidad. Dentro de las células, las fibras de actina que forman su estructura se agruparon y desorganizaron, un patrón asociado con la pérdida de los finos procesos pediculares que conforman el filtro. Otra proteína clave, la nefina, que ayuda a mantener unido el filtro y también apoya las acciones de la insulina, se redujo o se localizó incorrectamente cuando se inhibió MCT1. En filtros completos aislados de riñones de rata, la adición de lactato aumentó rápidamente la fuga de albúmina, y el bloqueo de MCT1 produjo un aumento similar, apoyando la idea de que el manejo alterado del lactato debilita directamente el filtro.
Implicaciones para la diabetes y la salud renal
Los autores proponen que el correcto movimiento del lactato a través de MCT1 es esencial para que los podocitos mantengan su programa energético preferido, respondan a la insulina y conserven una barrera de filtración hermética. Cuando esta “puerta” del lactato se ve alterada —por el bloqueo de MCT1 o por una hiperglucemia crónica que modifica el equilibrio del lactato—, los podocitos pierden flexibilidad metabólica, consumen menos glucosa, dependen en exceso de las mitocondrias y se vuelven estructuralmente inestables y permeables. Para las personas, este trabajo sugiere que cambios sutiles en cómo las células renales manejan el lactato pueden contribuir a la resistencia a la insulina y al daño renal temprano mucho antes de que la función renal global parezca anormal. Comprender y, en última instancia, dirigir este sistema de transporte de lactato podría abrir nuevas vías para proteger los filtros renales en la diabetes y otras enfermedades metabólicas.
Cita: Szrejder, M., Audzeyenka, I., Rachubik, P. et al. MCT1 as a critical regulator of insulin signaling, energy homeostasis and podocyte function. Sci Rep 16, 5906 (2026). https://doi.org/10.1038/s41598-026-37093-x
Palabras clave: podocitos renales, metabolismo del lactato, resistencia a la insulina, barrera de filtración glomerular, transportador MCT1