Clear Sky Science · es
Cuantificación automatizada de linfocitos infiltrantes de tumor mediante aprendizaje automático revela características pronósticas e inmunogenómicas en cáncer de pulmón
Por qué importa contar pequeñas células inmunitarias en tumores pulmonares
El cáncer de pulmón sigue siendo uno de los más letales, pero no todos los tumores se comportan igual. Algunos están fuertemente patrullados por células inmunitarias que se infiltran en el tumor, mientras que otros permanecen casi intactos. Estos linfocitos infiltrantes de tumor, o TILs, pueden indicar cómo le irá a un paciente y si podría beneficiarse de los fármacos inmunoterapéuticos modernos. El problema es que hoy en día los TILs suelen contarse a simple vista bajo el microscopio, lo cual es lento y subjetivo. Este estudio plantea una pregunta actual: ¿podemos usar aprendizaje automático para medir automáticamente estas células en los cortes de rutina, y qué revela eso sobre la biología del cáncer de pulmón y la supervivencia de los pacientes?
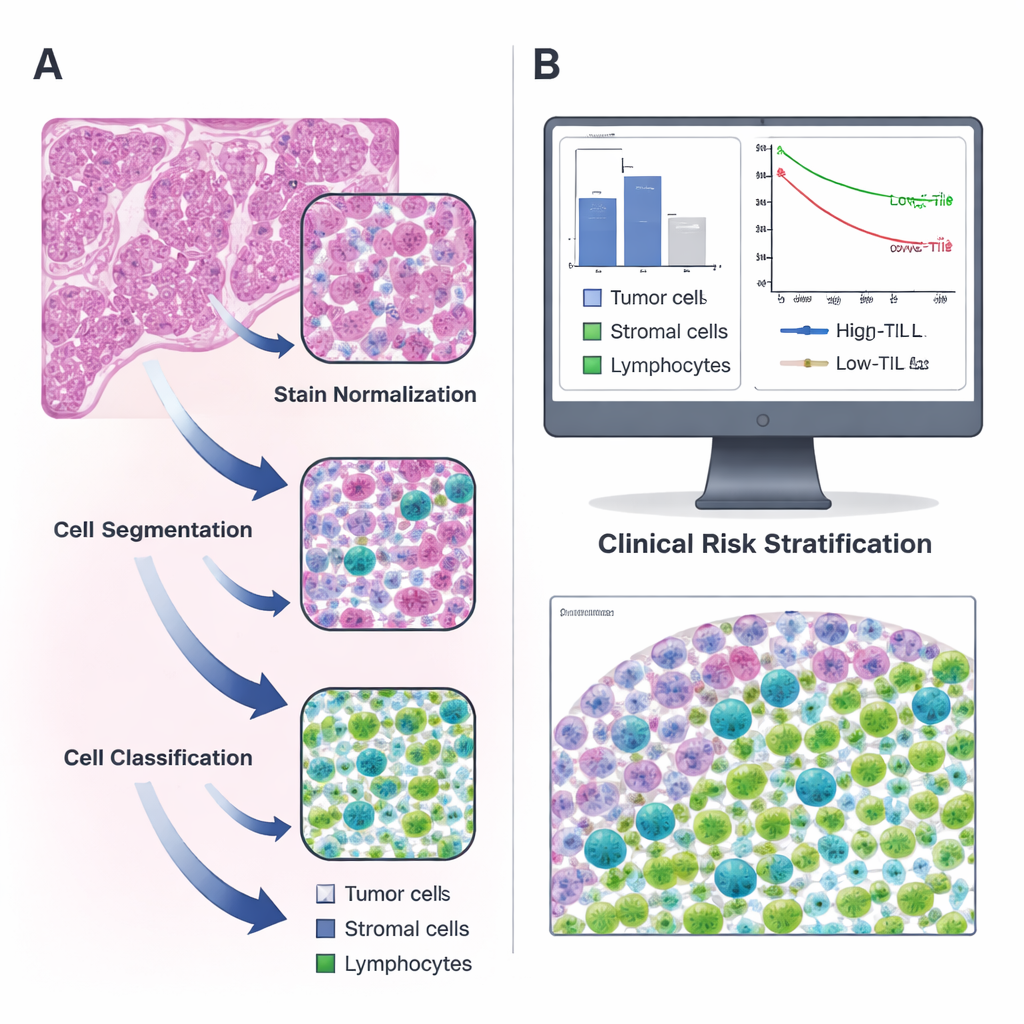
Convertir cortes ordinarios en mapas digitales
Los investigadores se centraron en el adenocarcinoma de pulmón, un tipo común de cáncer pulmonar, usando datos públicos de The Cancer Genome Atlas junto con un conjunto independiente de pacientes de su propio hospital. Para cada paciente analizaron los cortes tisulares estándar teñidos con hematoxilina y eosina (H&E), las imágenes rosa y púrpura que todo patólogo conoce bien. Con el software de código abierto QuPath, construyeron una canalización por pasos: primero corrigieron diferencias de color entre los cortes; a continuación usaron un algoritmo de watershed para separar núcleos celulares solapados; finalmente, un clasificador entrenado etiquetó cada célula detectada como tumor, tejido de sostén (estroma) o linfocito. Dos patólogos expertos revisaron y corrigieron repetidamente el trabajo de la máquina hasta que reconocía de forma fiable los distintos tipos celulares por sí sola.
Vincular el recuento de células inmunitarias con los resultados de los pacientes
Una vez que el sistema pudo identificar células con confianza, el equipo calculó cuántos linfocitos había por milímetro cuadrado de tejido tumoral en más de 300 pacientes. Encontraron que los niveles de TIL variaban ampliamente y que, en promedio, constituían solo una pequeña fracción de todas las células. Usando un enfoque estadístico para encontrar el punto de corte más informativo, eligieron 135 TIL por milímetro cuadrado como la línea divisoria entre tumores con TIL “altos” y “bajos”. Los pacientes cuyos tumores superaban este umbral vivieron más que aquellos con infiltración inmunitaria escasa, y este patrón se mantuvo tanto en el grupo original como en el de validación. En otras palabras, un número simple producido por una herramienta automatizada capturó diferencias significativas en la supervivencia, confirmando estudios anteriores más laboriosos que se basaron en recuentos manuales.
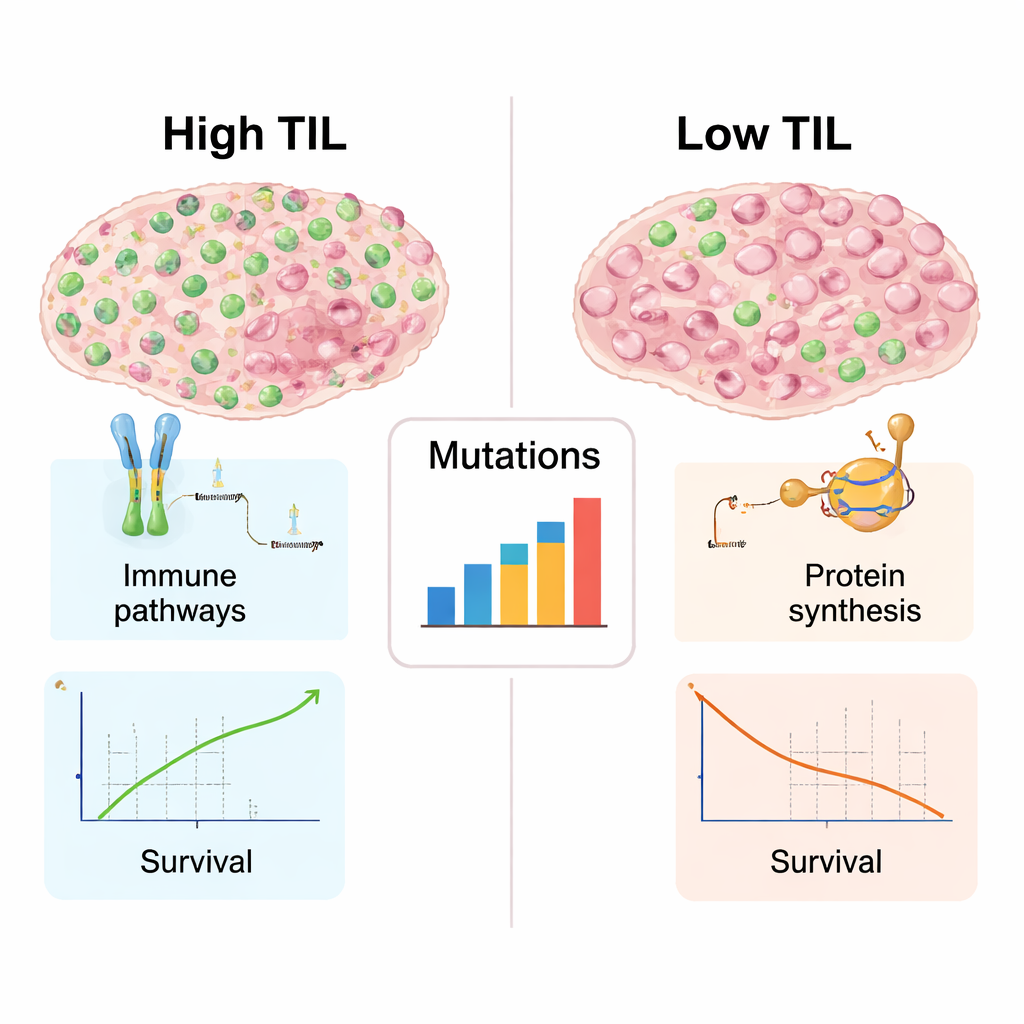
Cómo son por dentro los tumores ricos en inmunidad
Debido a que había datos genéticos y moleculares disponibles para muchos de estos tumores, los autores pudieron explorar qué distinguía a los cánceres con TIL altos de los de TIL bajos más allá de los simples recuentos celulares. Los tumores rebosantes de linfocitos mostraron firmas más claras de actividad inmune: genes implicados en reconocer proteínas anómalas, presentarlas a las células T y coordinar el ataque inmune estaban todos más activos. Además, estos tumores presentaban una mezcla más amplia de mutaciones en el ADN, que pueden generar nuevos objetivos para el sistema inmunitario. En contraste, los tumores con TIL bajos favorecían genes relacionados con la construcción de ribosomas y la síntesis de proteínas, un signo de maquinaria de crecimiento intensiva pero de una participación inmune relativamente tranquila. Esta división refleja el ya familiar contraste entre tumores “calientes”, ricos en células inmunitarias y más propensos a responder a la inmunoterapia, y tumores “fríos”, que el sistema inmunitario suele ignorar.
Enseñar a un ordenador a predecir el estado inmunitario
El equipo fue un paso más allá y se preguntó si un conjunto compacto de características de imagen podría predecir si un tumor pertenecería a la categoría de TIL alto o bajo sin contar explícitamente cada linfocito. Resumieron patrones texturales sutiles en los cortes —cómo cambian las intensidades de píxel en pequeños vecindarios— en las denominadas características de Haralick, y las combinaron con el estadio clínico del tumor en un modelo de bosque aleatorio. En validación cruzada, este clasificador separó correctamente tumores con TIL altos de los de TIL bajos con gran precisión, y conservó un rendimiento razonable en la cohorte hospitalaria independiente. Es importante destacar que todo el enfoque funciona en ordenadores estándar usando software libre, lo que sugiere que muchos laboratorios de patología podrían, en principio, adoptarlo sin hardware especializado.
Qué significa esto para la atención futura del cáncer de pulmón
Para un no especialista, el mensaje clave es que un ordenador puede aprender a leer cortes rutinarios de cáncer de pulmón de una forma que captura cuán intensamente el sistema inmunitario se ha implicado con el tumor. Niveles altos de linfocitos infiltrantes señalan una batalla inmune más activa, un paisaje de mutaciones más rico y una mejor supervivencia global. Aunque se necesita más trabajo —especialmente en pacientes tratados con inmunoterapia—, este método automatizado podría, con el tiempo, ayudar a los médicos a clasificar los tumores en las categorías inmunitarias “calientes” y “frías” de forma rápida y consistente. Eso, a su vez, podría guiar decisiones sobre quién es más probable que se beneficie de tratamientos basados en el sistema inmunitario y fomentar nuevas estrategias para convertir tumores fríos en calientes.
Cita: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Palabras clave: adenocarcinoma de pulmón, linfocitos infiltrantes de tumor, aprendizaje automático, patología digital, inmunoterapia contra el cáncer