Clear Sky Science · es
Diagnóstico automatizado de la forma Plus y de las etapas iniciales de la ROP mediante modelos de aprendizaje profundo
Por qué importan los ojos diminutos y las computadoras inteligentes
Cada año, miles de recién nacidos prematuros corren el riesgo de perder la vista porque los vasos sanguíneos en la parte posterior de sus ojos no se desarrollan normalmente, una afección llamada retinopatía del prematuro (ROP). Detectar este problema de forma temprana puede salvar la visión, pero exige exámenes oculares frecuentes realizados por especialistas altamente cualificados, profesionales que escasean en muchas regiones del mundo. Este estudio explora cómo la inteligencia artificial (IA) moderna puede ayudar a los médicos a detectar señales de alarma tempranas en fotografías retinianas, con lo que potencialmente se podría llevar cribado de nivel experto a hospitales y clínicas que carecen de especialistas en oftalmología.
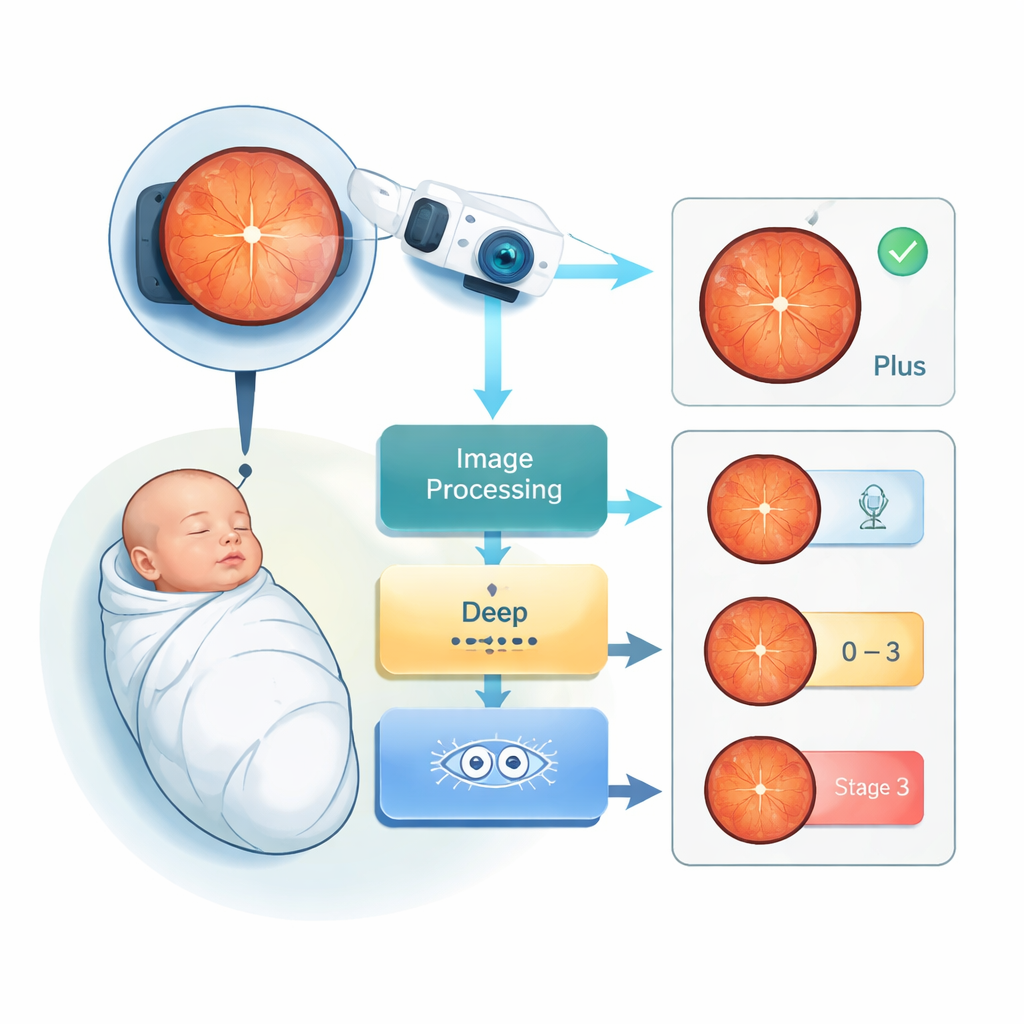
El problema: visión frágil en los pacientes más pequeños
La ROP se desarrolla cuando el nacimiento prematuro interrumpe el crecimiento normal de los vasos sanguíneos en la retina, la capa fotosensible en la parte posterior del ojo. Los bebés que nacen muy prematuros o con muy bajo peso presentan el mayor riesgo. En los casos leves, el ojo se recupera por sí solo. En los casos graves, los vasos anormales pueden tirar de la retina y provocar ceguera permanente. En todo el mundo, se estima que la ROP causa ceguera en unas 50.000 personas, especialmente en regiones donde la mejora de la atención neonatal ha aumentado la supervivencia pero los programas de cribado ocular y los especialistas no han seguido el ritmo. El cribado actual es laborioso, costoso y subjetivo: a veces dos expertos discrepan sobre la gravedad real de la enfermedad en un bebé.
Lo que buscan los médicos: vasos retorcidos y etapas iniciales
Los oftalmólogos evalúan la ROP basándose en dos indicadores principales en las imágenes de la retina. Uno es la etapa general de la enfermedad, desde la Etapa 0 (sin cambios visibles) hasta las etapas problemáticas tempranas (1–3). El otro es la «Plus disease», una señal de advertencia en la que los vasos sanguíneos de la retina se dilatan y retuercen de forma inusual. La Plus disease indica un mayor riesgo de daño grave y suele desencadenar tratamientos como la terapia láser o inyecciones de fármacos. Evaluar estas características a simple vista es un desafío, especialmente cuando las imágenes están borrosas o cuando los bebés requieren exámenes repetidos semana tras semana. Un sistema capaz de señalar automáticamente la Plus disease y estimar la etapa de la ROP solo a partir de imágenes sería una herramienta de gran ayuda para los clínicos.
Cómo ve la IA: trazado de mapas vasculares a partir de fotos oculares
Los investigadores construyeron una canalización de IA en dos pasos usando más de 6.000 imágenes retinianas procedentes de 188 lactantes. Primero, entrenaron una red neuronal para dibujar un «mapa de vasos» preciso de cada retina, destacando cada vaso visible, incluso las ramas más finas. Entre varios modelos de procesamiento de imágenes competidores, una versión llamada U-Net++ funcionó mejor para capturar patrones vasculares detallados, especialmente en imágenes ruidosas o con bajo contraste. Para mejorar la claridad, el equipo realzó cada foto con filtros de aumento de contraste y reducción de ruido antes de la segmentación. Para la detección de Plus disease, a continuación alimentaron solo los mapas de vasos —no las fotos en color completas— a una segunda red neuronal, porque la Plus disease se define casi enteramente por el grosor y la curvatura de los vasos.
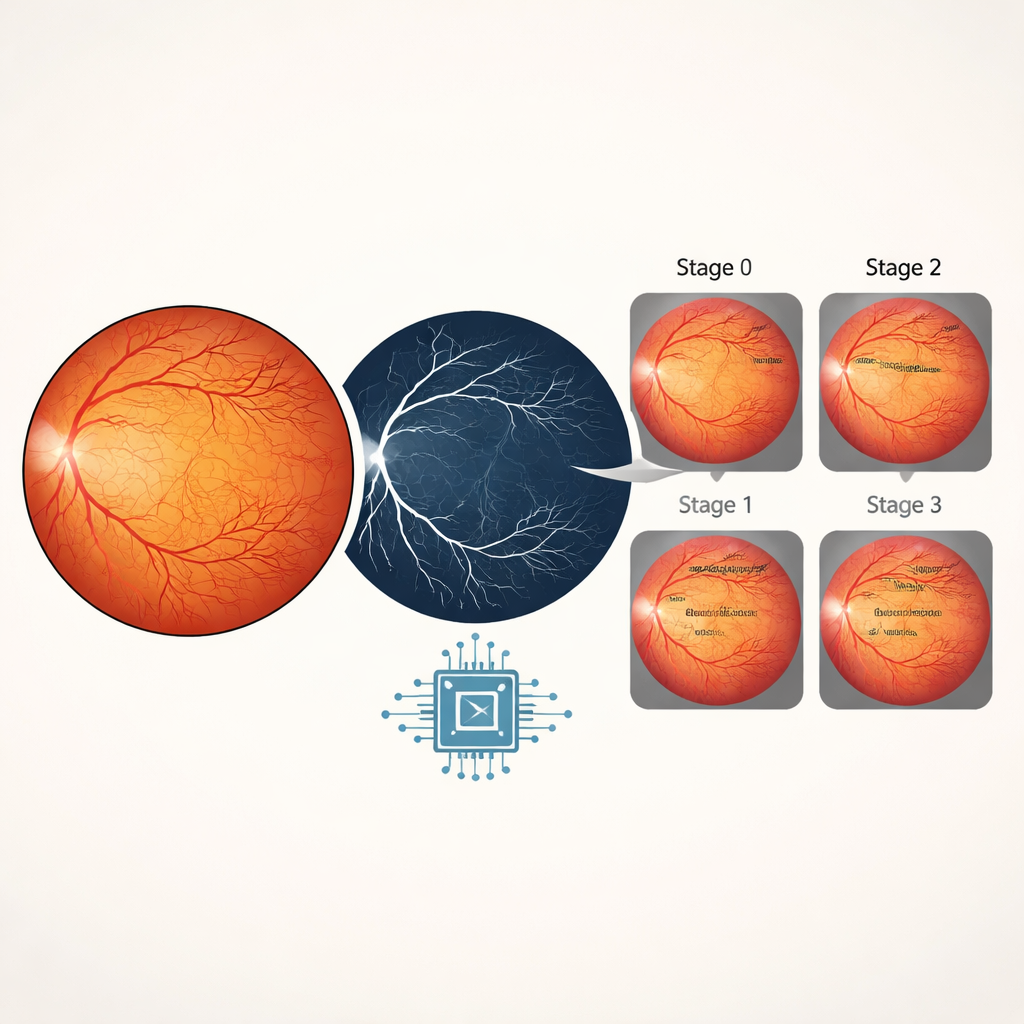
Enseñar a la red a calificar la gravedad de la enfermedad
Para juzgar la etapa de la ROP, la IA necesitaba algo más que la forma de los vasos sanguíneos. Por eso, el sistema combinó las imágenes retinianas en color originales con sus mapas de vasos correspondientes, proporcionando al modelo tanto la vista general de la retina como una visión afinada de sus vasos. El equipo probó varias arquitecturas de aprendizaje profundo conocidas y descubrió que un modelo llamado EfficientNetB4 ofrecía el mejor equilibrio entre precisión y eficiencia. En imágenes de validación retenidas, el detector de Plus disease alcanzó una precisión del 99,6 por ciento, mientras que el clasificador de etapas logró un 98 por ciento de precisión en las Etapas 0 a 3. Comprobaciones adicionales, incluidas curvas de precisión‑recuperación y curvas ROC, mostraron que el modelo mantenía alta sensibilidad (rara vez pasaba por alto la enfermedad) y alta especificidad (rara vez generaba falsas alarmas), aun cuando la Plus disease era mucho más rara que las imágenes normales.
Mirando dentro de la «caja negra»
Dado que los clínicos deben confiar en cualquier herramienta que influya en decisiones de tratamiento, los autores investigaron cómo la IA tomaba sus decisiones. Usando métodos de visualización como t‑SNE, mostraron que las imágenes de distintas clases (por ejemplo, Plus frente a Normal o Etapa 1 frente a Etapa 3) formaban clústeres bien separados en el espacio de características interno del modelo. Con técnicas de mapas de calor llamadas Grad‑CAM, destacaron qué partes de cada retina influían más en una predicción. Para la Plus disease, el modelo se centró en áreas donde los vasos eran anormalmente anchos o retorcidos, coincidiendo con lo que buscan los expertos. Para la clasificación de la etapa, también prestó atención a otras regiones como el disco óptico y la mácula, lo que sugiere que su razonamiento se alineó estrechamente con criterios médicos establecidos en lugar de con artefactos espurios de la imagen.
Qué significa esto para los bebés y las clínicas
En términos sencillos, este trabajo demuestra que un sistema de IA cuidadosamente diseñado puede leer imágenes retinianas de bebés prematuros con una precisión cercana a la de un experto, tanto para detectar cambios vasculares peligrosos como para juzgar hasta qué punto ha avanzado la enfermedad. El estudio se llevó a cabo en un único centro médico e incluyó solo etapas de leves a moderadas, por lo que aún se necesitan ensayos más amplios en varios hospitales y datos de casos más avanzados. Sin embargo, los resultados sugieren que, con una validación adicional e integración cuidadosa en plataformas de telemedicina, tales herramientas podrían ayudar a sistemas de salud sobrecargados a cribar a muchos más lactantes, de forma más consistente y a menor coste. Eso podría traducirse en tratamientos más tempranos y una mayor probabilidad de preservar la visión de algunos de los pacientes más vulnerables en la atención neonatal.
Cita: Vahidmoghadam, M., Ghorbani, P., Ahmadi, M.J. et al. Automated diagnosis of plus form and early stages of ROP using deep learning models. Sci Rep 16, 7234 (2026). https://doi.org/10.1038/s41598-026-37064-2
Palabras clave: retinopatía del prematuro, inteligencia artificial, aprendizaje profundo, imagen médica, enfermedad ocular neonatal