Clear Sky Science · es
Investigación sobre el mecanismo molecular de celastrol dirigido a CTNNB1/STAT3 para inhibir el melanoma uveal basada en farmacología de redes y análisis multi-ómico
Medicina ancestral frente al cáncer ocular
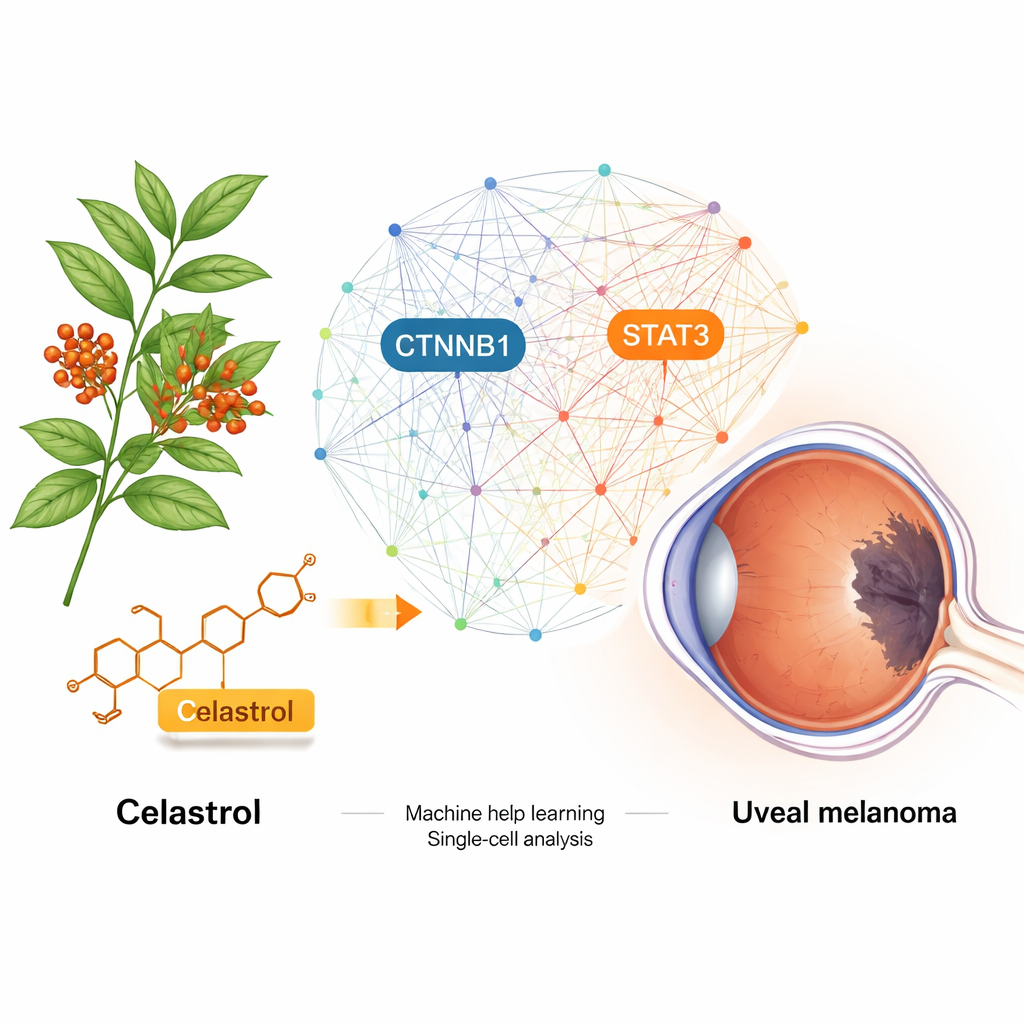
El melanoma uveal es un cáncer raro pero letal que se origina dentro del ojo. Una vez que hace metástasis, los tratamientos actuales apenas modifican el pronóstico. Este estudio explora si el celastrol —una molécula extraída de una planta utilizada en la medicina tradicional china— podría reutilizarse para combatir este cáncer. Combinando biología de grandes datos, simulaciones por ordenador y experimentos de laboratorio, los investigadores desvelan cómo el celastrol podría desactivar conmutadores moleculares clave que ayudan al melanoma uveal a crecer y diseminarse.
Qué hace que este tumor ocular sea tan peligroso
El melanoma uveal es el cáncer primario del ojo más frecuente en adultos, y aproximadamente la mitad de los pacientes desarrolla finalmente metástasis, por lo general en el hígado. En esa fase, la supervivencia suele medirse en meses. Los tratamientos estándar, como la cirugía, la radiación y las terapias locales, pueden controlar el tumor principal en el ojo, pero los fármacos sistémicos han tenido un éxito limitado y pueden causar efectos secundarios graves. Por ello, los científicos buscan medicamentos que frenen el crecimiento tumoral y sean mejor tolerados, un campo donde los productos naturales como el celastrol despiertan gran interés.
Un compuesto natural bajo la lupa
El celastrol procede de Tripterygium wilfordii, una planta utilizada desde hace tiempo en la medicina tradicional china. Trabajos previos mostraron que puede frenar el crecimiento de varios cánceres, pero su actuación en el melanoma uveal no estaba clara. El equipo comenzó explorando numerosas bases de datos biomédicas para predecir a qué proteínas humanas podría unirse el celastrol y qué proteínas están fuertemente relacionadas con el melanoma uveal. Al comparar ambas listas, identificaron 46 candidatos solapados. Usando herramientas informáticas que mapean cómo interactúan las proteínas entre sí, redujeron esa lista a un puñado de moléculas “hub” que se sitúan en puntos de control de las principales vías de crecimiento y supervivencia en las células tumorales.
Enfocándose en dos interruptores maestros
Para identificar a los actores más críticos, los investigadores combinaron datos genómicos de tumores de pacientes del Atlas del Genoma del Cáncer con tres métodos distintos de aprendizaje automático. Los tres enfoques convergieron en dos genes: CTNNB1, una pieza central de la vía de señalización Wnt que impulsa el crecimiento celular, y STAT3, un regulador clave de la inflamación, la supervivencia y la evasión inmune. Análisis adicionales de muestras tumorales agrupadas y de secuenciación de ARN a células individuales mostraron que estos genes están muy activos en las células del melanoma uveal, especialmente en subgrupos celulares más agresivos, y se asocian con cambios en las células inmunitarias circundantes. En resumen, CTNNB1 y STAT3 parecían interruptores maestros que ayudan al cáncer a prosperar mientras mantienen a raya al sistema inmunitario.
De modelos por ordenador a células vivas
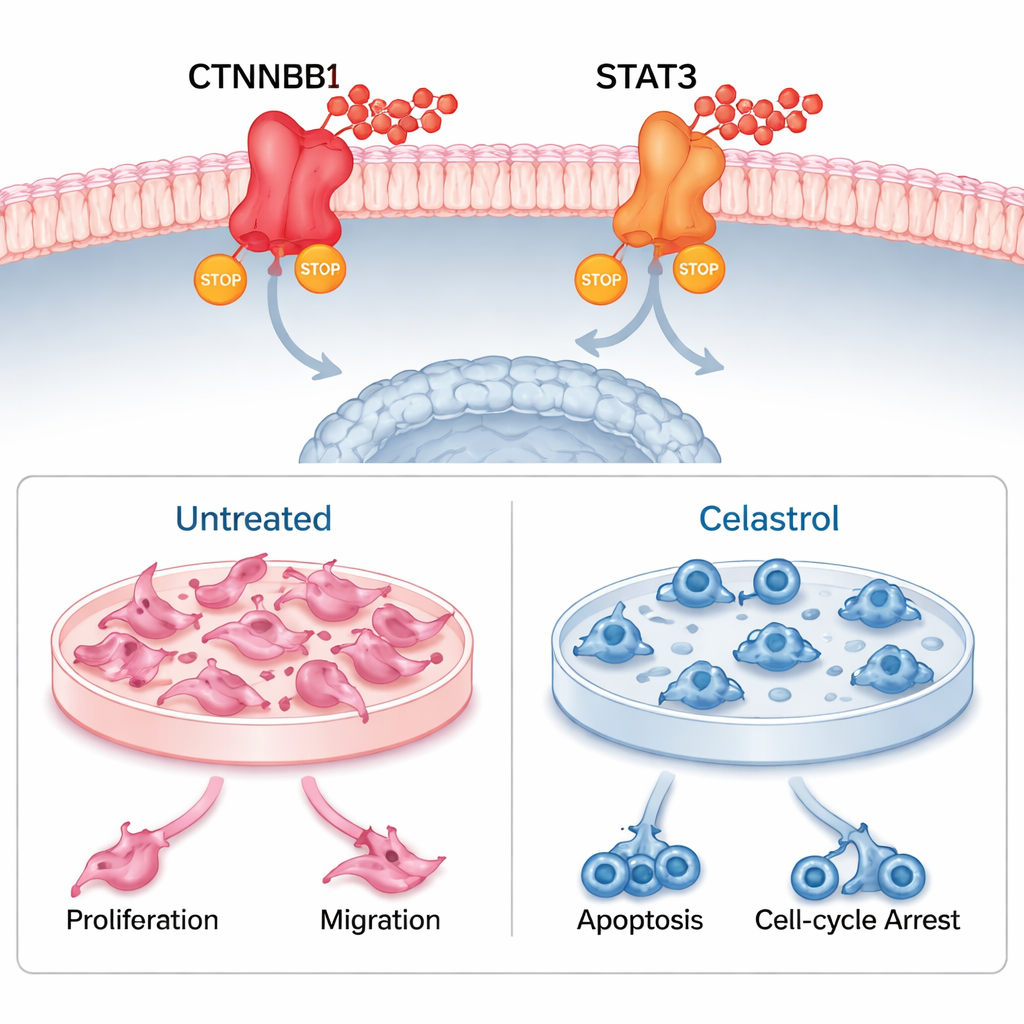
El equipo empleó entonces acoplamiento molecular y simulaciones extensas de dinámica molecular para probar si el celastrol podía unirse físicamente a CTNNB1 y STAT3. Los experimentos virtuales sugirieron una unión fuerte y estable, sostenida por múltiples enlaces de hidrógeno y un empaquetamiento estrecho alrededor del fármaco. A continuación, pasaron al laboratorio, tratando células humanas de melanoma uveal y una línea celular de melanoma de ratón relacionada con celastrol. En ambos casos, el celastrol redujo drásticamente la supervivencia celular y la formación de colonias, ralentizó la migración en ensayos de cicatrización de heridas y desencadenó la muerte celular programada. También provocó que las células se detuvieran en puntos específicos del ciclo celular, impidiendo su división. Al medir la actividad génica y los niveles de proteína, observaron que el celastrol disminuía notablemente CTNNB1 y STAT3, confirmando que alcanza sus dianas previstas dentro de células vivas.
Qué podría significar esto para tratamientos futuros
En conjunto, los resultados sugieren que el celastrol combate el melanoma uveal al inhibir simultáneamente CTNNB1 y STAT3. Esta acción dual no solo ralentiza el crecimiento y la diseminación tumoral, sino que también podría remodelar el microambiente inmunológico del tumor de formas que favorezcan una respuesta antitumoral. Aunque este trabajo se realizó en células y modelos computacionales —aún no en pacientes ni en modelos animales—, sienta una base sólida para pruebas adicionales. Para el lector general, el mensaje clave es que un compuesto con raíces en la medicina tradicional ha surgido como un candidato científicamente plausible para una nueva clase de tratamientos contra el cáncer ocular, que atacan tanto al tumor como al ecosistema celular que lo rodea.
Cita: Li, Z., Xi, R., Han, X. et al. Research on the molecular mechanism of celastrol targeting CTNNB1/STAT3 to inhibit uveal melanoma based on network pharmacology and multi-omics analysis. Sci Rep 16, 6140 (2026). https://doi.org/10.1038/s41598-026-37061-5
Palabras clave: melanoma uveal, celastrol, cáncer ocular, señalización del cáncer, microambiente tumoral