Clear Sky Science · es
Desarrollo y evaluación preliminar de ensayos de PCR en tiempo real para seis bacterias lácticas
Microbios beneficiosos detrás de los alimentos cotidianos
Muchos de los alimentos que vemos en los supermercados —desde el yogur y el queso hasta los encurtidos y las verduras fermentadas— deben su sabor y sus posibles beneficios para la salud a bacterias amistosas conocidas como probióticos. Pero para aprovechar estas “buenas bacterias” de forma segura y fiable, las empresas deben estar absolutamente seguras de qué especies bacterianas están realmente presentes en sus productos. Este estudio describe nuevas pruebas de laboratorio que pueden identificar rápida y precisamente seis bacterias probióticas prometedoras utilizadas en alimentos, ayudando a cerrar la brecha entre la microbiología de vanguardia y los alimentos que consumimos a diario.
Por qué importan estas bacterias probióticas
Las seis bacterias en el centro de este trabajo pertenecen a un grupo más amplio llamado bacterias lácticas, utilizadas desde hace tiempo en fermentaciones. Investigaciones recientes sugieren que pueden hacer mucho más que acidificar la leche o la col. Algunas cepas de Ligilactobacillus agilis y Ligilactobacillus salivarius podrían ayudar a combatir gérmenes intestinales perjudiciales, reducir la inflamación y apoyar la integridad de la barrera intestinal. Limosilactobacillus fermentum se ha asociado en estudios en animales con mejor control de la presión arterial y efectos antioxidantes. Lactobacillus johnsonii parece ayudar a equilibrar la microbiota intestinal de formas que podrían proteger diversos órganos. Pediococcus pentosaceus y Weissella cibaria muestran potencial para reducir el colesterol, combatir el deterioro microbiológico e incluso favorecer la salud bucal. Con una gama tan amplia de beneficios potenciales, la industria alimentaria está interesada en usar estas especies más ampliamente, pero solo si pueden identificarse con confianza.
El reto de distinguir microbios que se parecen entre sí
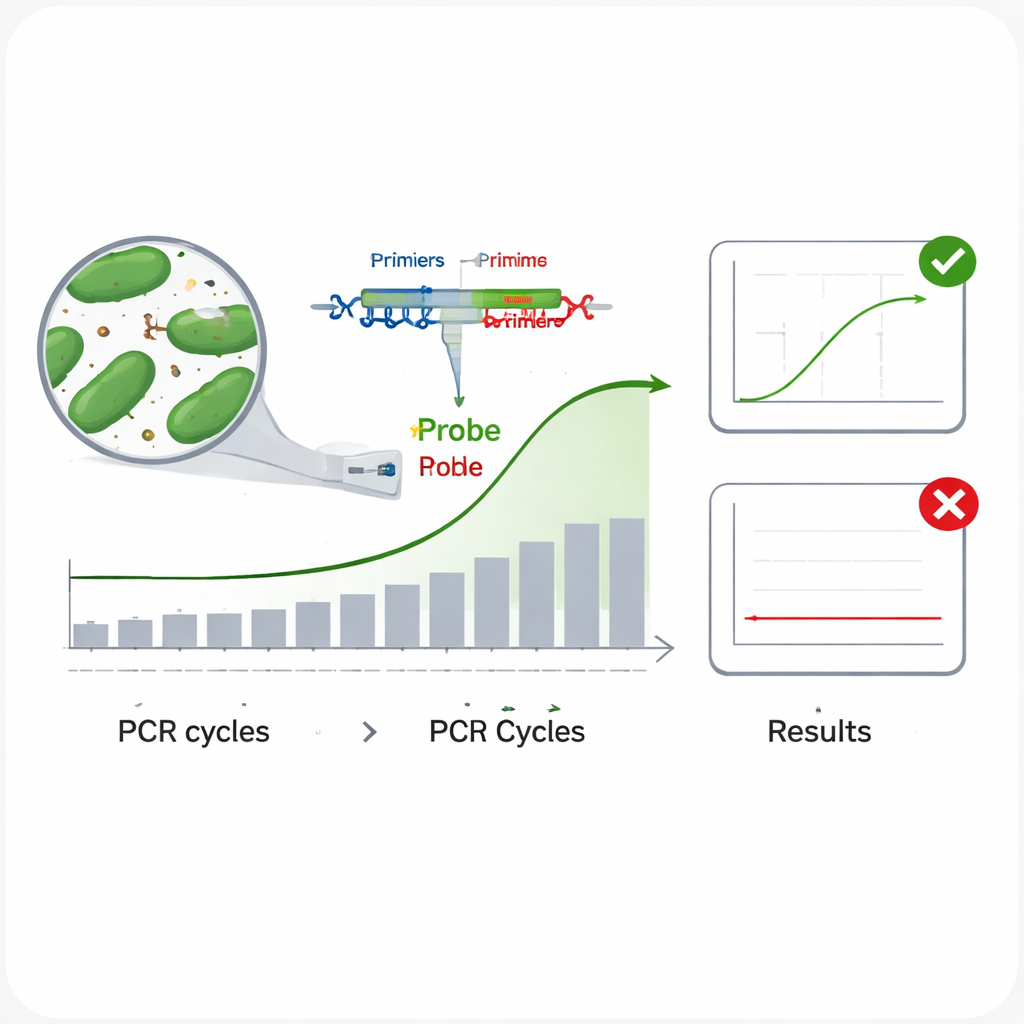
Los métodos tradicionales para identificar bacterias —hacerlas crecer en el laboratorio y realizar pruebas bioquímicas— son lentos y laboriosos. Los métodos modernos basados en ADN, especialmente la PCR en tiempo real, son mucho más rápidos. En la PCR en tiempo real, fragmentos cortos de ADN llamados cebadores y una sonda fluorescente se dirigen a un tramo único del código genético de un microbio; cuando está presente el microbio correcto, la máquina detecta una señal luminosa a medida que el ADN se copia ciclo tras ciclo. El problema es que bacterias estrechamente relacionadas pueden compartir ADN muy similar, por lo que regiones genéticas comúnmente usadas, como el gen 16S rRNA, a veces no distinguen una especie de otra. Eso puede dar lugar a pruebas que no detectan el objetivo (falsos negativos) o que reaccionan ante la especie equivocada (falsos positivos), ambos inaceptables para el etiquetado y la seguridad del producto.
Diseñando “códigos de barras” moleculares más precisos
Para solucionar esto, los investigadores revisaron secuencias genómicas completas en busca de regiones de ADN cortas que fuesen altamente conservadas dentro de cada especie objetivo y claramente diferentes de otras bacterias. Para cada una de las seis probióticas, diseñaron un conjunto de cebadores y una sonda con longitudes, composición de bases, temperaturas de fusión y una mínima propensión a formar estructuras secundarias o unirse entre sí cuidadosamente ajustadas. Comprobaciones informáticas usando la base de datos BLAST y programas de alineamiento de secuencias confirmaron que las regiones de ADN seleccionadas eran estables dentro de la especie y distintas frente a no‑objetivos. El equipo también desarrolló una mezcla de reacción estándar y un programa de calentamiento para que todos los ensayos pudieran correr en condiciones consistentes y prácticas en el mismo tipo de termociclador de PCR en tiempo real.
Poniendo las nuevas pruebas a prueba
Los científicos evaluaron a continuación el rendimiento de cada ensayo en la práctica. Para probar la inclusividad—si un ensayo puede detectar muchas cepas diferentes de la misma especie—ejecutaron cada ensayo con múltiples muestras de ADN de su bacteria objetivo. En todos los casos, todas las cepas ensayadas produjeron una curva de amplificación clara, lo que sugiere un bajo riesgo de dejar pasar objetivos verdaderos. Para comprobar la especificidad—si el ensayo ignora especies no objetivo—desafiaron cada prueba con ADN de 13 otras bacterias intestinales, incluidas bacterias lácticas relacionadas y microbios intestinales comunes como Escherichia coli. Ninguna de ellas produjo señal, lo que indica un riesgo muy bajo de falsas alarmas. El equipo también examinó la eficiencia de amplificación realizando una serie de diluciones en diez veces del ADN y confirmó que los seis ensayos copiaban sus objetivos con una eficiencia aproximada del 95–100%, cercana a lo ideal. Finalmente, midieron la precisión repitiendo ejecuciones a dos niveles de ADN y encontraron que las pequeñas variaciones entre repeticiones y entre experimentos independientes se mantuvieron muy por debajo de los límites aceptados.
Qué significa esto para los alimentos del futuro
En términos simples, los autores han desarrollado seis ensayos de huella genética de ADN finamente afinados que pueden distinguir especies probióticas clave de forma rápida, precisa y fiable. Aunque advierten que se necesita un muestreo más amplio con más cepas, más especies no objetivo y otros instrumentos de PCR antes de su adopción industrial rutinaria, los resultados iniciales son prometedores. Para los consumidores, avances como este ayudan a garantizar que los alimentos anunciados como conteniendo probióticos específicos realmente contengan los microbios correctos, favoreciendo así un etiquetado honesto, un mejor control de calidad y una investigación más fiable sobre cómo estos diminutos socios afectan a nuestra salud.
Cita: Li, SJ., Cui, B., Li, W. et al. Development and preliminary evaluation of real-time PCR assays for six lactic acid bacteria. Sci Rep 16, 6165 (2026). https://doi.org/10.1038/s41598-026-37047-3
Palabras clave: probióticos, bacterias lácticas, PCR en tiempo real, microbiología alimentaria, identificación microbiana