Clear Sky Science · es
Posibles biomarcadores de la inflamación periodontal temprana: investigación de células B CD5+, citocinas salivales y microbioma oral
Por qué tus encías importan para todo el cuerpo
Las encías sangrantes son fáciles de ignorar, pero la inflamación subyacente puede erosionar silenciosamente el hueso que sostiene los dientes y está relacionada con enfermedades del corazón, diabetes y otras dolencias. Este estudio se planteó si señales de alarma tempranas de ese daño pueden encontrarse en una muestra cotidiana: la saliva, junto con ciertas células inmunitarias en la sangre y la mezcla de bacterias que se esconden bajo la línea de las encías. Encontrar marcadores tempranos fiables podría ayudar a los dentistas a identificar pacientes de alto riesgo mucho antes de que ocurra una pérdida dental irreversible.
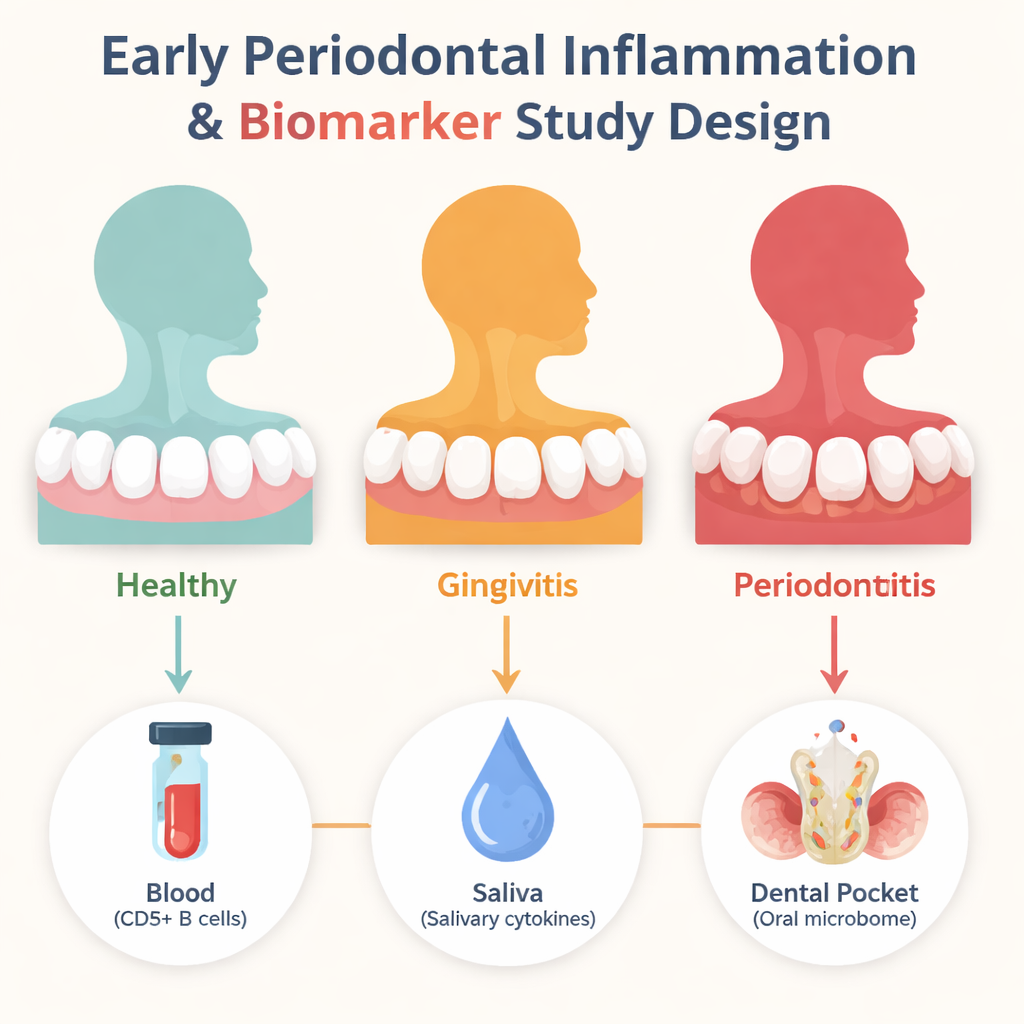
Buscando las primeras señales de advertencia
Los investigadores se centraron en tres tipos de pistas. Primero, examinaron un grupo especial de células inmunitarias en la sangre llamadas células B CD5-positivas, que en enfermedades graves de las encías y en artritis reumatoide se han vinculado con la destrucción ósea y ataques inmunitarios dirigidos al propio organismo. Segundo, midieron docenas de proteínas señalizadoras, o citocinas, en la saliva que actúan como alarmas químicas cuando los tejidos están irritados. Tercero, secuenciaron ADN bacteriano de líquido extraído de bolsas periodontales para ver cómo cambia el microbioma oral conforme la salud cede ante la gingivitis y luego ante la periodontitis moderada. Sesenta adultos no fumadores fueron agrupados cuidadosamente como sanos, con gingivitis o con periodontitis crónica moderada según la profundidad gingival, el sangrado y los índices de placa.
Las células inmunitarias en sangre permanecen silenciosas
Dado el trabajo anterior en enfermedad avanzada, el equipo esperaba que las personas con periodontitis ya mostraran niveles elevados de células B CD5-positivas en la circulación, señalando una reacción generalizada a la infección crónica de las encías. Sorprendentemente, los recuentos totales de estas células fueron esencialmente iguales en los tres grupos, rondando aproximadamente una quinta parte de todas las células B. Incluso cuando los científicos las desglosaron por etapas de desarrollo—inmaduras, naïve y varios tipos de células de memoria—ningún patrón claro alcanzó significación estadística. Algunas células de memoria, especialmente las vinculadas a respuestas de larga duración, tendieron a estar en menor número en las personas con enfermedad, lo que insinúa que podrían estar saliendo de la sangre para acumularse en el tejido gingival inflamado, pero serán necesarios estudios mayores para confirmar esta tendencia sutil.
La saliva y las bacterias cuentan una historia más contundente
En contraste, la saliva y la comunidad bacteriana bajo las encías reflejaron claramente la etapa de la enfermedad. Las personas con periodontitis presentaron aproximadamente el doble del nivel medio de la quimiocina IL-8 en saliva en comparación con participantes sanos o con gingivitis, y tenían muchas más probabilidades de presentar IL-17A detectable así como señales de actividad de IL-6 e IL-1β. Estas moléculas ayudan a reclutar células inmunitarias y a impulsar procesos de reabsorción ósea, por lo que su aumento sugiere que los circuitos inflamatorios ya están activos incluso en enfermedad moderada. Al mismo tiempo, la secuenciación de ADN mostró que las bocas sanas estaban dominadas por bacterias inofensivas y aeróbicas como Rothia y Streptococcus. Con gingivitis y, sobre todo, con periodontitis, el equilibrio se desplazó hacia especies gramnegativas y tolerantes a la falta de oxígeno, incluidas Tannerella, Fusobacterium, Treponema y Fretibacterium, que son culpables conocidos o emergentes en la destrucción gingival.
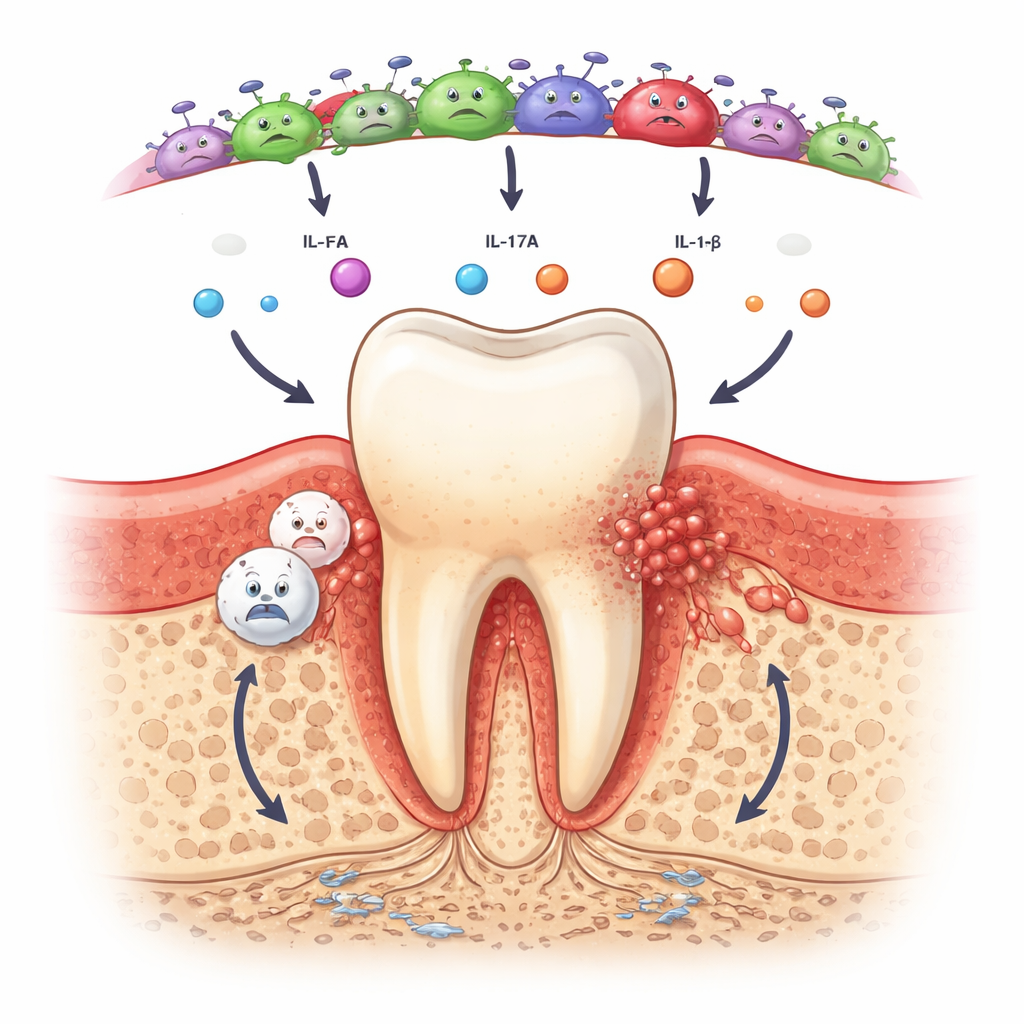
Primeras señales de una firma de alto riesgo
Combinando estadística y aprendizaje automático, el equipo identificó grupos bacterianos que mejor separaban sitios sanos de enfermos. Dos cepas de Tannerella forsythia y varias especies de Fretibacterium surgieron como particularmente informativas, mientras que una especie de Rothia señalaba encías más sanas. Un hallazgo intrigante provino del grupo con gingivitis: los niveles de IL-8 en saliva se correlacionaron estrechamente con la abundancia de un género bacteriano llamado Megasphaera. Este vínculo no apareció en bocas sanas ni en la periodontitis avanzada, lo que sugiere que Megasphaera junto con IL-8 podría actuar como un indicador en etapa temprana mientras el daño aún es limitado y potencialmente reversible. Sin embargo, el tamaño de la muestra fue modesto y los autores subrayan que tales patrones deben probarse en estudios más grandes y a largo plazo antes de poder guiar la atención clínica.
Qué significa esto para los pacientes
Para las personas preocupadas por sus encías, la conclusión es que el organismo sí envía señales bioquímicas tempranas de problema, pero estas aparecen más en la saliva local y en las bacterias gingivales que en las células inmunitarias circulantes cuando la enfermedad aún es moderada. Las pruebas sanguíneas rutinarias de células B CD5-positivas difícilmente identificarán una periodontitis temprana. En su lugar, el enfoque más prometedor podría ser un panel combinado de saliva y microbioma que monitorice varias citocinas—especialmente IL-8 e IL-17A—junto con especies bacterianas clave como Tannerella, Fretibacterium y Megasphaera. Si se valida, una prueba tan sencilla basada en la boca podría ayudar a los dentistas a detectar pacientes de alto riesgo antes, adaptar limpiezas y terapias, y quizá prevenir tanto la pérdida dental como algunos de los problemas de salud más amplios vinculados a la inflamación crónica de las encías.
Cita: Gottschalk, E.C., Chabanovska, O., Vasudevan, P. et al. Potential biomarkers for early periodontal inflammation: investigating CD5+ B cells, salivary cytokines and oral microbiome. Sci Rep 16, 7192 (2026). https://doi.org/10.1038/s41598-026-37044-6
Palabras clave: enfermedad de las encías, microbioma oral, biomarcadores salivales, periodontitis, inflamación