Clear Sky Science · es
Predicción, con aprendizaje automático, de la transformación hemorrágica tras trombectomía usando DSA cuantitativa
Por qué importa esto para los pacientes con ictus
Cuando alguien sufre un ictus mayor, a veces los médicos pueden extraer el coágulo de la arteria principal del cerebro mediante un pequeño dispositivo en un procedimiento llamado trombectomía mecánica. Esto ha transformado la atención del ictus, pero muchos pacientes siguen evolucionando mal después porque algunos desarrollan un nuevo sangrado en el cerebro. El estudio detrás de este artículo plantea una pregunta sencilla pero crucial: ¿podemos usar la información que los médicos ya registran en quirófano, junto con técnicas modernas de aprendizaje automático, para predecir qué pacientes tienen más probabilidades de sangrar y precisar protección adicional?
Más allá de “arteria abierta o cerrada”
Hoy en día, el éxito tras una trombectomía suele juzgarse por si la arteria bloqueada vuelve a verse abierta en la angiografía, una especie de película de rayos X en tiempo real de los vasos sanguíneos. Pero esa valoración tosca no revela lo que ocurre en los pequeños vasos aguas abajo del cerebro, donde realmente se producen el daño y el sangrado. Algunos pacientes con una reapertura de grandes vasos aparentemente perfecta terminan desarrollando una hemorragia cerebral grave, una complicación llamada transformación hemorrágica. Los autores sospecharon que mediciones más detalladas del flujo sanguíneo en esos pequeños vasos, extraídas de la misma angiografía, podrían contener pistas ocultas sobre quién está en riesgo.
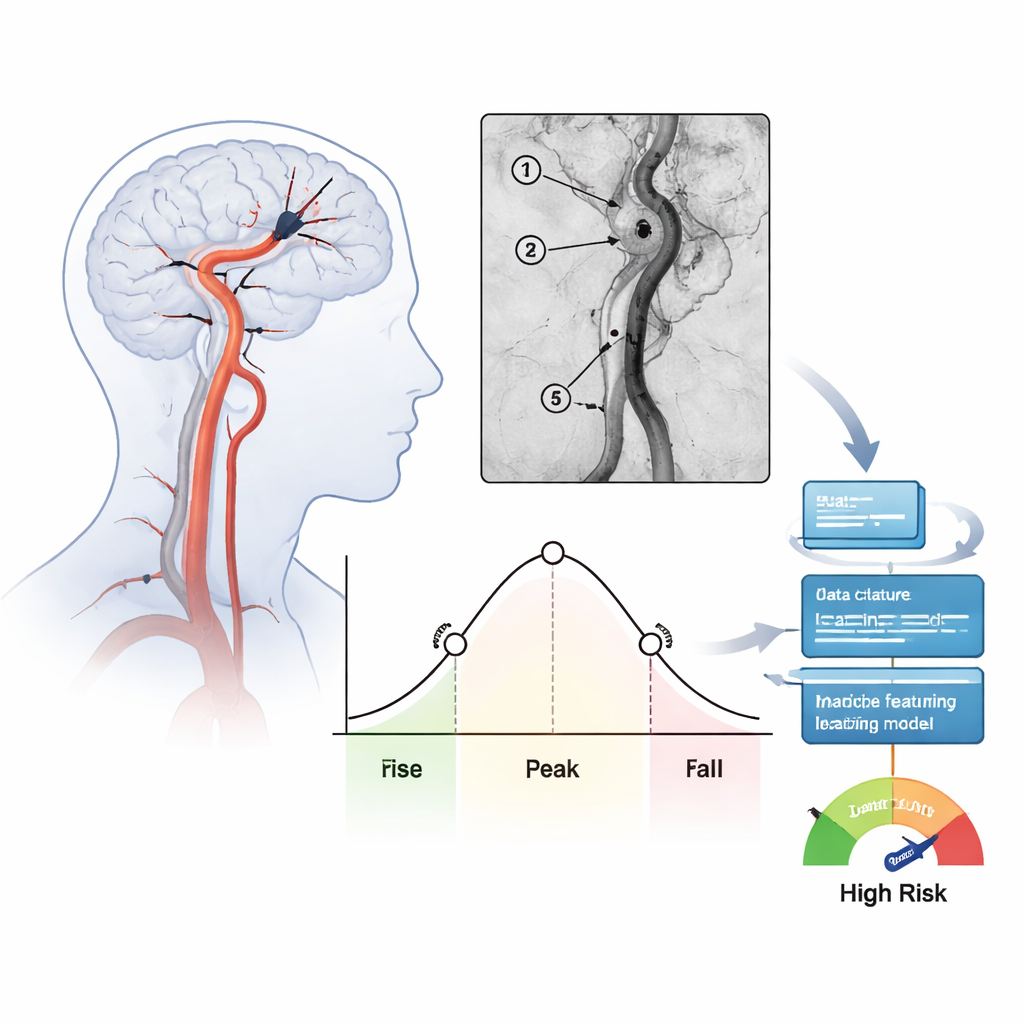
Convertir las películas angiográficas en números
El equipo estudió a 171 personas tratadas por ictus severo en la región anterior del cerebro a lo largo de un año en un único hospital. Tras la extracción del coágulo y la restauración del flujo, registraron vistas angiográficas estándar y analizaron cómo el contraste inyectado entraba y salía en varios puntos clave a lo largo de la arteria tratada. Para cada región calcularon medidas temporales, como cuánto tardaba la sangre en pasar (tiempo medio de tránsito) y qué anchura tenía la oleada principal de contraste (anchura a media altura). Estos números resumen si la sangre se mueve despacio y constante o pasa rápidamente en un pulso estrecho. En total, se extrajeron 39 características de flujo por paciente y se comprobó su consistencia entre evaluadores independientes.
Enseñar al ordenador a reconocer patrones riesgosos
Los investigadores usaron entonces un conjunto de métodos comunes de aprendizaje automático para ver si esas características de flujo, solas o combinadas con datos clínicos básicos como la edad y la gravedad del ictus, podían distinguir a los pacientes que más tarde desarrollaron sangrado cerebral de los que no. Para evitar el sobreajuste, primero aplicaron cinco técnicas diferentes de selección de características para elegir las mediciones más informativas, y dividieron repetidamente los datos en grupos de entrenamiento y prueba con validación cruzada. Entre muchas combinaciones evaluadas, el modelo relativamente simple—regresión logística, afinada con un filtro de características “Elastic Net”—fue el que mejor rendimiento mostró. Cuando se basó únicamente en medidas de flujo derivadas de la angiografía, separó correctamente a los pacientes con y sin hemorragia con un área bajo la curva ROC media de aproximadamente 0,81. Al añadir factores clínicos, el rendimiento subió a alrededor de 0,86, lo que sugiere que el modelo podría ser una valiosa ayuda para la toma de decisiones.
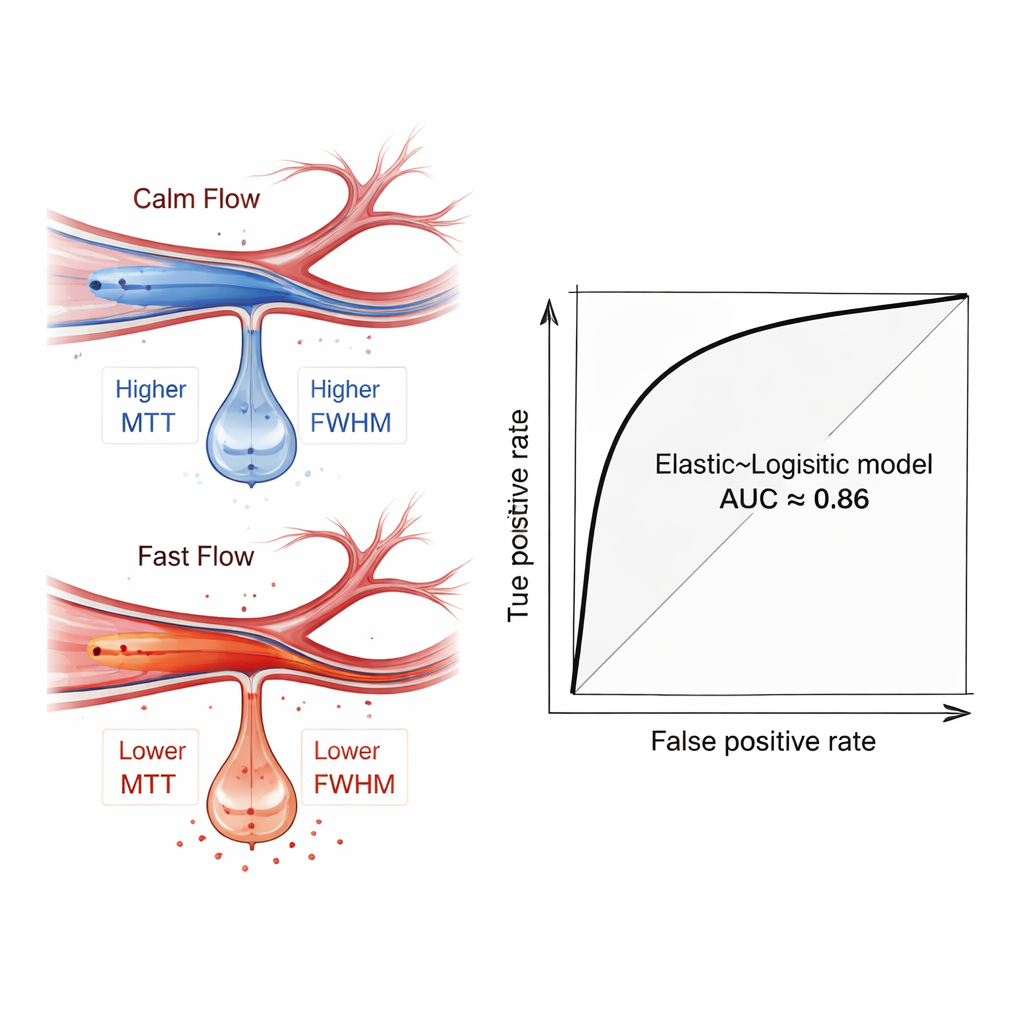
Lo que revelaron las señales de flujo sanguíneo
Al indagar en los modelos entrenados, los autores emplearon una técnica de interpretabilidad llamada SHAP para ver qué características eran más relevantes. Destacaron especialmente las medidas que capturan cuánto dura y cuán disperso está el pulso de flujo—sobre todo en una rama más distal de la arteria cerebral media—como predictores clave. Los pacientes que luego sangraron tendieron a mostrar un flujo más rápido y más focalizado en esos vasos distales, reflejado por tiempos de tránsito más bajos y picos más estrechos. Este patrón es una huella hemodinámica de la “hiperperfusión”, un estado en el que el tejido cerebral frágil, repentinamente inundado por sangre a alta velocidad tras el periodo de isquemia, es más propenso a filtrarse y sangrar. Es importante señalar que esta señal emergió incluso cuando comparaciones simples entre grupos no mostraron diferencias estadísticas dramáticas, subrayando el valor de un análisis multicaracterística y basado en máquinas.
Cómo podría cambiar la atención en la cama del paciente
Puesto que el método usa imágenes que ya se adquieren durante la trombectomía, no requiere exploraciones, contraste o radiación adicionales. Una vez dibujadas las regiones de interés—un paso que actualmente toma unos minutos—el ordenador puede calcular automáticamente las medidas de flujo y generar una estimación personalizada del riesgo de sangrado. En principio, esto podría ayudar a los médicos a ajustar objetivos de presión arterial, decidir cuán agresivos ser con los anticoagulantes y programar tomografías computarizadas tempranas en los pacientes identificados como de alto riesgo. Los autores advierten que su estudio es retrospectivo y procede de un único centro, por lo que hacen falta ensayos más amplios y multicéntricos antes de que la herramienta pueda guiar la práctica habitual. Aun así, ofrece una prueba de concepto clara: al convertir las angiografías de ictus en datos numéricos ricos y dejar que el aprendizaje automático los analice, podemos pasar de preguntar simplemente “¿está la arteria abierta?” a “¿es segura la microcirculación cerebral?”—un cambio que, en última instancia, podría evitar que más pacientes sufran hemorragias peligrosas tras el tratamiento.
Cita: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Palabras clave: ictus, trombectomía mecánica, hemorragia cerebral, aprendizaje automático, angiografía