Clear Sky Science · es
Impacto de los tratamientos sistémicos específicos para neoplasias neuroendocrinas en la expresión y función de CXCR4 en células de tumores neuroendocrinos
Por qué esto importa para la atención oncológica futura
Cuando ciertos cánceres raros del intestino y el páncreas se vuelven más agresivos, con frecuencia dejan de responder a los tratamientos dirigidos estándar. Médicos e investigadores necesitan con urgencia nuevas maneras de visualizar y atacar estos tumores más resistentes. Este estudio plantea una pregunta práctica con grandes implicaciones: ¿alteran los fármacos quimioterápicos y dirigidos que ya reciben los pacientes un marcador tumoral clave llamado CXCR4, que se está desarrollando tanto como “señal” diagnóstica como diana terapéutica?
Un blanco cambiante en células tumorales agresivas
Las neoplasias neuroendocrinas son cánceres poco frecuentes que se originan en células productoras de hormonas, con mayor frecuencia en el intestino y el páncreas. En su forma inicial, más ordenada, estos tumores suelen mostrar en la superficie una molécula llamada receptor de somatostatina 2, que los médicos pueden visualizar y tratar con fármacos radiactivos especializados. A medida que la enfermedad se vuelve más agresiva, estos tumores tienden a perder ese marcador, lo que dificulta su detección y tratamiento. Al mismo tiempo, muchos activan otra molécula de superficie, un receptor llamado CXCR4, que se asocia con mayor crecimiento, diseminación a órganos distantes y peor supervivencia. Dado que CXCR4 puede visualizarse con un trazador PET y potencialmente atacarse con fármacos radiactivos o basados en anticuerpos, se ha convertido en una prometedora diana “de reserva” cuando fallan las opciones estándar.
Probando fármacos del mundo real en modelos celulares tumorales
Los investigadores quisieron saber cómo afectan al propio CXCR4 los fármacos que ya se usan para tratar tumores neuroendocrinos de alto grado. Si estos medicamentos reducen inadvertidamente CXCR4, podrían debilitar futuras técnicas de imagen o terapias basadas en CXCR4 —pero también podrían contribuir a frenar la agresividad del cáncer. El equipo trabajó con tres líneas celulares humanas diferentes que representan formas agresivas de la enfermedad, incluida una línea híbrida que imita de cerca tumores especialmente difíciles de tratar. Expusieron estas células a seis agentes comunes: las quimioterapias cisplatino, etopósido, estreptozotocina, 5‑fluorouracilo, el fármaco oral temozolomida y el inhibidor dirigido de mTOR everolimus. Tras el tratamiento, midieron CXCR4 a nivel genético y proteico y evaluaron la capacidad de las células para captar un trazador PET dirigido a CXCR4.
Algunos fármacos atenúan la señal de CXCR4
Los resultados mostraron que no todos los fármacos antitumorales actúan igual respecto a este receptor. El cisplatino redujo claramente la actividad genética de CXCR4 en dos de las tres líneas celulares y disminuyó de forma significativa la captación del trazador en dos, lo que indica que había menos receptores funcionales para que el trazador se uniera. La temozolomida y el everolimus también bajaron los niveles genéticos y proteicos de CXCR4 en varios tipos celulares, aunque esto no siempre se tradujo en una caída estadísticamente clara de la captación del trazador. En contraste, el etopósido y la estreptozotocina tuvieron poco efecto sobre CXCR4, mientras que el 5‑fluorouracilo produjo cambios modestos que no alteraron de forma contundente la unión del trazador. En conjunto, el patrón sugiere que cisplatino, temozolomida y everolimus pueden atenuar CXCR4 en estas células tumorales agresivas, mientras que los otros agentes lo mantienen mayormente sin cambios.
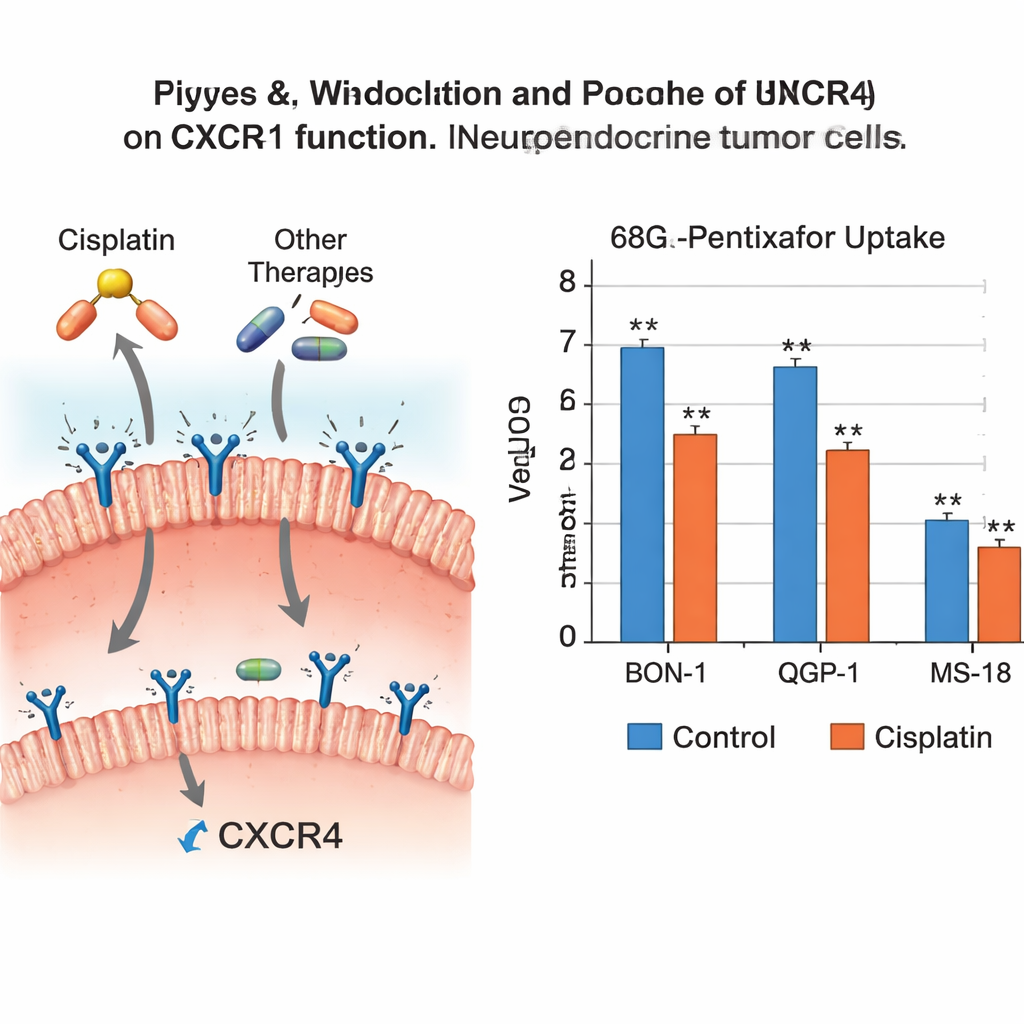
Qué significa esto para las exploraciones y el momento del tratamiento
Estos hallazgos transmiten un mensaje doble para la atención futura de los pacientes. Por un lado, la reducción de CXCR4 podría formar parte del modo en que fármacos como cisplatino, temozolomida y everolimus frenan la diseminación tumoral, porque niveles altos de CXCR4 se vinculan con invasividad y metástasis. Por otro lado, si el CXCR4 de un tumor queda suprimido por un tratamiento en curso, las PET basadas en CXCR4 podrían subestimar la cantidad de enfermedad presente, y las terapias radiactivas dirigidas a CXCR4 podrían disponer de menos sitios de anclaje. El estudio sugiere que combinar tratamientos dirigidos a CXCR4 directamente con estos fármacos sistémicos probablemente no potencie las terapias centradas en CXCR4 e incluso podría debilitarlas.
Una nueva pieza del rompecabezas para la terapia personalizada
Para el público general, la conclusión clave es que un único marcador tumoral puede desempeñar dos papeles a la vez: ser un signo de enfermedad agresiva y, al mismo tiempo, una herramienta útil para la imagen y el tratamiento dirigido. Esta investigación muestra que algunos fármacos oncológicos establecidos pueden ajustar discretamente ese marcador al alza o a la baja. En la práctica, esto podría influir en cuándo programar exploraciones y terapias basadas en CXCR4 —idealmente cuando el receptor esté más abundante— y puede ayudar a explicar por qué ciertos tratamientos son eficaces contra tumores neuroendocrinos de crecimiento rápido. Aunque estos resultados proceden de modelos celulares y deben confirmarse en pacientes, constituyen un paso importante hacia una secuenciación más inteligente de las terapias para personas con estos cánceres complejos.
Cita: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
Palabras clave: tumores neuroendocrinos, CXCR4, cisplatino, everolimus, imagen dirigida