Clear Sky Science · es
Un biosensor electroquímico M13 modificado–rGO para la detección rápida de una proteína viral en matrices complejas
Por qué siguen siendo importantes las pruebas rápidas de virus
La pandemia de COVID-19 puso de manifiesto lo crucial que es detectar virus con rapidez, no solo en pacientes, sino también en entornos como aguas residuales y líneas de procesamiento de alimentos. Las pruebas de laboratorio actuales son potentes pero pueden ser lentas, caras y depender de reactivos biológicos frágiles que son difíciles de enviar y conservar. Este estudio presenta un nuevo tipo de sensor electrónico diminuto que utiliza virus modificados y una lámina de un material de carbono avanzado para detectar una proteína clave del SARS-CoV-2 en menos de un segundo, incluso en muestras reales y complejas como suero sanguíneo, leche y aguas residuales.
Convertir un virus inofensivo en un detector inteligente
El núcleo del dispositivo es M13, un virus inofensivo que normalmente infecta bacterias. Su cuerpo largo y en forma de varilla está cubierto por numerosas proteínas de la cápside idénticas que los científicos pueden reprogramar genéticamente. El equipo insertó un péptido corto y diseñado en una de estas proteínas para que las partículas de M13 reconocieran y se unieran al fragmento S1 de la proteína spike del coronavirus. Una segunda versión del virus, que portaba un péptido aleatorizado, se empleó como control para demostrar que la respuesta proviene de un reconocimiento específico y no de una unión fortuita.
Construido sobre una lámina de carbono de un átomo de grosor
Para convertir este virus programable en un sensor, los investigadores lo fijaron a una película plana de óxido de grafeno reducido, una forma altamente conductora de carbono obtenida mediante el tratamiento químico del grafito. Tras depositar óxido de grafeno en pequeños chips de vidrio y calentarlos para convertirlo en óxido de grafeno reducido, añadieron una molécula enlazadora que se adhiere a la superficie de carbono y también se une a grupos amina del virus. Esto creó una capa densa de partículas de M13 ancladas a la lámina conductora. La microscopía electrónica y la microscopía de fuerza atómica confirmaron que cada paso de fabricación modificaba la superficie según lo esperado, y las mediciones eléctricas mostraron que la adición del enlazador y luego del virus aumentaba de forma progresiva la resistencia, señal de que la superficie estaba quedando recubierta con éxito.
Leer la unión viral como un pulso eléctrico
A diferencia de muchos biosensores que necesitan reactivos adicionales o partes móviles, esta plataforma funciona como una simple resistencia bajo una tensión constante muy baja. Cuando la proteína S1 aterriza en la superficie recubierta por el virus y se une al péptido desplegado, altera ligeramente la forma en que la carga se mueve a través de la capa de grafeno. Esto aparece como un breve pico en la corriente eléctrica que surge aproximadamente 300 milisegundos después de posar una gota de muestra sobre el chip y luego se atenúa a medida que el sistema se estabiliza. Ajustando la tensión aplicada, el equipo identificó un punto óptimo alrededor de −0,8 milivoltios, donde la señal por la unión específica de S1 era fuerte mientras que el ruido de fondo y las respuestas a proteínas no relacionadas, como la albúmina sérica bovina, permanecían bajas.
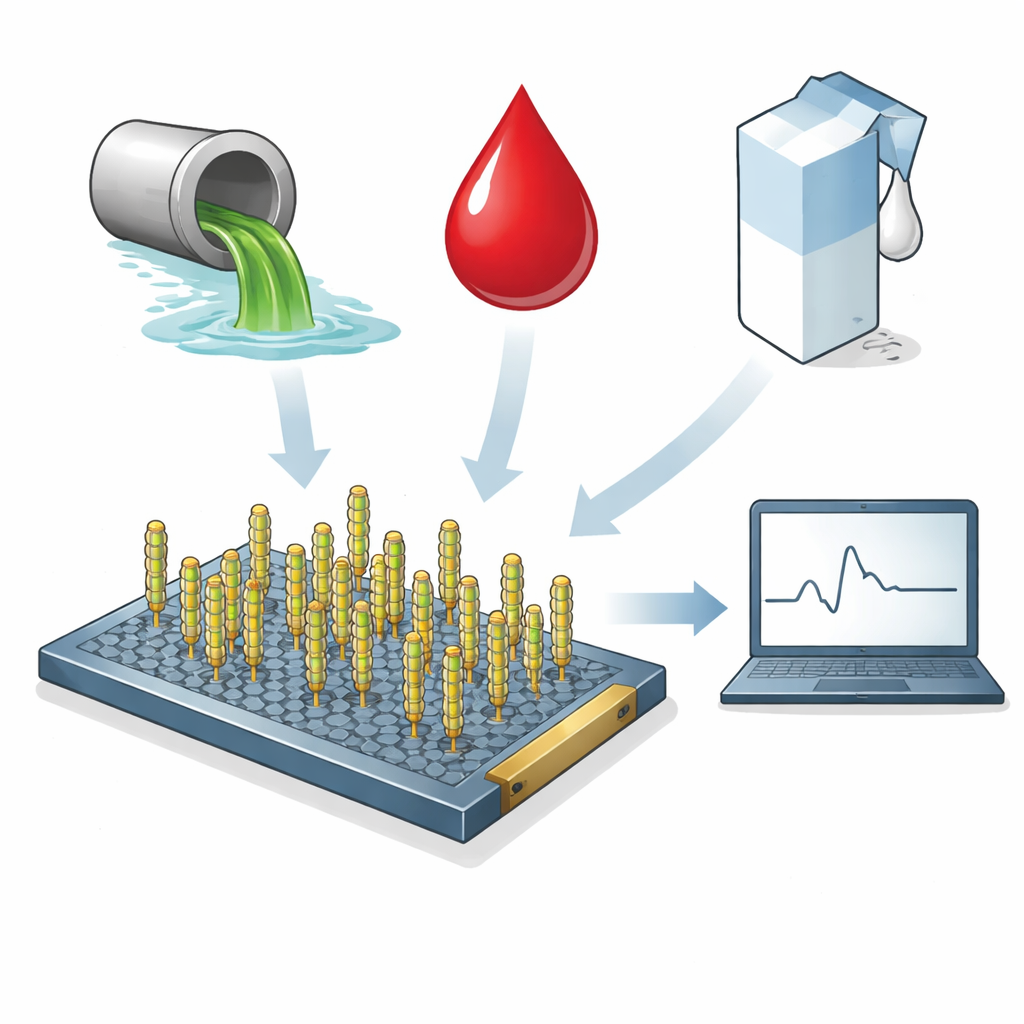
Funcionamiento en muestras reales y complejas
Los investigadores sometieron entonces el sensor a los tipos de mezclas complejas que a menudo frustran a los reactivos delicados de laboratorio. Probaron el dispositivo en tampón, aguas residuales municipales, suero fetal bovino (un sustituto de la sangre) y leche pasteurizada, con y sin adición de proteína S1. Usando un umbral estadísticamente definido para marcar un resultado positivo, el sensor detectó niveles extremadamente bajos de proteína en tampón—hasta alrededor de 10⁻⁴ picogramos por mililitro—comparables o superiores a muchos sistemas basados en anticuerpos. En aguas residuales, el dispositivo señalizó de forma fiable niveles más altos de S1, mientras que en suero y leche detectó de manera consistente concentraciones más bajas también, todo ello en una fracción de segundo. Es importante que un sensor de control fabricado con el virus aleatorizado mostró poca respuesta a S1, confirmando que la señal depende de la secuencia de unión diseñada. Un sensor paralelo utilizando un anticuerpo convencional sobre la misma plataforma de grafeno rindió de forma similar, lo que sugiere que el sistema basado en virus puede igualar la sensibilidad de los anticuerpos y, potencialmente, ser más barato y fácil de producir.

Qué podría significar esto para las pruebas cotidianas
Los anticuerpos, pilares de muchos diagnósticos, son costosos de fabricar, sensibles al calor y por lo general requieren cadena de frío desde la fábrica hasta la clínica. En contraste, los virus M13 pueden cultivarse en bacterias como un cultivo sencillo, toleran condiciones más adversas y pueden reprogramarse reescribiendo su código genético. Al casar esta robustez y flexibilidad con una lectura electrónica rápida y de bajo consumo sobre grafeno, el estudio traza una vía hacia dispositivos portátiles y de bajo coste que podrían adaptarse para detectar muchos marcadores de enfermedad o contaminantes simplemente cambiando el péptido mostrado. El trabajo aún está en fase de prueba de concepto y no se ha evaluado todavía en muestras clínicas humanas, pero apunta hacia un futuro en el que sensores de mano podrían detectar proteínas virales y otros biomarcadores en clínicas, alcantarillas o incluso productos alimentarios en segundos, sin la carga logística de las pruebas tradicionales basadas en anticuerpos.
Cita: Alshehhi, H.Y., Tizani, L., Palanisamy, S. et al. An engineered M13 phage–rGO electrochemical biosensor for rapid detection of viral protein in complex matrices. Sci Rep 16, 9279 (2026). https://doi.org/10.1038/s41598-026-37008-w
Palabras clave: biosensor, grafeno, bacteriófago, SARS-CoV-2, detección electroquímica