Clear Sky Science · es
Secuenciación de amplicones con Oxford Nanopore Technologies como alternativa diagnóstica para los lentivirus de pequeños rumiantes en ovejas
Infecciones ocultas en las ovejas de todos los días
En todo el mundo, las ovejas albergan silenciosamente virus que pueden minar su salud, acortar su vida y costar dinero a los ganaderos —a menudo sin síntomas evidentes durante años. Este estudio explora una nueva forma de descubrir esas infecciones ocultas mediante una tecnología de secuenciación de ADN portátil, ofreciendo un posible cambio de escala en la manera de proteger el bienestar animal, los ingresos agrícolas e incluso la seguridad alimentaria.
Una enfermedad lenta, costosa y difícil de detectar
El trabajo se centra en los lentivirus de pequeños rumiantes (SRLV), un grupo de virus que infectan ovejas y cabras. En ovejas causan la enfermedad Maedi-Visna, una infección de larga duración que puede provocar problemas respiratorios, artritis, enfermedades neurológicas e inflamación crónica de la ubre. Muchos animales infectados nunca muestran signos claros, pero el virus aún reduce la producción de leche, aumenta la mortalidad de los corderos y obliga a sacrificios prematuros. En algunas explotaciones lecheras europeas, incluidas las de España y Grecia, aproximadamente la mitad de los animales puede estar infectada, lo que convierte a esta enfermedad en una de las más importantes en granjas intensivas.
Por qué las pruebas actuales no detectan a muchos animales infectados
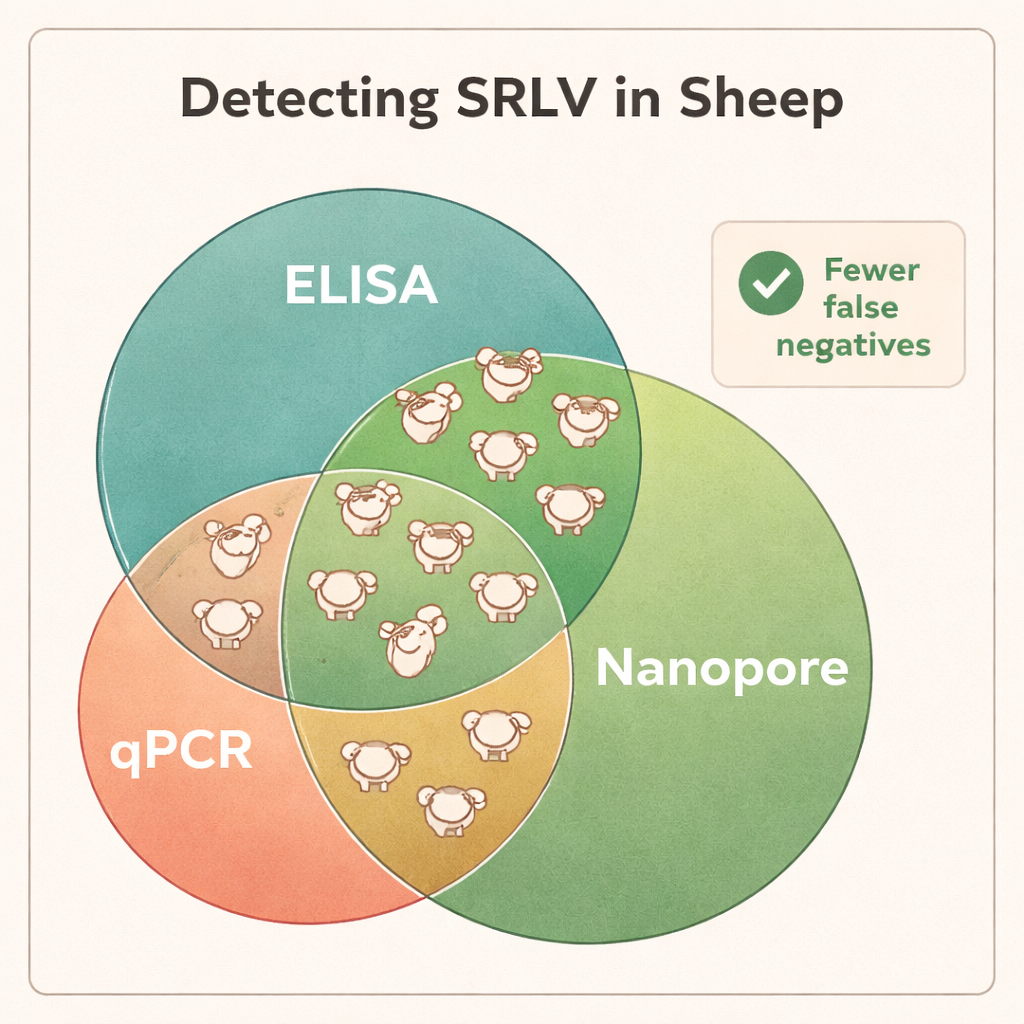
Hoy en día, las explotaciones se basan principalmente en análisis de sangre que buscan anticuerpos (ELISA) o en pruebas estándar de ADN (qPCR) para decidir qué animales están infectados y deben eliminarse del rebaño. Pero los SRLV mutan y recombinan rápidamente, generando muchas variantes virales ligeramente diferentes. Algunas variantes son poco reconocidas por las pruebas de anticuerpos, y algunos animales infectados nunca desarrollan respuestas fuertes de anticuerpos. La qPCR, que apunta a fragmentos cortos y muy específicos del ADN viral, también puede fallar si esas regiones objetivo cambian. Como resultado, muchos animales realmente infectados dan negativo en las pruebas y permanecen en el rebaño, propagando silenciosamente el virus.
Usar la lectura de ADN en tiempo real para encontrar el virus
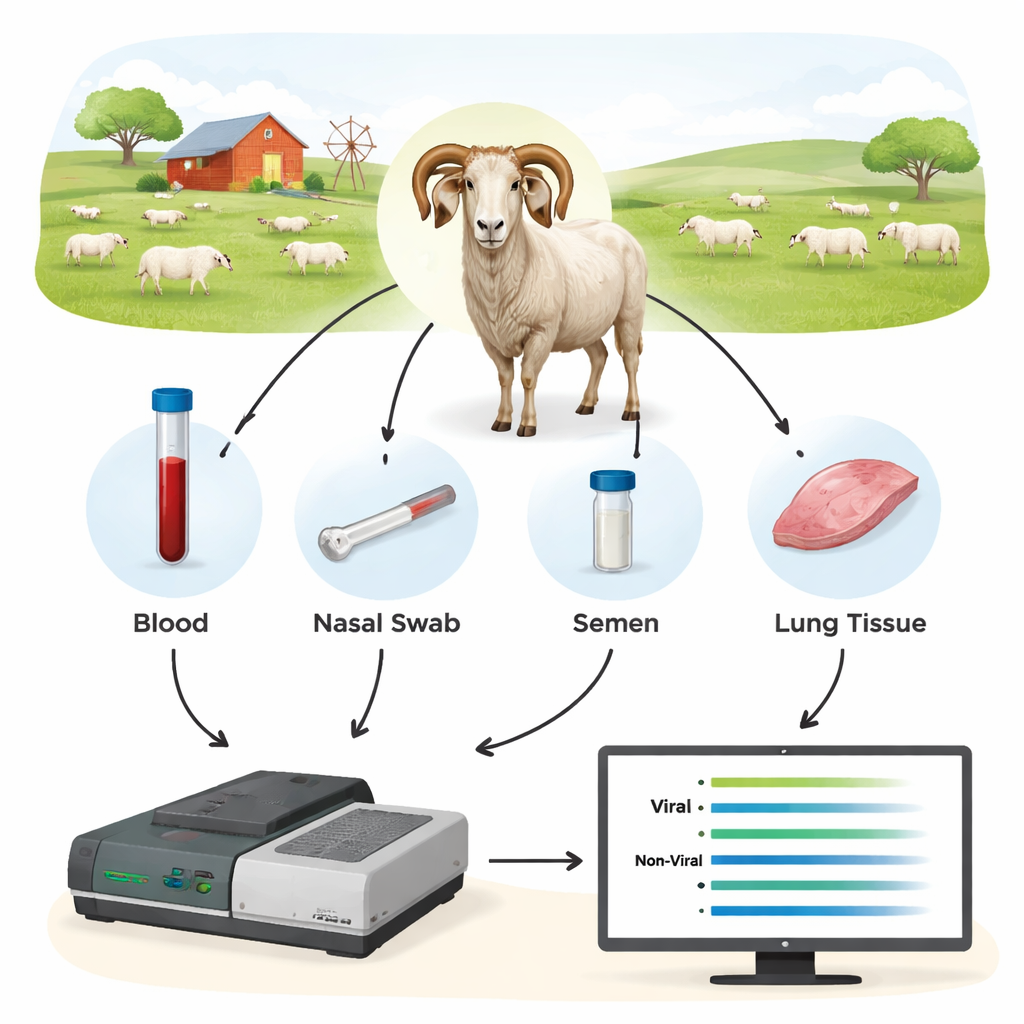
Los investigadores probaron un método de tercera generación llamado secuenciación Oxford Nanopore como una nueva herramienta diagnóstica. En lugar de buscar un único y pequeño fragmento de ADN viral, primero amplificaron tramos más largos de genes virales clave a partir de las muestras de los animales y luego secuenciaron esas piezas en tiempo real en un dispositivo Nanopore. Recogieron sangre, hisopos nasales, semen y células procedentes de sangre y pulmón de 44 carneros y de ovejas adicionales, muchas de las cuales ya habían sido analizadas por métodos convencionales. Al centrarse en regiones virales relativamente conservadas pero lo suficientemente largas como para revelar la cepa exacta, el equipo pudo tanto detectar la infección como identificar qué tipos virales estaban presentes.
La sangre funciona mejor — y detecta lo que otras pruebas pasan por alto
La secuenciación mostró que el ADN de sangre total fue el material más fiable para descubrir SRLV, aunque el virus vive principalmente en un subconjunto reducido de leucocitos. El tejido pulmonar de animales muy infectados rindió cantidades muy altas de ADN viral, pero tales muestras solo están disponibles tras el sacrificio. En contraste, los hisopos nasales, el semen y los glóbulos blancos purificados ofrecieron material viral insuficiente para un diagnóstico consistente. Cuando los científicos compararon los resultados de Nanopore con las pruebas estándar ELISA y qPCR, las diferencias fueron notables: la secuenciación Nanopore confirmó la infección en todos los carneros positivos por ELISA, pero además reveló que muchos animales negativos por ELISA estaban, de hecho, infectados. En distintos rebaños, aproximadamente el 40–45 % de los animales catalogados como “negativos” por ELISA resultaron portar el virus, y la qPCR pasó por alto una fracción aún mayor. Los datos de secuenciación también descubrieron coinfecciones con diferentes tipos de SRLV en algunos carneros, información que las pruebas tradicionales no proporcionan fácilmente.
De respuestas simples de sí/no a conocimientos más profundos
Puesto que Nanopore lee las secuencias virales reales, puede ir más allá de un diagnóstico simple de sí o no. El equipo utilizó los datos para comparar cepas virales, construir árboles filogenéticos de los virus que circulaban en sus rebaños y estudiar diferencias sutiles en proteínas virales que podrían explicar por qué algunos animales escapan a la detección por los kits ELISA estándar. Demostraron que ciertas versiones de una proteína viral clave, diana de las pruebas serológicas comerciales, difieren de forma notable entre animales con anticuerpos y animales sin ellos. Con el tiempo, esa información podría ayudar a perfeccionar tanto las pruebas serológicas como los programas de cría orientados a seleccionar animales naturalmente más resistentes a la infección.
Qué significa esto para los ganaderos y la salud animal
Para el público general, el mensaje principal es simple: leyendo tramos más largos de ADN viral directamente, la secuenciación Nanopore puede descubrir más ovejas infectadas, antes y con mayor precisión, que las pruebas rutinarias actuales. También indica qué cepas virales exactas están presentes en un rebaño. Aunque este enfoque sigue siendo más complejo y costoso que un simple análisis de sangre, la tecnología se está volviendo más rápida, barata y portátil. Si se integra en los programas de control, podría reducir drásticamente el número de portadores “ocultos”, mejorar el diseño de vacunas y pruebas, y apoyar la cría de animales más resistentes —haciendo la producción ovina más sostenible y humana.
Cita: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Palabras clave: salud ovina, lentivirus, secuenciación nanopore, diagnóstico veterinario, Maedi-Visna