Clear Sky Science · es
Nanopartículas antimicrobianas de amplio espectro con baja toxicidad para prevenir la formación de biofilm en dispositivos urológicos
Por qué los implantes médicos a veces se vuelven en nuestra contra
La medicina moderna depende de tubos y dispositivos implantables de plástico para drenar la orina, aliviar obstrucciones renales y restaurar la función sexual. Sin embargo, esos mismos dispositivos pueden convertirse en imanes para las bacterias, que forman comunidades protectoras viscosas llamadas biofilms. Una vez que se establece un biofilm, las infecciones son difíciles de tratar, lo que a menudo obliga a los médicos a retirar o reemplazar el dispositivo. Este estudio explora un nuevo tipo de recubrimiento microscópico, compuesto por oro y plata envueltos en una capa de carbono, diseñado para impedir que esos biofilms se formen desde el principio.
El problema oculto de los gérmenes pegajosos
Catéteres, stents ureterales y prótesis peneanas inflables ayudan a cientos de miles de pacientes, pero también ofrecen un hábitat ideal para los microbios. Las bacterias se adhieren a la superficie del dispositivo y secretan una matriz adhesiva de azúcares, proteínas y lípidos, formando una fortaleza que las protege de los antibióticos y del sistema inmunitario. Como resultado, las infecciones relacionadas con dispositivos constituyen más de una cuarta parte de todas las infecciones nosocomiales y cuestan cientos de millones de dólares al año. Los recubrimientos actuales basados en antibióticos o en plata simple tienen dificultades para prevenir biofilms a largo plazo y pueden contribuir al aumento de la resistencia a los antibióticos.
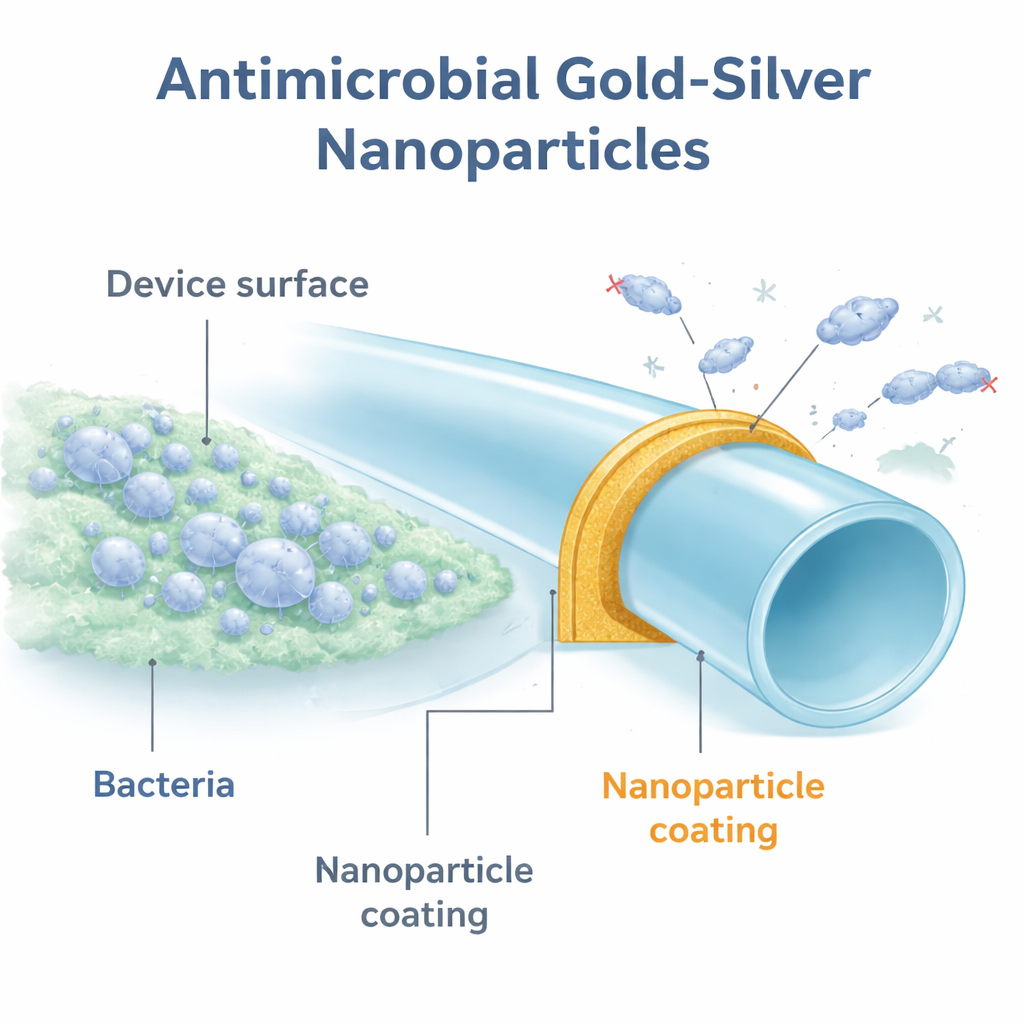
Un nuevo tipo de armadura protectora
Los investigadores se centraron en partículas metálicas diminutas de apenas unos pocos miles de millones de metros de ancho. Estas nanopartículas se construyeron alrededor de una estructura de carbono llamada polihidroxi fullereno, conocida por ser no tóxica y por potenciar el rendimiento de ciertos metales. Crearon varias versiones con diferentes metales y luego recubrieron pequeños discos de poliuretano, un plástico de uso común en dispositivos urológicos. Al probar estos discos recubiertos frente a una cepa estándar de Escherichia coli, solo las partículas que contenían plata mostraron efectos antibacterianos contundentes. La combinación que destacó fue una mezcla de oro y plata, denominada GSNPs, que redujo el número de bacterias hasta en 100.000 veces en comparación con el plástico sin recubrimiento.
Deteniendo los gérmenes urológicos del mundo real
Para comprobar si este efecto se mantenía más allá de una cepa de laboratorio, el equipo evaluó su mejor recubrimiento frente a seis tipos de bacterias tomadas directamente de stents ureterales y prótesis peneanas infectadas. Estas incluían especies Gram-positivas y Gram-negativas conocidas por causar infecciones difíciles de erradicar. Con niveles bacterianos similares a los encontrados en pacientes, las superficies recubiertas con GSNP lograron una reducción del 100 % tanto de bacterias en suspensión como de las adheridas a la superficie para cada cepa probada. En experimentos separados, los investigadores expusieron las bacterias a diferentes concentraciones de nanopartículas en líquido y estimaron la cantidad de GSNP necesaria para detener el crecimiento. Todas las cepas quedaron totalmente inhibidas a 3 microgramos de GSNP por mililitro de líquido o menos, requiriéndose cantidades algo mayores para algunos organismos Gram-positivos.
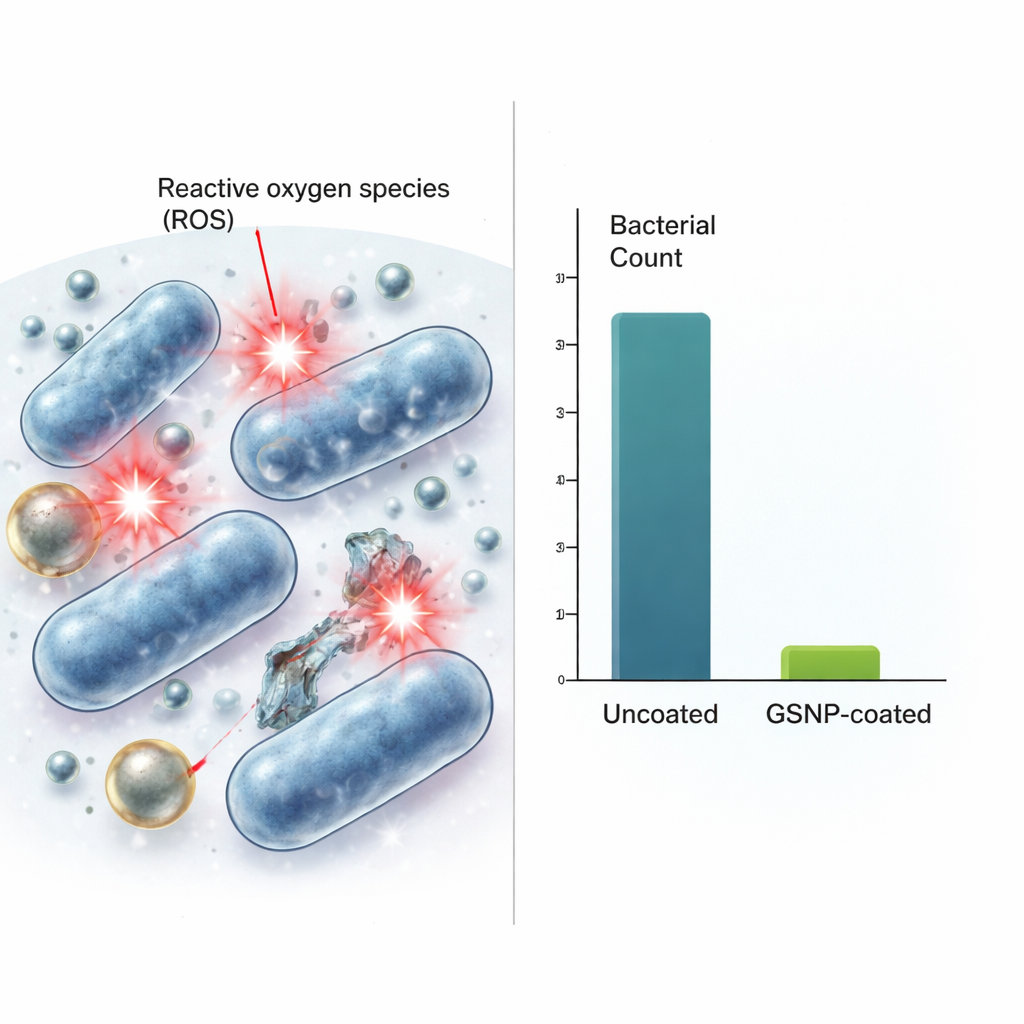
Cómo actúan y cuán seguras son
El equipo investigó a continuación cómo estos recubrimientos matan a las bacterias y si también podrían dañar células humanas. Sus datos señalan a las especies reactivas de oxígeno —formas de oxígeno químicamente reactivas— como una parte clave del mecanismo de muerte. Aunque las nanopartículas por sí solas no generaron estas moléculas reactivas, las bacterias expuestas a GSNP produjeron niveles mucho más altos que las bacterias sin tratar, lo que sugiere que las partículas desencadenan una química dañina dentro o cerca de los microbios. Cuando células fibroblásticas de ratón se expusieron a concentraciones similares o superiores de GSNP, más del 80 % de las células permanecieron vivas con la dosis antibacteriana de peor escenario. En otras palabras, los niveles que eliminaron las bacterias tuvieron solo un impacto modesto sobre las células de mamíferos. Los GSNP también fueron notablemente más eficaces que un producto comercial de nanopartículas oro–plata probado en paralelo, logrando aproximadamente una reducción bacteriana un millón de veces mayor a dosis equivalentes.
Qué podría significar esto para los pacientes
Aunque este trabajo se realizó en laboratorio y aún no en animales ni en humanos, los hallazgos apuntan a una estrategia prometedora para implantes médicos más seguros. Una capa delgada de GSNP en un catéter o prótesis podría ofrecer protección amplia frente a muchas bacterias diferentes, reducir la necesidad de retirar dispositivos y hacerlo sin depender de los antibióticos tradicionales. El recubrimiento usa cantidades pequeñas de metal, muestra toxicidad relativamente baja en las pruebas iniciales y es sencillo de fabricar. Con más ingeniería para mejorar la estabilidad a largo plazo y ensayos cuidadosos en modelos realistas, estos recubrimientos de nanopartículas oro–plata podrían ayudar a mantener los dispositivos urológicos vitales funcionando para los pacientes en lugar de convertirse en un foco de infección.
Cita: Rodriguez-Alvarez, J.S., Xu, Y., Gutierrez-Aceves, J. et al. Broad spectrum antimicrobial nanoparticles with low toxicity to prevent biofilm formation on urologic devices. Sci Rep 16, 7333 (2026). https://doi.org/10.1038/s41598-026-36969-2
Palabras clave: biofilm, dispositivos urológicos, recubrimiento antimicrobiano, nanopartículas, oro-plata