Clear Sky Science · es
Análisis proteómico cuantitativo del plasma tras el condicionamiento isquémico remoto en el ictus isquémico agudo
Por qué apretar un brazo podría ayudar a proteger el cerebro
Cuando alguien sufre un ictus por la obstrucción de un vaso sanguíneo, cada minuto de flujo sanguíneo perdido pone en riesgo a las células cerebrales. Los tratamientos estándar intentan reabrir la arteria bloqueada, pero muchos pacientes llegan demasiado tarde o no son elegibles. Los investigadores están explorando una terapia complementaria sorprendentemente sencilla: cortar brevemente el flujo sanguíneo de un brazo o una pierna con un manguito de presión arterial, una estrategia llamada condicionamiento isquémico remoto (CIR). Este estudio plantea una pregunta clave para convertir esa idea en terapia real: ¿qué cambios produce exactamente el CIR en la sangre de los pacientes con ictus, y podrían esos cambios indicar quiénes podrían beneficiarse más?
Una señal de estrés suave enviada del miembro al cerebro
El CIR funciona inflando repetidamente un manguito en un miembro durante unos minutos y luego desinflándolo, creando episodios cortos e inofensivos de bajo flujo sanguíneo. Experimentos en animales y ensayos clínicos iniciales sugieren que este “estrés controlado” puede enviar señales a órganos distantes, incluido el cerebro, para activar programas protectores. En un gran ensayo clínico llamado RICAMIS, los pacientes con ictus isquémico moderado que recibieron CIR además de la atención habitual evolucionaron mejor a los 90 días que los que recibieron solo la atención habitual. Sin embargo, otro ensayo (RESIST) no encontró ese beneficio, dejando a los médicos inseguros sobre cuándo y para quién funciona realmente el CIR. El estudio actual examina la sangre de los pacientes en busca de pistas moleculares: proteínas medibles, o biomarcadores, que cambian con el tiempo con el CIR.
Siguiendo la sangre de los pacientes durante su estancia hospitalaria
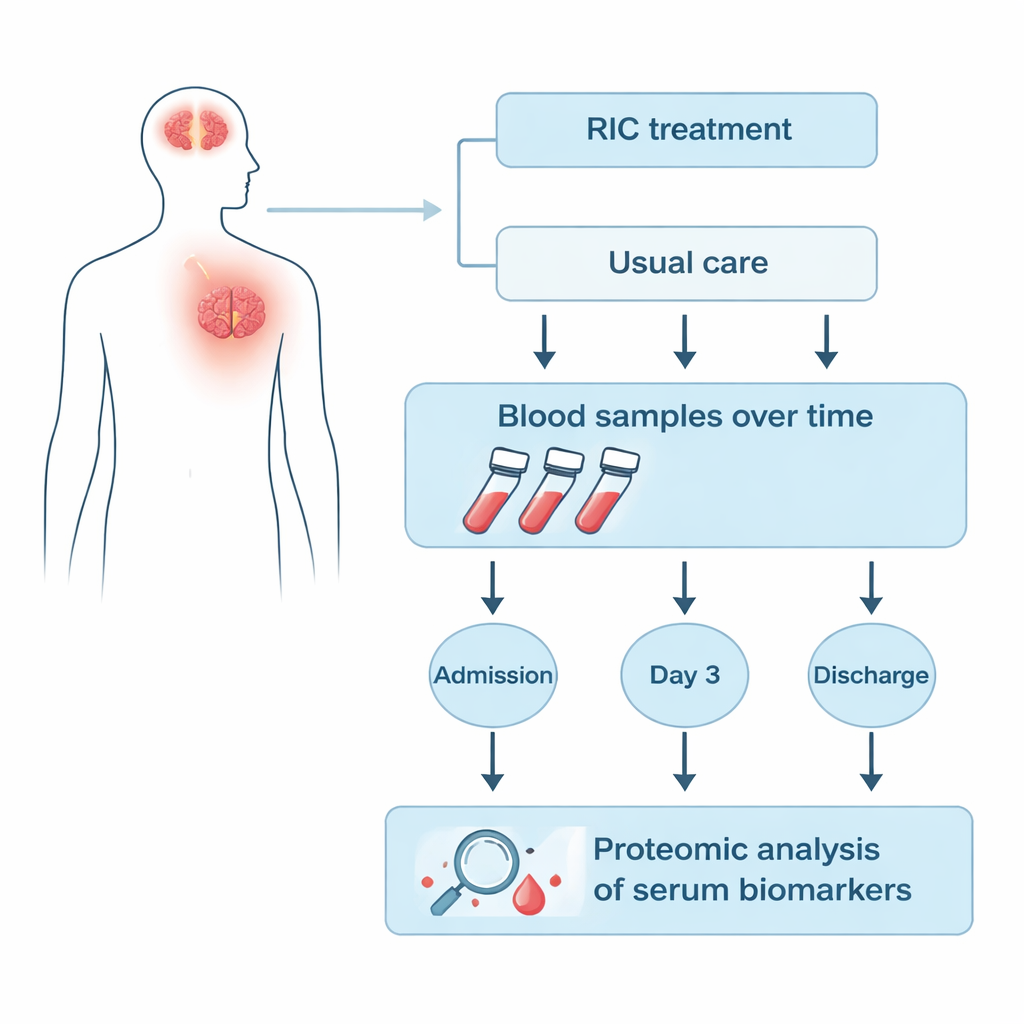
Los investigadores se centraron en 25 pacientes del ensayo RICAMIS a quienes se les recogieron muestras de sangre en tres momentos: al ingreso, a los tres días de asignado el tratamiento y al alta hospitalaria. Nueve pacientes recibieron CIR además de la atención habitual, mientras que dieciséis recibieron solo la atención habitual. Usando una técnica llamada proteómica cuantitativa, el equipo midió cientos de proteínas en la fracción sérica de la sangre de una sola vez, en lugar de analizar solo unos pocos marcadores preseleccionados. Luego compararon cómo subía o bajaba el nivel de cada proteína con el tiempo en el grupo CIR frente al grupo control para encontrar firmas que estuvieran vinculadas de forma única al CIR.
Nueve señales destacadas en el torrente sanguíneo
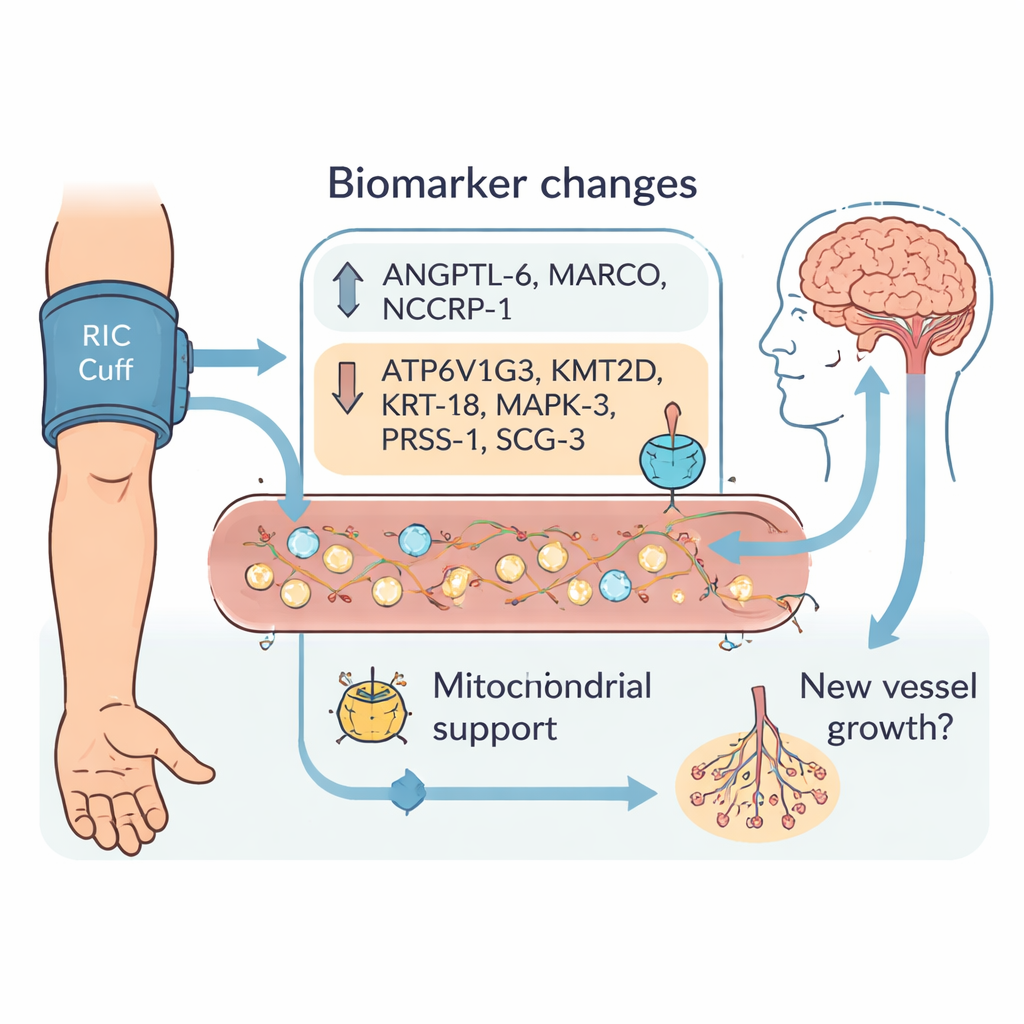
A lo largo de la estancia hospitalaria, docenas de proteínas cambiaron de forma diferente entre los dos grupos. Tras un filtrado cuidadoso, el equipo destacó nueve biomarcadores cuyos cambios desde el ingreso hasta el día 3 y hasta el alta separaron claramente a los pacientes tratados con CIR de los controles. Tres proteínas—ANGPTL‑6, MARCO y NCCRP‑1—aumentaron más con CIR. Otras seis—ATP6V1G3, KMT2D, KRT‑18, MAPK‑3, PRSS‑1 y SCG‑3—tendieron a disminuir. Muchas de estas moléculas participan en cómo las células gestionan la energía en sus pequeñas centrales, las mitocondrias, o en cómo crecen y remodelan los vasos sanguíneos. Esto encaja con la idea de que el CIR no solo protege a las neuronas del daño, sino que puede ayudar a las regiones cerebrales lesionadas a reorganizarse, reparar su suministro sanguíneo y recuperar función en días o semanas.
Pistas sobre el uso de energía y el crecimiento de nuevos vasos
Para entender mejor qué podrían estar haciendo estas nueve proteínas, los autores las mapearon en rutas biológicas conocidas. Dos de ellas, KMT2D y MAPK‑3, están relacionadas con cómo se empaqueta el ADN y cómo se activan o desactivan genes, especialmente en programas vinculados al crecimiento vascular. Otras, como ATP6V1G3 y KRT‑18, se han asociado en trabajos previos con el mantenimiento de mitocondrias saludables y la protección del tejido cardiaco tras una lesión. En conjunto, estos patrones apuntan a que el CIR empuja al organismo hacia un uso de energía más eficiente y favorece el crecimiento o remodelado de vasos sanguíneos, lo que podría mejorar el flujo alrededor del área dañada por el ictus. Al mismo tiempo, algunos marcadores, como NCCRP‑1 y MARCO, pueden reflejar las respuestas agudas de estrés e inmunitarias del cuerpo al procedimiento de inflado del manguito, subrayando que el CIR desencadena una reacción corporal compleja y sistémica.
Qué significa esto para la atención del ictus en el futuro
Este pequeño estudio exploratorio no puede demostrar exactamente cómo el CIR protege el cerebro, y solo incluyó a 25 pacientes de un único país, por lo que los hallazgos deben confirmarse en grupos mucho más grandes y diversos. Aun así, identificar una lista breve de nueve proteínas que cambian de manera consistente en direcciones opuestas con y sin CIR es un paso importante. En el futuro, tales biomarcadores podrían ayudar a los médicos a saber rápidamente si el CIR está “haciendo efecto” en un paciente concreto, orientar la selección de quién debería recibirlo o incluso inspirar tratamientos farmacológicos que imiten sus efectos beneficiosos sin el manguito. Por ahora, el trabajo refuerza una idea simple pero potente: al estresar de forma segura una parte del cuerpo, podemos inducir al cerebro a un estado más resiliente y con mayor capacidad de reparación tras un ictus.
Cita: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
Palabras clave: ictus isquémico agudo, condicionamiento isquémico remoto, biomarcadores séricos, análisis proteómico, neuroprotección