Clear Sky Science · es
Análisis del proteoma y fosfoproteoma basado en Orbitrap Astral identifica proteínas candidatas asociadas con la fosfatasa de fosfatida MoPah1 en Magnaporthe oryzae
Por qué importa una enzima de una enfermedad del arroz
El arroz es un alimento básico para miles de millones de personas, pero un único hongo microscópico, Magnaporthe oryzae, causa la enfermedad conocida como blast del arroz que puede arrasar cosechas enteras. Este estudio profundiza en la química interna de ese hongo, centrándose en una enzima, MoPah1, que ayuda a gestionar las grasas celulares y las moléculas de señalización. Al mapear miles de proteínas y sus interruptores on‑off, los investigadores revelan cómo esta enzima conecta el metabolismo básico con la capacidad del hongo para infectar las plantas de arroz.
Un hongo que penetra las plantas de arroz
Magnaporthe oryzae infecta las hojas de arroz mediante una estructura especializada llamada apresorio, que acumula una enorme presión interna para perforar la superficie de la hoja. Para impulsar este proceso, el hongo consume rápidamente azúcares y grasas almacenadas. Trabajos previos mostraron que MoPah1, una enzima que convierte una molécula grasa llamada ácido fosfatídico en otra llamada diacilglicerol, es vital para este modo de vida: eliminar el gen MoPah1 debilita al hongo y reduce su capacidad para causar la enfermedad. Pero cuáles otras proteínas están vinculadas a MoPah1 y cómo encaja esta enzima en redes celulares más amplias seguía siendo desconocido.
Uso de mapeo proteico de nueva generación
Para responder a estas preguntas, el equipo comparó hongos normales con un mutante carente de MoPah1. Se centraron en el crecimiento filamentoso (micelio), porque el mutante no puede producir las esporas que normalmente se usan en estudios de infección. Empleando un espectrómetro de masas avanzado llamado Orbitrap Astral y una estrategia de adquisición independiente de datos (DIA), midieron tanto la abundancia de proteínas como la presencia de etiquetas fosfato que actúan como interruptores moleculares. En total identificaron 6.799 proteínas y más de 15.000 sitios de fosforilación, con cientos que mostraron aumentos o disminuciones claros en el mutante. Este conjunto de datos amplio y de alta calidad ofrece una instantánea detallada de cómo la eliminación de MoPah1 remodela la célula fúngica.
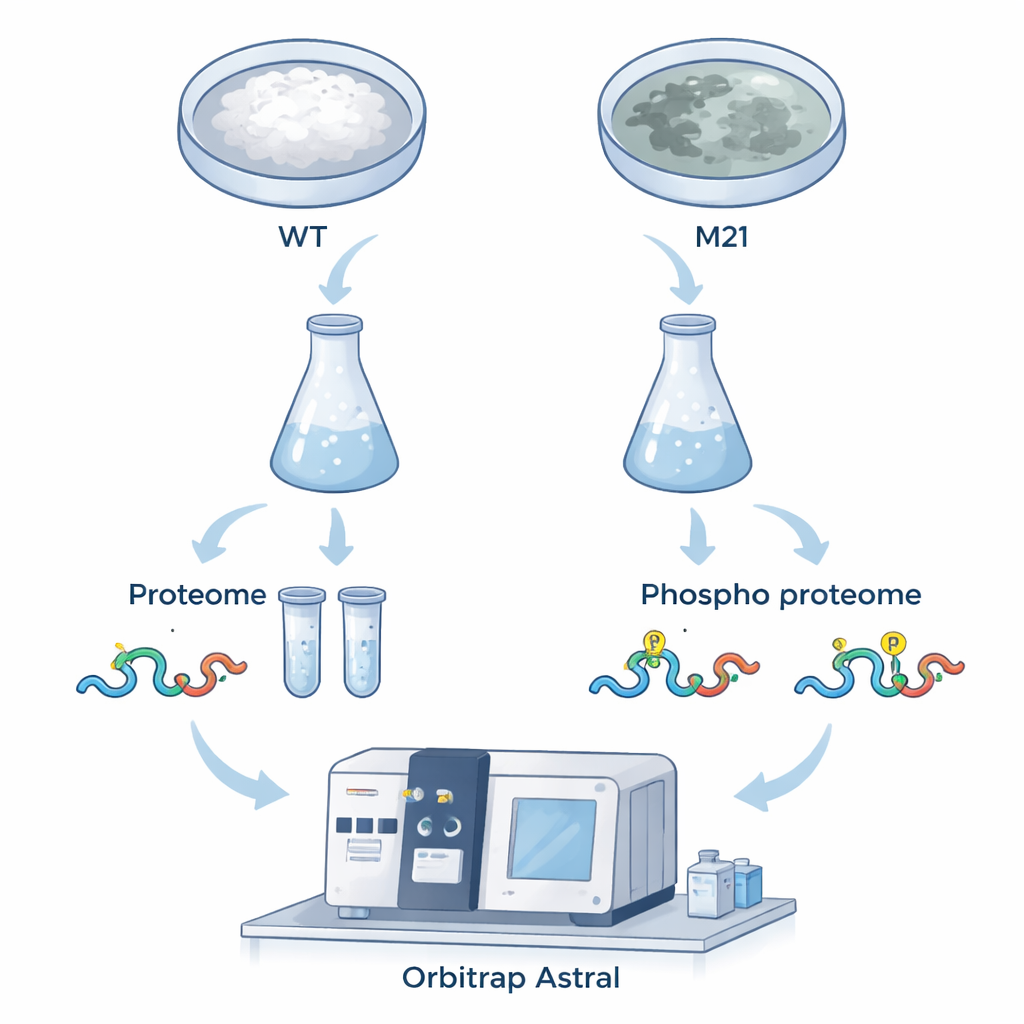
Desplazamientos en el uso de energía y el reciclaje celular
Cuando los investigadores examinaron qué tipos de proteínas cambiaron, surgieron dos temas principales: el metabolismo de los lípidos de membrana y un proceso de “autodigestión” llamado autofagia, que las células usan para reciclar componentes y sobrevivir al estrés. Muchas proteínas implicadas en glicerofosfolípidos —los componentes de las membranas celulares— y en vías energéticas relacionadas resultaron alteradas. Las proteínas vinculadas a la autofagia mostraron cambios especialmente marcados en sus patrones de fosforilación, lo que sugiere que MoPah1 afecta no solo cómo se sintetizan y degradan las grasas, sino también cómo el hongo recicla su propio material durante el crecimiento y la infección. Un subconjunto de 72 proteínas cambió tanto en cantidad como en estado de fosforilación, lo que las marca como candidatas principales para el control directo o indirecto por MoPah1.
Encontrar los socios proteicos de MoPah1
Para ir más allá de las correlaciones, el equipo preguntó qué proteínas se unen físicamente a MoPah1. Produjeron una proteína MoPah1 fusionada a un “asa” (GST) en bacterias, y luego la usaron como cebo para pescar proteínas interactoras en extractos fúngicos. La espectrometría de masas identificó 183 candidatas, muchas de las cuales se agrupan en grandes complejos proteicos, lo que refuerza la idea de que MoPah1 se sitúa en el centro de extensas redes celulares. Entre estos socios, destacó una proteína: Pmk1, una proteína de señalización clave en la vía MAPK que controla la formación del apresorio, el crecimiento dentro de la planta y las respuestas al estrés. Pruebas adicionales con el sistema de dos híbridos en levadura confirmaron que MoPah1 y Pmk1 pueden interactuar directamente.
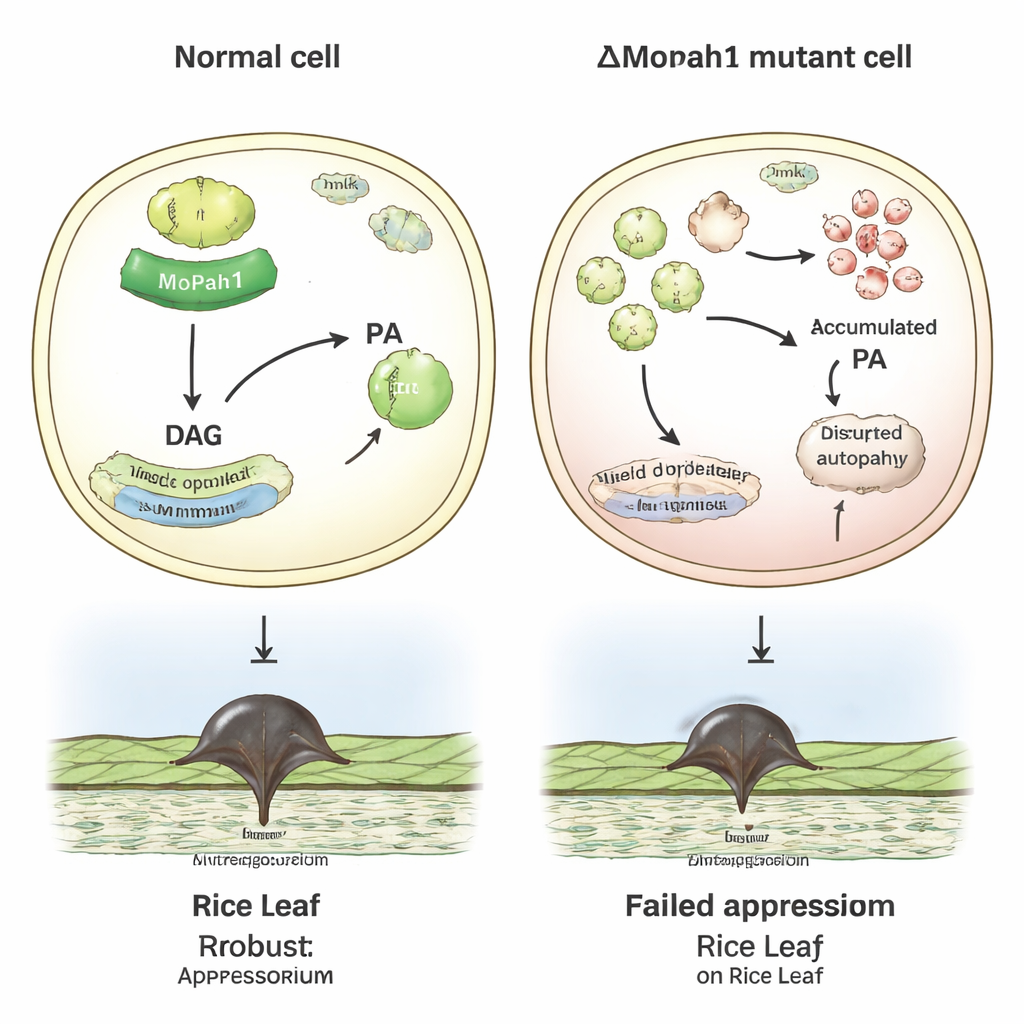
Vinculando el control de las grasas con las señales de infección
Poniendo estas piezas juntas, los autores proponen que MoPah1 ayuda a ajustar tanto el equilibrio de los lípidos de membrana como las principales rutas de señalización en Magnaporthe oryzae. En los hongos sin MoPah1, alteraciones amplias en el metabolismo lipídico, el reciclaje de proteínas y la señalización MAPK parecen socavar la formación y la eficacia de las estructuras de infección necesarias para penetrar las hojas de arroz. Aunque el estudio se limitó a muestras de micelio —porque el mutante no puede formar esporas—, aún proporciona un recurso rico de datos de proteínas y fosforilación, además de una lista reducida de proteínas que probablemente trabajen junto a MoPah1. Para los no especialistas, la conclusión clave es que controlar una sola enzima en un patógeno de cultivos puede propagarse por muchos sistemas celulares, ofreciendo nuevos enfoques para comprender, y quizás algún día interrumpir, al hongo que amenaza a una de las fuentes alimentarias más importantes del mundo.
Cita: Zhao, J., Yang, L., Shi, X. et al. Orbitrap Astral–based proteome and phosphoproteome analysis identifies candidate proteins associated with the phosphatidate phosphatase MoPah1 in Magnaporthe oryzae. Sci Rep 16, 6901 (2026). https://doi.org/10.1038/s41598-026-36940-1
Palabras clave: hongo de la roya del arroz, Magnaporthe oryzae, redes proteicas, metabolismo de lípidos, patogenicidad fúngica